Yleistä
muskariinireseptoreihin vastaa luonnollisen ligandin asetyylikoliini on laajalle levinnyt kudoksiin jakautumisesta ja ovat mukana valvonnassa lukuisia keski-ja reuna-fysiologisia reaktioita, sekä merkittävä lääkkeen kohde-ihmisen sairaus. Jo jonkin aikaa on tiedetty, että tämä g-proteiineihin kytkettyjen reseptoreiden perhe koostuu viidestä M1-M5: ksi nimetystä jäsenestä . Geeniperhe kokonaisuudessaan näyttää 26.,3% yleinen aminohappo identiteettiä, vaihtelu-reseptorin alatyyppejä on nähnyt pitkälti sisällä solunsisäinen silmukoita. Kolmas solunsisäinen silmukka on erityisen muuttuja, osoittaa vain 2,7% identiteetin välillä reseptorin, verrattuna keskimäärin 66% identiteetin löydy säilytetty, jotka toimivat aloilla. Klassisesti nämä reseptorit jaetaan kahteen laajaan ryhmään, jotka perustuvat niiden ensisijaiseen kytkentätehokkuuteen G-proteiineihin., Näin ollen, M2 ja M4-muskariinireseptoreihin osaa pari pertusiss-toksiini herkkä Gi/o-proteiineja, ja M1, M3 ja M5-muskariinireseptoreihin pari Gq/11-proteiineja . Se on kuitenkin selvää, että muskariinireseptorin perhe voi pari laajan valikoiman erilaisia signalointireittien, joista välittyvät G-proteiinien ja muut, jotka ovat G-proteiini-riippumaton .
Muskariinireseptorin farmakologian
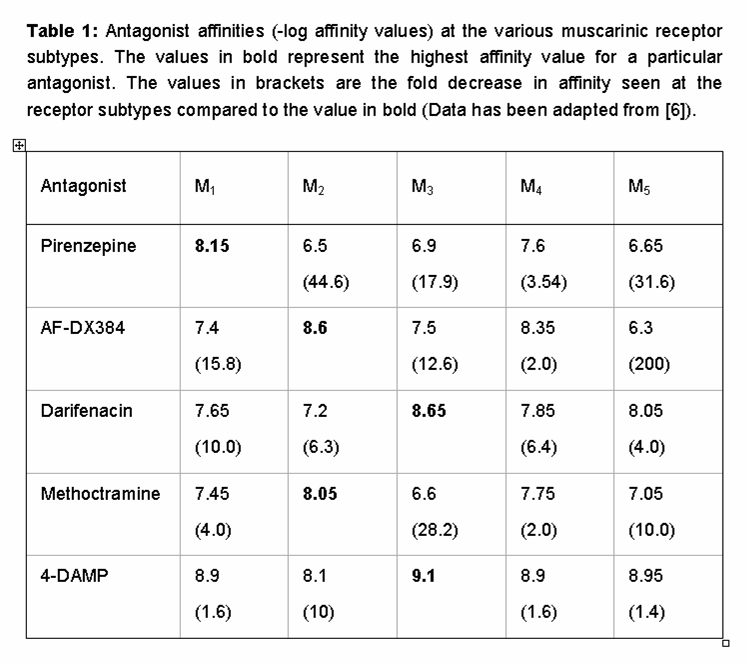
orthosteric sitova tasku muskariinireseptorin perhe on hyvin säilytetty, jolloin kehitys alatyyppi-spesifisiä agonisteja ja antagonisteja, hyvin vaikeaa., Taulukossa 1 on esitetty sitoutumisaffiniteetit joitakin yleisimmin käytetty muskariinireseptorin ligandien ja korostaa vaatimaton määrin alatyyppiä spesifisyys näitä aineita. Jos pirentsepiiniä, esimerkiksi, tämä antagonisti on 44-kertainen selektiivisyyden M1-muskariinireseptorin yli M2 , mutta vain 17.9 ja 3,5 kertaisen selektiivisyyden M3 ja M4-muskariinireseptorin alatyyppejä vastaavasti . Samoin, darifenasiini, joka on laajalti pidetään M3 valikoiva ja on hyväksytty kliiniseen käyttöön hoidossa yli-aktiivinen rakko on enintään 10-kertainen valikoivuus yli M1/M4/M5-reseptoreihin .,
Yrittää tuottaa uusia muskariini ligandien on viime aikoina keskittynyt kehittämiseen allosteerinen sääntelyviranomaisten, jotka toimivat non-sivustot säilytetty ja näin ollen tarjota mahdollisuus alatyyppi valikoivuus . Kohdentamalla allosteerinen sivustoja muskariinireseptoreihin, sisälsi solunulkoisen silmukoita ja solunulkoisen alueilla läpäisevä heliksejä , allosteerinen modulaattori pystyvät säätelemään sitova affiniteetti ligandien klo orthosteric sivuston., Esimerkiksi läsnäolo allosteerinen modulaattori thiochrome affiniteetti asetyylikoliinin klo M4-muskariinireseptorin on lisääntynyt, mutta affiniteetti asetyylikoliinin muiden muskariinireseptorin alatyyppejä on ennallaan . Lisäksi alatyyppi-agonisteja, jotka sitoutuvat ja aktivoi reseptorin kautta sitovia verkkotunnuksia erillään orthosteric sitova sivusto on myös raportoitu. Näitä ovat erittäin M1-selektiiviset allosteriset agonistit AC-42 ja TBPB ., Nämä romaani agonisteilla on huomattavaa terapeuttista potentiaalia, mutta miten niiden merkinanto-ominaisuuksia verrata orthosterically toimivat agentit ovat vasta alkaneet tutkia .
Näin ollen mahdollinen terapeuttinen hyöty allosteerinen modulaattori/agonistit on, että ne osoittavat alatyyppi valikoivuus tavalla, joka ei ole saavutettavissa kanssa orthosteric ligandien. Lisäksi allosteerinen modulaattori, jotka toimivat säätelemällä affiniteetti luonnollinen ligandi on mahdollisuus olla aktiivinen vain, milloin ja missä asetyylikoliini on läsnä ja näin ollen vähentää mahdollisia sivuvaikutuksia .,
Muskariinireseptorin fysiologinen rooli
rooli muskariinireseptoreihin supistuminen sileän lihaksen, erityisesti hengitysteiden, sykkyräsuoli, iris ja virtsarakon, pidetään klassisen muskariini vastaus välittyy ensisijaisesti M3-muskariinireseptoreihin ilmaistuna sileän lihaksen soluissa . Co-ilmaista M3-muskariinireseptoreihin sileä lihas on usein suurempi väestö M2-muskariinireseptoreihin, jotka näkyvät pelata paljon pienempi rooli sileän lihaksen supistuvien vastaus ., Sen sijaan, M2-muskariinireseptoreihin ilmaistuna sydän on merkittävä rooli valvoa sydämen myosyyttien supistuminen . Täällä asetyylikoliinin vapautumista vagaalinen parasympaattisen hermosoluissa vähentää sydän lyö taajuudella lähes yksinomaan toimii tällä M2-muskariinireseptoreihin . Eksokriininen eritys, etenkin syljen , ja kuten näkyy, viime aikoina, insuliini , on ensisijaisesti välittyy M3-muskariinireseptoreihin pienempi rooli M1-reseptoreita erityisesti pelastus .,
sukupolven siirtogeenisiä muskariinireseptorin knockout-hiirillä, missä M1-M5 geenit ovat olleet ablated, on paljastanut lukuisia romaani muskariinireseptorin toimintoja . Muskariinireseptorin knockout-hiiret ovat elinkelpoisia ja hedelmällisiä ilman merkittäviä fysiologisia vikoja, mikä mahdollistaa näiden reseptorien fysiologisen roolin tutkimisen aikuisilla hiirillä in vivo. Erityisen kiehtovia ovat olleet havaitut lukuisat käyttäytymis-ja neurologiset fenotyypit, jotka paljastavat tämän reseptoriperheen tärkeän neuromodulatorisen roolin., M1-muskariinireseptorin knockout-hiirillä osoittaa voimakas kasvu liikeaktiivisuutta , joka on ehdotettu vaikutus muistiin ja oppimiseen, ja se voi tarjota mallin oppimisen alijäämät ehtoja, kuten adhd . Edelleen liikuntaelinten fenotyypit ovat havaittu M4-muskariinireseptorin tyrmäys eläimiä, missä tämä reseptorin alatyypin on ajateltu välittävän estävä vaikutus striatumin dopamiini-välitteisen liikeaktiivisuutta ., M2-muskariinireseptoreihin ilmaistu thermo-sääntely-keskuksia hypotalamuksen ovat todennäköisesti mukana sääntelyn kehon lämpötilaa , kun taas M3-muskariinireseptoreihin on raportoitu moduloida ruokahalu asetuksella melaniinin-keskittämällä hormoni (MCH) hermosoluissa hypotalamuksen feeding centre .,
muskariinireseptoreihin kuten huumeiden tavoitteet
Mukaisesti ymmärrystä neuromodulatory rooli muskariinireseptoreihin on tullut keskittyä enemmän mahdollisuus, että tämän reseptorin perhe voi olla tehokas terapeuttinen tavoitteiden useita neurologisia ja psykiatrisia sairauksia . Historiallisesti tämä painopiste on keskittynyt Alzheimerin tauti, joka liittyy menetys kolinergisen hermotuksen aivokuori ja hippokampus, ja on tällä hetkellä hoitaa parantaa kolinergisen neurotransmission kautta farmakologinen esto koliiniesteraasin aktiivisuus., Ottaa huomioon, että vuosia, tämä hoito oli ajatellut pitää sen hyödyllisiä vaikuttaa stimulaation M1-muskariinireseptorin alatyyppi , työ M1-reseptorin knockout-hiirillä on ehdottanut, että tämän reseptorin alatyypin voi pelata niin tärkeä rooli kognition kuin aiemmin on ajateltu . Näin ollen romaanin anti-Alzheimerin tauti lääkkeitä, jotka kohdistuvat muihin muskariinireseptorin alatyyppejä, kuten M2-, M4 – ja M5-muskariinireseptoreihin, ovat nyt alle voimakkaampi huomioon., Mielenkiintoista, muskariinireseptorin modulaatio dopaminergisen transmission on antanut pontta kehittämiseen muskariinireseptorin ligandien hoitoon skitsofrenia ja Parkinsonin tauti . Molemmissa tapauksissa painopiste on ollut M1-ja M4-muskariinireseptoreihin, jossa se on ilmoittanut, että agonistit näihin reseptoreihin saattaa olla hyötyä skitsofreniaa ja antagonistit ovat todennäköisesti hyötyä Parkinsonin tauti.,
lisäksi terapeuttista potentiaalia kohdistaminen tiettyyn muskariinireseptoreihin KESKUSHERMOSTON häiriöt on edelleen huomattavaa terapeuttista potentiaalia kehittämiseen muskariini ligandien enemmän klassisen muskariini-keskitetty tauti tavoitteet. Esimerkiksi, kun kyseessä on krooninen keuhkoahtaumatauti (COPD) ja astma, jotka ovat tällä hetkellä käsitellä ei-selektiivinen muskariinireseptorin antagonisteja ipratropium ja tiotropium saattaa olla merkittävää kliinistä hyötyä kehittäminen valikoiva M2-ja M3-muskariinireseptorin ligandien., Samoin yliaktiivisessa virtsarakossa muskariinireseptoriligandien parempi selektiivisyys auttaisi vähentämään ei-toivottuja sivuvaikutuksia . Taulukossa 2 (mukautettu viitearvosta ) on luettelo sellaisten yhdisteiden mahdollisista terapeuttisista sovelluksista, jotka kohdistuvat erityisesti muskariinireseptorin alatyyppeihin.
