Ensin pitää tietää valenssielektronien määrä. Voit tehdä tämän (1) piirustus electron kokoonpano per elementti tai (2) konsultointi jaksollisen.,
Jos päätät piirtää electron kokoonpano per elementti, sinulla on jotain, kuten tämä:
#N# (järjestysluku = 7) : #1s^2# #väri (punainen) (2s^2)# #väri (punainen) (2p^3)# (5 syrjäisimpien elektronit)
#O# (järjestysluku = 8) : #1s^2# #väri (punainen) (2s^2)# #väri (punainen) (2p^4)# (6 syrjäisimpien elektronit)
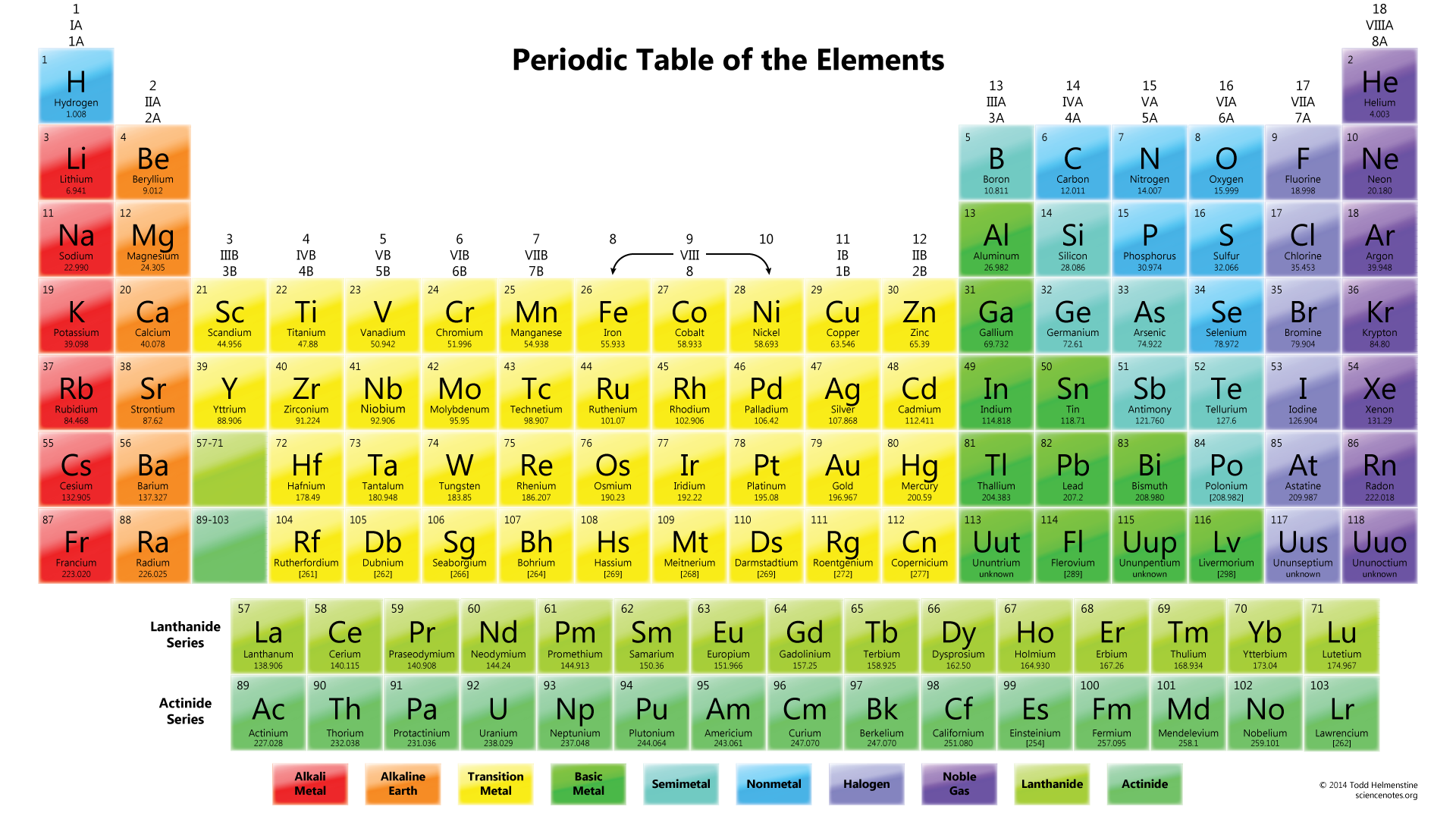
Jos valitsit ota yhteys jaksollinen, vain huomata, että #N# kuulua Ryhmään 5A, kun #O# kuuluu Ryhmä 6A. Ryhmän numero tarkoittaa määrä syrjäisimpien elektronit.,
Nyt kun tiedät määrä valence elektronit per elementti, sinun täytyy laskea kokonaispinta-valence elektroneja varten #NO_3^”-1″# ion.
5 + (3 x 6) = 23 elektronia
, mutta koska koko molekyylillä on -1 varaus, sinun on lisättävä myös tämä. Valenssielektroneja on siis yhteensä 24.
seuraavaksi arvotaan. Normaalisti kemiallisen kaavan ensimmäinen alkuaine on keskusatomi. Tällöin# n # atomia ympäröi kolme# O # atomia.,
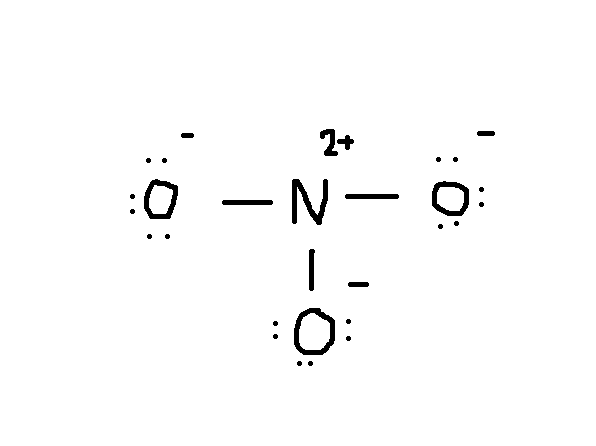
Huomaa, että yksinäinen pari elektroneja #O# ovat myös mukana kuvassa. Jos lasket elektronien kokonaismäärän edellä olevaan piirustukseen, se on jo 24 elektronia (yksi rivi laskee 2 elektronia). Mutta tämä piirustus on rikkonut oktetti sääntö, koska keski-atom on vain 6 elektronit sen sijaan oikea numero 8. Joten mitä tehdä?
Lisää toinen side, mutta missä?,
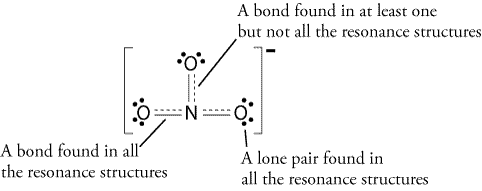
näin Ollen, resonanssi rakenne näyttää tältä: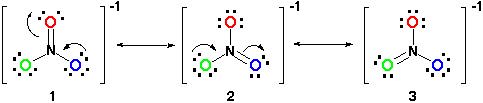
Kaikki resonanssi rakenteita ovat oikein, koska se kaikki seuraa oktetti sääntö ja kaikki on yhteensä 24 elektroneja. Huomaa vain, että ainoa sidoksen liikuttaja on pi (#pi#) – sidos tai maallikon termillä kaksoissidos ja yksi elektronipareista #O# atomista.