OSS Pharm. 2012;37(12):HS1-HS8.
SAMMENDRAG: Som narkotika eksperter, farmasøyter arelooked ved å gi riktig veiledning for behandling av acutebacterial peritonitis i sykehus. Akutt bacterialperitonitis er forbundet med en høy risiko for dødelighet. Immediateintervention er nødvendig, som forsinkelse kan tillate en gang-lokalisert diseaseprocess å skade andre organer i hele kroppen. Appropriateidentification og behandling av akutt bakteriell peritonitt er tastene tobetter utfall., I tillegg til kirurgisk inngrep, pharmacologictreatment er også nødvendig. Behandling eller forebygging av hypovolemiaassociated med peritonitis kan gjennomføres per recommendationsof den Surviving Sepsis Campaign retningslinjer. Til slutt, siden antibiotictherapy er den tredje hjørnesteinen i behandlingen, er det viktig toconsider det riktige valget, dosering og varighet av antibiotika.
Peritonitis er en akutt betennelse i peritoneallining på grunn av bakteriell infeksjon så vel som av andre årsaker, slik aschemicals, bestråling, og utenlandske organ skade.,1 Krenkelse av peritoneal foring av noen av disse stoffene kan føre til en inflammatorisk respons, kjent som akutt peritonitt.1 TABELL 1 viser vanlige patogene etiologien av akutt bakteriell peritonitt.
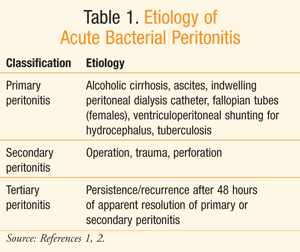
Dødelighet forbundet med peritonitis var around90% i begynnelsen av 1900-tallet. Disse prisene har siden kommet ned toapproximately 30% med bruk av egnet medikament behandling andsupportive omsorg.2
Sykdom Oversikt
Klassifisering av bakteriell peritonitt er basert på kilden av smittsomme bakterier.,2 Primær-eller spontan peritonitisrefers til en extraperitoneal etiologi, der smittsomme bacteriaenter peritoneal cavity gjennom sirkulasjonssystemet eller lymphaticsystem.1,2 I disse tilfeller, pasienten vanligvis har en underliggende comorbidity som kan føre til bakteriell overføring til peritoneum.1Such comorbidities kan omfatte ascites og iboende peritonealdialysis katetre. Primære peritonitis er anslått til å skje i 10% to30% av pasienter med alkoholholdige cirrhose.,1 i Tillegg,pasienter på kronisk oppegående peritoneal dialyse (CAPD) har, onaverage, én forekomst av peritonitis hver 33 måneder.1
Sekundær peritonitis, den mest vanlige etiologi, er resultatet av smittsomme bakterier fra en kilde i bukhinnen.1Considering mengde mikroflora eksisterende innenfor abdominalorgans, overføring av bakterier fra noen av de organer i thesterile bukhinnen kan føre til en inflammatorisk respons, noe som resulterer insecondary peritonitis. Spredning av bakterier fra sin vert organer mayresult fra punktering på grunn av traume, kirurgi, eller perforering.,1 Sårdannelse, iskemi, eller obstruksjon kan føre til perforasjon av abdominale organer.1 Endelig, tertiær peritonitisis vedvarende eller tilbakevendende peritonitis som igjen minst 48 hoursafter tilsynelatende oppløsning av en primær eller sekundær peritonitis.2 Data på forekomst av sekundær og tertiær peritonitis er begrenset.1 Klassifisering av peritonitis er nyttige i klinisk praksis som det kan bidra til å tilrettelegge for riktig diagnose og behandling.,
Klinisk Presentasjon og Diagnostikk
Bakteriell innføring i bukhinnen resulterer i en umiddelbar humoral og cellulær immunrespons.1This svar utløser en inflammatorisk prosess, noe som resulterer i fluidshifts i peritoneal cavity. Dette væskeopphopning, sammen withdecreased intestinal motilitet, fører ofte til abdominal oppblåsthet.I tillegg, væske vekt i magen, kjent som tredje alternativet,kan resultere i redusert blodvolum, som fører til hypovolemia i severecases., Feber, oppkast og diaré kan også følge peritonitis,compounding væske ubalanser og øker risikoen for hypovolemia.Ubehandlet hypovolemia kan resultere i redusert minuttvolum, og,til slutt, hypovolemic sjokk.1
I tillegg til væske skift, utenlandske stoffer asfeces og slim tilstede i bukhulen kan forverre peritonitisby svekke immunforsvaret mekanismer som for eksempel bakterielle phagocytosis.1Bacterial og endotoksin absorpsjon i blodet er facilitatedby en betent bukhinnen og kan føre til sepsis., Døden kan resultfrom negative effekter på organsystemer fra alvorlige komplikasjoner som sepsis. I tillegg, andre alvorlige komplikasjoner, slik ashypoalbuminemia forårsaket av protein tap samt pulmonarycomplications som lungebetennelse som følge av diaphragmatic hemming dueto splinting, kan forverre prognosen. Sammen med verten immunitet andtreatment tilstrekkelighet, mengde og virulence infisere organismer andthe tilstedeværelse av utenlandske stoffer i bukhulen har astor innvirkning på den resulterende utfallet av bukhinnebetennelse.,1
uspesifikke kliniske presentasjon av primaryperitonitis varierer drastisk fra den iøynefallende presentasjon ofsecondary peritonitis.1 i Motsetning til videregående peritonitis, primaryperitonitis kan utvikle seg over flere uker, uten noen tegn til acutedistress. Selv om pasienten kan klage over abdominal ømhet,kvalme, oppkast eller diaré, primær peritonitis er vanligvis firstsuspected når dialysate vises skyet hos pasienter undergoingperitoneal dialyse eller når encefalopati forverres hos pasienter withcirrhosis., Laboratoriet funn etter mistanke om primaryperitonitis kan vise mild heving av den hvite blodceller (WBC) countand en positiv kultur for peritoneal dialysate eller asketiske væske.1
I motsetning til pasienter med sekundær peritonitis oftenpresent med en boardlike magen, abdominal oppblåsthet, svak bowelsounds som reduseres over tid, og uutholdelige magesmerter thatleads til ufrivillig vokter, med liten bevegelser som breathingor rocking av sengen forårsaker sterke smerter., Som tidligere nevnt,hypovolemia kan oppstå i fravær av behandling, som kan ultimatelyresult i hypotensjon og sjokk. Andre tegn og symptomer includetachypnea, takykardi, kvalme og oppkast, redusert urin utgang, andelevated temperatur.1 I videregående peritonitis, laboratorieprøver kan vise leukocytosis, med dominerende neutrofiler og forhøyet band.1
Behandling av Peritonitis
De ønskede resultatene i peritonitis inkluderer oppløsning av den underliggende etiologi og drenering av abscesser.,1Secondary mål for behandling inkluderer eliminering av infeksjon andprotection mot uønskede stoffet hendelser så vel som ende-organskade,herunder at til lunger, lever, hjerte og nyrer.1Elements av riktig intervensjon består av væske-og lungeredning,source control prosedyre (kirurgi), og empiriske antimikrobiell behandling.3Most tilfeller av primær peritonitis krever bruk av antimicrobialagents som bærebjelke i terapi, og drenering prosedyrer vanligvis arenot nødvendig.1
Sekundær peritonitis krever kirurgisk behandling, kjent som kilde kontroll, for å korrigere underliggende patologi.,1 Sourcecontrol har til hensikt å korrigere anatomiske derangements, fjerne infectiousfoci, og kontrollere faktorer fremme pågående infeksjon.4Specific faktorer som sannsynligvis vil være til hinder for en vellykket kilde controlinclude en forsinkelse på mer enn 24 timer før prosedyren, en AcutePhysiology og Kroniske Helse-Evaluering (APACHE) score på minst 15;alder >70 år, tilstedeværelse av comorbidity; lav albumin nivå; poornutritional status; diffuse peritonitis, og tilstedeværelse av malignitet.,3 Mislyktes source control er angitt med tilbakevendende infeksjon på stedet, anastomotic feil, eller fistel dannelse.3 Perkutan -, bilde-guidet drenering er foretrukket over kirurgisk drenasje, spesielt når infeksjonen er godt lokalisert.1,3
Hypovolemia i innstillingen av peritonitis kan føre toorgan feil. Derfor, uavhengig av tilstedeværelse av septisk sjokk,rask væske-og lungeredning er garantert i alle pasienter med peritonitisin for å fremme fysiologiske stabilitet.,3 Mer aggressiverestoration av intravaskulært volum bør gis til de withseptic sjokk og orgel svikt i den måten som er beskrevet i SurvivingSepsis Kampanje retningslinjer for håndtering av septisk sjokk.3 The2012 oppdateringer til Surviving Sepsis retningslinjer vil angivelig statethat den første væske utfordring bør være minst 1 L av crystalloid,og et minimum av 30 mL/kg i de første 4 til 6 timer. Inkrementell fluidboluses kan følge så lenge pasientens vitale tegn fortsette å showimprovement.,5 Noradrenalin er foretrukket vasopressor,og dobutamine inotropic terapi kan legges til pasienter withcardiac dysfunksjon.5 Kontinuerlig hydrocortisone infusiontotaling 200 mg/24 timer er anbefalt for de withvasopressor-ildfaste septisk sjokk. Feber, tachypnea, kvalme andvomiting, og redusert inntak av væske kan føre til dehydrering i patientswith peritonitis.3
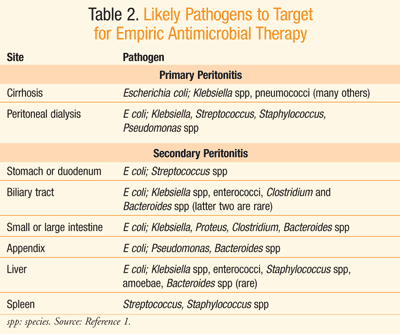
Empirisk antibiotikabehandling bør initieres ved mistanke om peritonitis.,3Practice retningslinjer fra Smittsomme Sykdommer Society of America(IDSA) anbefaler at empiric antimikrobiell behandling initieres withinthe første timen av anerkjennelse av peritonitt hos pasienter withcompromised hemodynamisk eller organ funksjon; ellers, terapi bør beinitiated innen 8 timer av presentasjonen.3 Selv om det islimited verdi til blod kulturer i behandling av samfunnet-acquiredperitonitis, Gram flekker for å oppdage tilstedeværelsen av gram-positive coccior gjær er ivaretatt i høy-risiko enkeltpersoner så vel som i de withhealth vare–ervervet peritonitis.,3 antibiotikabehandling kan bealtered på resultater fra kultur-og følsomhet data. I utgangspunktet,men IV empiric antibiotikum utvalget bør målet sannsynlig organismspresent på stedet som peritonitis ble utledet, som vist i TABELL 2.1
Det er forskjeller mellom helse–forbundet og samfunnet-assosierte infeksjoner (TABELL 3).,3,6 Aminoglykosider er blant de representanter som er anbefalt for bruk i empiricalantimicrobial terapi for helse–forbundet complicatedintra-abdominal infeksjoner, særlig de som er forårsaket byEnterobacteriaceae organismer som produserer utvidet-spectrumbeta-lactamases (esbl-er, skal).3 Vankomycin er anbefalt i samme situasjon når meticillin-resistente Staphylococcus aureus (MRSA) er den utløsende organismen av helse–forbundet infeksjon.3 Theorigination av smitte i form av anatomiske området som godt assetting (dvs.,, sykehus eller samfunnet) som hjelper utvalg av mostreasonable empirisk antibiotikabehandling.

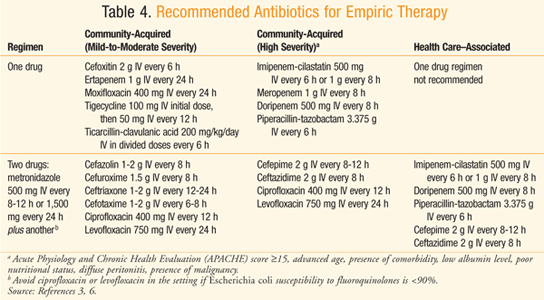
TABELL 4 viser den anbefalte empiriske antibiotikum regimer for pasienter med peritonitis som har normal nyre-og lever-function3,6 eller en kreatininclearance mellom 70 og 100 mg/dL.7 Vurderer den økende motstanden av Escherichia coli å kinoloner, slike medisiner bør bare brukes i et sykehus som undersøkelsen indikerer >90% mottakelighet av E coli å kinoloner.,3 Det er også bekymring over den hyppige bruken av ertapenem fører til fremveksten av carbapenem-resistente Enterobacteriaceae organismer og Pseudomonas og Acinetobacter arter.3 Ampicillin-sulbactam bør unngås når du målretter E coli, med tanke på utbredelsen av motstand mot stoffet.,3,8 Når en helse-omsorg–forbundet infeksjon er av interesse, det er en høyere risiko for infeksjon på grunn av Candida-og Enterococcusspecies, Fluconazole garanteres hos pasienter som har en malignitet,transplantasjon, inflammatorisk sykdom, tilbakevendende intra-abdominal infeksjoner,magesår på syre undertrykkelse, eller er på immundempende therapyfor neoplasm.3 Ampicillin eller vankomycin kan legges toempiric terapi for å målrette enterokokker i de med helse–forbundet infeksjon, spesielt når det er en postoperativeinfection.,3 Pasienter er kjent for å være kolonisert med MRSAand de med helse–forbundet peritonitis bør behandles withan antimikrobielle som dekker MRSA, som vancomycin.3
Det er bestemt antimikrobielle dosering hensyn for pasienter som er kritisk syke og/eller overvektige.9Due til fysiologiske endringer i disse pasientene, certainpharmacokinetic faktorer kan være endret, slik som tilsynelatende volumet ofdistribution og/eller klaring.,3 i Tillegg, hvis dosageis avhengig av nyrefunksjon, kreatinin clearance kan ha å bedirectly målt på grunn av problemer med estimering knyttet toabove-gjennomsnittlig kroppsvekt.3 Kritisk syke pasienter kan alsoexperience endringer i visse farmakokinetiske parametre. Forexample, pasienter i de tidlige stadier av sepsis kan oppleve ahypermetabolic staten og skift væske som kan føre til økt volum ofdistribution og fortolling.3 Slike skift kan resultere i lavere serum konsentrasjoner av antimikrobielle midler som beta-lactamer.,3On en lignende merk, redusert serum konsentrasjoner av antimikrobielle midler som cefalosporiner og carbapenemer har vært observert hos overvektige pasienter.3As et resultat av slike farmakokinetiske endringer, justeringer som higherdoses og/eller hyppigere administrasjonen kan være nødvendig i thesesubgroups av pasienter.3 I tilfeller hvor vankomycin er anappropriate agent for kritisk syke og/eller overvektige pasienter, total kroppsvekt bør brukes ved beregning av den første dosen.3 i Tillegg, disse pasientene bør ha serum vancomycin konsentrasjon overvåkes for å kunne gi individuell dosering.,3,10
Intraperitoneal dosering er foretrukket over IV dosering forpatients på peritoneal dialyse for å gi høyere lokalt nivå ofantibiotics. Empirisk behandling må dekke både gram-positive andgram-negative organismer kjent for å forårsake peritonitis. Intraperitonealantibiotics kan bli gitt gjennom kontinuerlig dosering eller intermittentdosing. Dosering regimer bør tas hensyn til gjenværende renalfunction, definert som >100 mL/dag urin utgang, som caserecommended doser bør være empirisk økt med 25%.,11Dwell-time exchange bør være minst 6 timer hvis du bruker intermittentdosing. Den anbefalte varigheten av behandlingen er 2 uker, eller 3 uker i mer alvorlige tilfeller. Behandlingen er avhengig av klinisk respons, whichshould sees innen 72 timer etter initiering av behandling med antibiotika.Pasienter med overskyet avløpsvann etter 4 til 5 dager i appropriateantibiotic terapi er antatt å ha ildfast peritonitis og shouldhave deres kateteret fjernes.11
Akutt nyresvikt er den viktigste prediktor for død blant pasienter med spontan bakteriell peritonitt (SBP).,12Albumin har vært brukt i SBP til å føre plasma volum ekspansjon i orderto redusere forekomsten av nyresvikt hos pasienter med cirrhosisundergoing stort volum parasentese.13 En studie evaluatingthe bruk av IV albumin i tillegg til antimikrobiell behandling versusantimicrobial terapi alene hos pasienter med cirrhose og SBP resultedin en redusert forekomst av nyresvikt og redusert dødelighet.,13It ble det funnet at pasienter som ble behandlet var mest sannsynlig å benefitfrom albumin hvis de hadde serum bilirubin nivåer >4 mg/dL, serumcreatinine >1 mg/dL, og en blod-urea-nitrogen (BUN) konsentrasjon>30 mg/dL.13 En annen studie bekreftet previouslyreported funn og brukt samme dosering på 1,5 g/kg administreres onthe første dag og 1 g/kg administreres på den tredje dag.,14Presently, det er ikke nok data til å støtte bruk av albumin inneliggende pasienter med komplisert SBP, eller med et serum bilirubin <4 mg/dL anda kreatinin av <1 mg/dL. Den Europeiske Foreningen for Studier ofthe Leveren sier at flere studier er nødvendig for å vurdere theefficacy av albumin og andre volum utvidere i forvaltningen av KOLLEGAPROGRAMMET.15
Antimikrobiell behandling bør være begrenset til 4 til 7 dager.3 Hvis tegn og symptomer på peritonitt har løst på denne tiden, antibiotika er ikke lenger anbefalt.,3If pasienten er på bedringens på denne tiden, kan tolerere en muntlig kosthold,og ikke viser motstand, step-down terapi med oralantibiotics garanteres.3 Antibiotika som anbefales i thissetting inkluderer moxifloxacin, en kombinasjon av metronidazole med eitherlevofloxacin eller en muntlig cephalosporin, eller amoxicillin-clavulanate.Disse orale midler kan også brukes for de som er behandlet i theoutpatient innstilling, men ble initiert på institusjon IV terapi.,3
feil Behandling etter 4 til 7 dager etter behandling bør beinvestigated gjennom passende imaging teknikker som CT-scan orultrasound.3 Antimikrobiell behandling effektiv mot initialorganisms bør videreføres og ekstra-abdominal kilder til infectionshould utelukkes hos pasienter som er nonresponsive til terapi.Aerobe og anaerobe kulturer er anbefalt for pasienter withinfection gjenværende etter første behandling.3
Bestemt pasient bestander bør vurderes forprophylaxis av bakterielle peritonitt., Primær bakteriell peritonitt canbe forhindret ved hjelp av antibiotika hvis det er en kjent risikofaktor. Forexample, en enkelt IV dose av vankomycin 1 g gitt ved den tid ofcatheter plassering i pasienter som gjennomgår peritoneal dialyse kan helpprevent bakteriell peritonitt.11 Et alternativ til vankomycin er en enkelt dose av cefazolin 1 g IV.11Secondary bakteriell peritonitt profylakse bør vurderes inneliggende pasienter med cirrhose som er innlagt for øvre GI-blødning.,12i det siste, norfloxacin 400 mg daglig hadde vært stoffet av valget i innstillingen av øvre GI-blødning; imidlertid, alternativ antimicrobialshave siden vært betraktet som på grunn av epidemiologiske endringer av bacterialinfections i cirrhose.12 Ceftriaxone 1 g IV har vist seg å være et effektivt alternativ.16
Konklusjon
Peritonitis, en akutt betennelse i bukhinnen, canoccur på grunn av patogener eller andre årsaker som for eksempel kjemisk eksponering.Klinisk presentasjon av primære peritonitis er ofte uspesifikke andmay mangel første tegn og symptomer., Omvendt, sekundær peritonitisoften presenterer med fremtredende symptomer, inkludert alvorlig smerte. Untreatedperitonitis kan resultere i sepsis og ende-organskade; derfor,be til behandling av bakteriell peritonitt bør styres av specificetiology og comorbidities.
Vanlige antimikrobielle midler av valget for samfunnet-acquiredperitonitis inkluderer cefalosporiner og fluorokinoloner. Helse–ervervet peritonitis kan kreve behandling med bredt spectrumantimicrobials som carbapenemer., Pasienten egenskaper må beconsidered i dosering beslutninger, og enkelte pasient undergrupper slik asthe kritisk syke og/eller overvektige kan kreve dosejustering på grunn tovariations i farmakokinetiske parametre. I tilfeller av nonresponse toempirical terapi, infeksjonskilder utsiden av magen bør beconsidered. I alle tilfeller av peritonitis, støttende omsorg bør beadministered som angitt i for å minimere komplikasjoner.
1. Dipiro JT, Howdieshell TR. Intraabdominal Infeksjoner. I: Dipiro JT, Talbert RL, Yee GC, et al, red. Behandling Med Legemidler: En Pathophysiologic Tilnærming. 8th ed., New York, New York: McGraw-Hill; 2011.
2. Ordonez CA, Carlos J. Forvaltning av peritonitis i den kritisk syke pasienten. Surg Clin North Am. 2006;86:1323-1349.
3. Solomkin JS, Mazuski JE, Bradley JS, et al. Diagnosisand styring av kompliserte, intra-abdominal infeksjoner hos voksne andchildren: retningslinjer ved Kirurgisk Infeksjon Samfunnet og theInfectious Diseases Society of America. Clin Infisere Dis. 2010;50:133-164.
4. Marshall JESUS kristus, Maier BOBIL, Jimenez M, Dellinger EP. Sourcecontrol i behandling av alvorlig sepsis og septisk sjokk: anevidence-basert vurdering. Crit Care Med., 2004;32(suppl):S513-S526.
5. Friswell A. Surviving Sepsis Campaign forhåndsvisninger oppdaterte retningslinjer for 2012. Pulmonal Rev. 2012;17:1,5. www.pulmonaryreviews.com/Article.aspx?ArticleId=sC3JHu+0hSA=. Tilgang Til September 7, 2012.
6. Klevens RM, Morrison MA, Nadle J, et al. Invasive meticillin-resistente Staphylococcus aureus infeksjoner i Usa. JAMA. 2007;208:1763-1771.
7. Rybak MJ, Lomaestro BM, Rotschafer JESUS kristus, et al.,Vancomycin terapeutiske retningslinjer: et sammendrag av consensusrecommendations fra Smittsomme Sykdommer Society of America, theAmerican Samfunn av Helse-System Farmasøyter, og Samfunnet ofInfectious Sykdommer Farmasøyter. Clin Infisere Dis. 2009;49:325-327.
– 8. Scheetz MH, Vondt KM, Noskin GA, Oliphant CM. Søker antimikrobielle pharmacodynamics å motstandsdyktig mot gram-negative bakterier. Am J Helse-Syst Pharm. 2006;63:1346-1360.
9. Murphy JE, Schauer DE, Bateman CV. Forutsigbarhet ofvancomycin gjennom konsentrasjoner ved hjelp av syv tilnærminger for estimatingpharmacokinetic parametere., Am J Helse-Syst Pharm. 2006;63:2365-2370.
10. Owens RC Jr, Shorr AF. Rasjonell dosering av antimikrobielle midler: farmakokinetiske og farmakodynamiske strategier. Am J Helse-Syst Pharm. 2009;66(4 suppl):S23-S30.
11. Piraino B, Bailie GR, Bernardini J, et al. Peritoneal dialyse-relatert infeksjon anbefalinger: oppdatering i 2005. Perit Ringe Int. 2005;25:107-131.
12. Alaniz C, Regal RE. Spontan bakteriell peritonitt: en gjennomgang av behandlingstilbud. S T. 2009;34:204-210.
13. Sorter P, Navasa M, Arroyo V, et al., Effekten ofintravenous albumin på nedsatt nyrefunksjon og dødelighet hos pasienter withcirrhosis og spontan bakteriell peritonitt. N Engl J Med. 1999;341:403-409.
14. Sigal SH, Stanca CM, Fernandez J, et al. Begrenset bruk av albumin for spontan bakteriell peritonitt. Gut. 2007;56:597-599.
15. EASL klinisk praksis, retningslinjer for forvaltningen ofascites, spontan bakteriell peritonitt, og hepatorenal syndrom incirrhosis. J Hepatol. 2010;53:397-417.
16. Fernandez J, Ruiz del Arbol L, Gomez C, et al.,Norfloxacin vs ceftriaxone in the prophylaxis of infections in patientswith advanced cirrhosis and hemorrhage. Gastroenterology. 2006;131:1049-1056.