us Pharm. 2012; 37 (12):HS1-HS8.
samenvatting: als medicijndeskundigen worden apothekers verzocht passende richtlijnen te geven voor de behandeling van acutebacteriële peritonitis in het ziekenhuis. Acute bacterialperitonitis wordt geassocieerd met een hoog risico op mortaliteit. Onmiddellijk ingrijpen is noodzakelijk, omdat de vertraging kan toestaan dat het eenmaal gelokaliseerde ziekteproces andere organen door het hele lichaam beschadigt. Passende identificatie en behandeling van acute bacteriële peritonitis zijn sleutels tot betere resultaten., Naast chirurgische interventie is ook farmacologische behandeling noodzakelijk. Behandeling of preventie van hypovolemie geassocieerd met peritonitis kan worden uitgevoerd volgens de aanbevelingen van de overlevende sepsis Campagnerichtlijnen. Tot slot is het, aangezien antibioticatherapy de derde hoeksteen van de behandeling is, belangrijk om de juiste selectie, dosering en duur van antibiotica te overwegen.
Peritonitis is een acute ontsteking van de peritoneallining als gevolg van bacteriële infectie en andere oorzaken zoals chemicaliën, bestraling en vreemd lichaam letsel.,1 belediging van de peritoneale voering door een van deze middelen kan leiden tot een ontstekingsreactie, bekend als acute peritonitis.1 Tabel 1 toont gemeenschappelijke pathogene etiologie van acute bacteriële peritonitis.
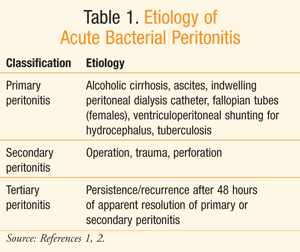
mortaliteit geassocieerd met peritonitis was rond 90% in de vroege jaren 1900. deze percentages zijn sindsdien gedaald tot ongeveer 30% met het gebruik van geschikte medicamenteuze therapieën en ondersteunende zorg.2
overzicht van de ziekte
classificatie van bacteriële peritonitis is gebaseerd op de bron van de infectieuze bacteriën.,2 primaire of spontane buikvliesontsteking verwijst naar een extraperitoneale etiologie, waarbij de infectieuze bacterie de buikvliesholte binnendringt via de bloedsomloop of het lymfatische systeem.1,2 in deze gevallen, heeft de patiënt gewoonlijk een onderliggende comorbiditeit die tot bacteriële migratie in het buikvlies kan leiden.1s dergelijke comorbiditeiten kunnen ascites en inwonende peritonealedialyse katheters omvatten. Primaire peritonitis komt naar schatting voor bij 10% tot 30% van de patiënten met alcoholische cirrose.,1 bovendien hebben patiënten die chronische ambulante peritoneale dialyse (CAPD) ondergaan, gemiddeld één incidentie van peritonitis elke 33 maanden.1
secundaire peritonitis, de meest voorkomende etiologie, is het resultaat van infectieuze bacteriën uit een bron in het peritoneum.1consideringde overvloed van microflora die binnen de abdominalorgans, migratie van de bacteriën van om het even welk van de organen in het sterile peritoneum kan leiden tot een ontstekingsreactie, resulterend insectary peritonitis. Verspreiding van bacteriën uit hun gastheerorganen kan het gevolg zijn van punctie als gevolg van trauma, chirurgie, of perforatie.,1 ulceratie, ischemie, of obstructie kan de perforatie van de buikorganen veroorzaken.1 tot slot, tertiaire peritonitis persisterende of terugkerende peritonitis die ten minste 48 uur na schijnbare resolutie van een primaire of secundaire peritonitis verschijnt.2 gegevens over de incidentie van secundaire en tertiaire peritonitis zijn beperkt.1 Classificatie van peritonitis is nuttig in de klinische praktijk omdat het een geschikte diagnose en behandeling kan helpen vergemakkelijken.,
klinische presentatie en diagnose
bacteriële introductie in het peritoneum resulteert in een onmiddellijke humorale en cellulaire immuunrespons.1Deze reactie leidt tot een ontstekingsproces, wat resulteert in fluidshifts in de peritoneale holte. Deze vochtophoping, samen met verminderde intestinale motiliteit, leidt vaak tot opgezette buik.Bovendien, vochtafvoer in de buik, bekend als derde-spacing,kan resulteren in een verminderd bloedvolume, wat leidt tot hypovolemie in severecases., Koorts, braken, en diarree kunnen ook gepaard peritonitis,compounding vloeistof onevenwichtigheden en het verhogen van het risico op hypovolemie.Onbehandelde hypovolemie kan resulteren in een verminderde cardiale output, en, uiteindelijk, hypovolemische shock.1
naast vloeistofverschuivingen kunnen vreemde stoffen zoals feces en slijm aanwezig in de buikholte peritonitis verergeren door het verzwakken van immuunmechanismen zoals bacteriële fagocytose.1bacteriële en endotoxine absorptie in de bloedbaan wordt vergemakkelijkt door een ontstoken peritoneum en kan leiden tot sepsis., Overlijden kan het gevolg zijn van negatieve effecten op orgaansystemen door ernstige complicaties zoals sepsis. Bovendien, kunnen andere ernstige complicaties, zoals asypoalbuminemie veroorzaakt door eiwitverlies evenals pulmonarycomplicaties zoals longontsteking als gevolg van diafragmatische remming dueto spalken, de prognose verergeren. Samen met gastheer immuniteit en behandeling adequaatheid, de hoeveelheid en virulentie van infecterende organismen en de aanwezigheid van vreemde stoffen in de buikholte hebben een grote impact op het resulterende resultaat van peritonitis.,1
De niet-specifieke klinische presentatie van primaryperitonitis varieert drastisch van de opvallende presentatie van secondaire peritonitis.1 in tegenstelling tot secundaire peritonitis kan primaryperitonitis zich gedurende enkele weken ontwikkelen zonder tekenen van acutedistress. Hoewel de patiënt kan klagen over abdominale tederheid, misselijkheid, braken, of diarree, primaire peritonitis is meestal eerst vermoed wanneer het dialysaat troebel lijkt in patiënten ondergaperitoneale dialyse of wanneer encefalopathie verergert bij patiënten metcirrhose., De laboratoriumbevindingen na verdenking van primaryperitonitis kunnen lichte verhoging van het aantal witte bloedcellen (WBC) en een positieve cultuur van het peritoneale dialysaat of ascetische vloeistof tonen.1
daarentegen vertonen patiënten met secundaire peritonitis vaak een boardachtige buik, een opgezette buik, zwakke darmgeluiden die na verloop van tijd afnemen, en ondraaglijke buikpijn die leidt tot onwillekeurige bewaking, met minuscule bewegingen zoals ademen of schommelen van het bed die ernstige pijn veroorzaken., Zoals eerder vermeld,kan hypovolemie optreden zonder behandeling, wat uiteindelijk kan resulteren in hypotensie en shock. Andere tekenen en symptomen zijn onder meer keelneu, tachycardie, misselijkheid en braken, verminderde urineproductie en geëvacueerde temperatuur.1 in secundaire peritonitis kunnen laboratoriumtests leukocytose aantonen, met overheersende neutrofielen en verhoogde banden.1
behandeling van Peritonitis
de gewenste resultaten bij peritonitis omvatten het verdwijnen van de onderliggende etiologie en drainage van abcessen.,1secondaire doelstellingen van behandeling omvatten verwijdering van besmetting en bescherming tegen ongunstige druggebeurtenissen evenals eind-orgaanschade, met inbegrip van die aan de longen, lever, hart, en nieren.1elementen van geschikte interventie bestaan uit vochtreanimatie, broncontroleprocedure (chirurgie) en empirische antimicrobiële therapie.3de meeste gevallen van primaire peritonitis vereisen het gebruik van antimicrobiële middelen als de steunpilaar van de therapie, en drainage procedures zijn meestal niet vereist.1
secundaire peritonitis vereist chirurgische behandeling, bekend als Broncontrole, om de onderliggende pathologie te corrigeren.,1 Sourcecontrol is bedoeld om anatomische ontsporingen te corrigeren, infectiousfoci te verwijderen en de factoren te controleren die aanhoudende infectie bevorderen.4specifieke factoren die een succesvolle Broncontrole waarschijnlijk uitsluiten, omvatten een vertraging van meer dan 24 uur tot de procedure; een ACUTEPHYSIOLOGY and Chronic Health Evaluation (APACHE) score van ten minste 15;leeftijd >70 jaar; aanwezigheid van comorbiditeit; laag albuminegehalte; poornvoedingsstatus; diffuse peritonitis; en aanwezigheid van maligniteit.,3 mislukte Broncontrole wordt aangegeven door terugkerende infectie op de plaats, anastomotic mislukking, of fistelvorming.3 percutane, beeld geleide drainage heeft de voorkeur boven chirurgische drainage, vooral wanneer de infectie is goed gelokaliseerd.1,3
hypovolemie in de setting van peritonitis kan leiden tot orgaanfalen. Daarom is,ongeacht de aanwezigheid van septische shock, snelle vochtreanimatie gerechtvaardigd bij alle patiënten met buikvliesontsteking om fysiologische stabiliteit te bevorderen.,3 meer agressieverestoratie van intravasculair volume dient te worden verstrekt aan mensen meteptische shock en orgaanfalen op de wijze die is beschreven in de Overlevingsepsis Campagnerichtsnoeren voor de behandeling van septische shock.3 The2012 updates aan de overlevende sepsis richtlijnen zullen naar verluidt statethat de aanvankelijke vloeistof uitdaging ten minste 1 L kristalloid,en een minimum van 30 mL/kg in de eerste 4 tot 6 uren zou moeten zijn. Incrementele fluidbolussen kunnen volgen zolang de vitale functies van de patiënt blijven verbeteren.,5 Norepinephrine is de aangewezen vasopressor, en dobutamine inotrope therapie kan aan patiënten metcardiac dysfunctie worden toegevoegd.5 continue hydrocortisoninfusie tot 200 mg / 24 uur wordt aanbevolen voor mensen met een vasopressor-refractaire septische schok. Koorts, tachypneu, misselijkheid envomiting, en verminderde vochtinname kan leiden tot uitdroging bij patiënten met peritonitis.
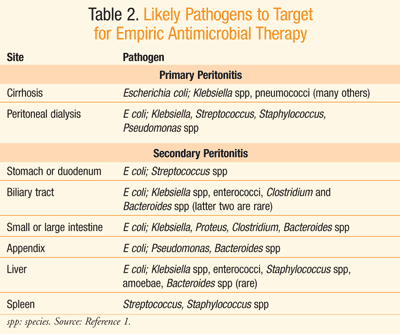
empirische antibioticumtherapie dient te worden gestart op verdenking van peritonitis.,3praktijkrichtlijnen van de Infectious Diseases Society of America(IDSA) bevelen aan dat empirische antimicrobiële therapie wordt geïnitieerd binnen het eerste uur van de herkenning van peritonitis bij patiënten metgecompromitteerde hemodynamische of orgaanfunctie; anders dient de therapie binnen 8 uur na de presentatie te worden geïnitieerd.3 hoewel er bij de behandeling van door de gemeenschap verworven peritonitis een beperkte waarde aan bloedculturen is, zijn Gramkleuringen om de aanwezigheid van gram-positieve cocciorgist op te sporen gerechtvaardigd bij personen met een hoog risico en bij personen met door de gezondheidszorg verworven peritonitis.,3 antibiotische therapie kan bealtered op resultaten van cultuur en gevoeligheidsgegevens. In eerste instantie zou IV empirische antibioticakeuze zich echter moeten richten op waarschijnlijke organismenspresentatie op de plaats waar peritonitis werd afgeleid,zoals weergegeven in tabel 2.1
Er zijn verschillen tussen zorggerelateerde en gemeenschapsgerelateerde infecties (tabel 3).,3,6 aminoglycosiden behoren tot de middelen die worden aanbevolen voor gebruik in empiricalantimicrobial therapie voor gezondheidszorg–geassocieerde complicatedintra-abdominale infecties, in het bijzonder die veroorzaakt door Enterobacteriaceae organismen die extended-spectrumbeta-lactamases (ESBL ‘ s) produceren.3 Vancomycine wordt aanbevolen in dezelfde situatie wanneer methicilline-resistente Staphylococcus aureus (MRSA) het veroorzakende organisme is van de gezondheidszorggerelateerde infectie.3 Deoorsprong van de infectie in termen van anatomische plaats en assetting (d.w.z.,, ziekenhuis of gemeenschap) helpt bij de selectie van de meest redelijke empirische antibioticatherapie.

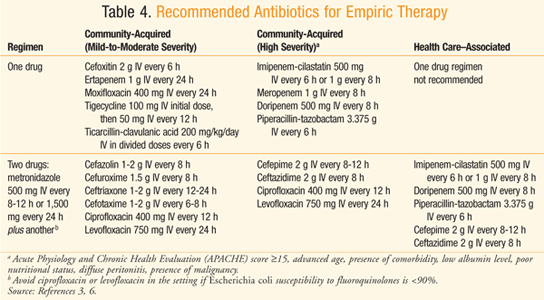
tabel 4 toont de aanbevolen empirische antibioticaregimes voor patiënten met peritonitis met een normale nier-en leverfunctie 3,6 of een creatinineklaring tussen 70 en 100 mg / dL.Gezien de toenemende resistentie van Escherichia coli tegen chinolonen, dienen dergelijke geneesmiddelen alleen te worden gebruikt in een ziekenhuis waarvan onderzoek aangeeft dat >90% gevoeligheid van E coli voor chinolonen.,3 Er bestaat ook bezorgdheid over het frequente gebruik van ertapenem dat leidt tot het ontstaan van carbapenem-resistente Enterobacteriaceae-organismen en Pseudomonas-en Acinetobacter-soorten.Ampicilline-sulbactam dient te worden vermeden bij het richten op E coli, rekening houdend met de prevalentie van resistentie tegen het geneesmiddel.,3,8 wanneer een zorggerelateerde infectie zorgwekkend is, is er een hoger risico op infectie als gevolg van Candida–en Enterokokkenspecies, is fluconazol gerechtvaardigd bij patiënten met een maligniteit,transplantatie, ontstekingsziekte, recidiverende intra-abdominale infectie,maagzweer bij zuuronderdrukking of die immunosuppressieve therapie volgen voor neoplasma.3 ampicilline of vancomycine kunnen worden toegevoegd aan de empirische therapie om enterococcen te richten bij mensen met een infectie die verband houdt met de gezondheidszorg, vooral wanneer het een postoperatieve infectie is.,3 patiënten waarvan bekend is dat ze gekoloniseerd zijn met MRSA en patiënten met gezondheidszorggerelateerde peritonitis moeten worden behandeld met een antimicrobieel middel dat MRSA omvat, zoals vancomycine.3
Er zijn specifieke overwegingen met betrekking tot antimicrobiële dosering voor patiënten die ernstig ziek en/of zwaarlijvig zijn.Als gevolg van fysiologische veranderingen bij deze patiënten kunnen bepaalde farmacokinetische factoren veranderen, zoals het schijnbare distributievolume en/of klaring.,3 indien de dosering afhankelijk is van de nierfunctie, kan het bovendien nodig zijn de creatinineklaring direct te meten vanwege de moeilijkheid van de schatting die toe te schrijven is aan bovengemiddeld lichaamsgewicht.Ernstig zieke patiënten kunnen ook veranderingen in bepaalde farmacokinetische parameters ervaren. Bijvoorbeeld, patiënten in de vroege stadia van sepsis kunnen ervaren aypermetabole toestand en vloeistof verschuivingen die kunnen leiden tot een verhoogd volume vandistributie en klaring.3 dergelijke verschuivingen kunnen resulteren in lagere serumconcentraties van antimicrobiële stoffen zoals bètalactams.,3 bij obese patiënten zijn eveneens verlaagde serumconcentraties van antimicrobiële stoffen zoals cefalosporinen en carbapenems waargenomen.3 als gevolg van dergelijke farmacokinetische veranderingen kunnen aanpassingen zoals hogere doses en/of frequentere toediening nodig zijn in deze subgroepen van patiënten.3 in gevallen waarin vancomycine een geschikt middel is voor ernstig zieke en / of zwaarlijvige patiënten, dient het totale lichaamsgewicht te worden gebruikt bij de berekening van de aanvangsdosering.Bovendien dienen deze patiënten de serumconcentratie vancomycine te laten controleren om geïndividualiseerde dosering te verkrijgen.,3,10
intraperitoneale dosering heeft de voorkeur boven I.V. dosering voor patiënten die peritoneale dialyse ondergaan om hogere lokale antibiotica te bieden. Empirische therapie moet zowel gram-positieve als Ram-negatieve organismen omvatten waarvan bekend is dat ze peritonitis veroorzaken. Intraperitonealantibiotica kunnen worden gegeven door middel van continue dosering of intermitterende dosering. Doseringsschema ‘ s dienen rekening te houden met residuele renalfunction, gedefinieerd als >100 mL/dag urineproductie, waarbij casereaanbevolen doses empirisch moeten worden verhoogd met 25%.,11Dwell-time exchange dient ten minste 6 uur te zijn bij gebruik van intermitterende toediening. De aanbevolen behandelingsduur bedraagt 2 weken of 3 weken voor meer ernstige gevallen. De behandeling is afhankelijk van de klinische respons, die binnen 72 uur na aanvang van de antibioticatherapie moet worden waargenomen.Van patiënten met troebel effluent na 4 tot 5 dagen gepaste antibiotische therapie wordt aangenomen dat zij refractaire peritonitis hebben en hun katheter moeten worden verwijderd.
acuut nierfalen is de belangrijkste voorspeller van overlijden bij patiënten met spontane bacteriële peritonitis (SBP).,Albumine is gebruikt bij SBP om plasmavolume-expansie te veroorzaken om de incidentie van nierfalen bij patiënten met cirrose te verminderen die paracentese met een groot volume ondergaan.Een studie waarin het gebruik van IV albumine naast antimicrobiële therapie versusantimicrobiële therapie alleen werd geëvalueerd bij patiënten met cirrose en SBP resulteerde in een verminderde incidentie van nierfalen en een verminderde mortaliteit.,Er werd vastgesteld dat patiënten die werden behandeld hoogstwaarschijnlijk baat hadden bij albumine als ze serumbilirubinewaarden >4 mg/dL, serumcreatinine >1 mg/dL, en een concentratie van ureumstikstof (BUN)>30 mg/dL hadden.Een tweede studie bevestigde de eerder gerapporteerde Bevindingen en gebruikte dezelfde dosering van 1,5 g/kg toegediend op de eerste dag en 1 g/kg toegediend op de derde dag.,Er zijn momenteel onvoldoende gegevens om het gebruik van albumine-patiënten met gecompliceerde SBP, of met een serumbilirubine <4 mg/dL en een creatinine van <1 mg/dL te ondersteunen. De Europese Vereniging voor de studie van de lever stelt dat aanvullende studies nodig zijn om de doeltreffendheid van albumine en andere volumeuitbreidders in het beheer van SBP te beoordelen.
antimicrobiële therapie moet worden beperkt tot 4 tot 7 dagen.3 als de tekenen en symptomen van peritonitis op dit moment zijn verdwenen, worden antibiotica niet langer aanbevolen.,3Als de patiënt op dit moment herstelt, een oraal dieet kan verdragen en geen resistentie vertoont,is een afbouwtherapie met oralantibiotica gerechtvaardigd.3 antibiotica aanbevolen in deze setting omvatten moxifloxacine, een combinatie van metronidazol met eitherlevofloxacine of een oraal cefalosporine, of amoxicilline-clavulanaat.Deze orale middelen kunnen ook worden gebruikt voor degenen die worden behandeld in de outpatient setting, maar werden geïnitieerd op intramurale IV therapie.,
falen van de behandeling na 4 tot 7 dagen behandeling dient onderzocht te worden met behulp van geschikte beeldvormingstechnieken zoals CT-scan of ultrasound.Antimicrobiële therapie die effectief is tegen initiale organismen moet worden voortgezet en extra-abdominale infectiebronnen moeten worden uitgesloten bij patiënten die niet reageren op de therapie.Aërobe en anaërobe culturen worden aanbevolen voor patiënten metinfectie die na de initiële behandeling blijft.
bepaalde patiëntenpopulaties moeten worden overwogen voorprofylaxe van bacteriële peritonitis., Primaire bacteriële peritonitis kan worden voorkomen met behulp van antibiotica als er een bekende risicofactor. Zo kan bijvoorbeeld een enkelvoudige IV-dosis van vancomycine 1 g, gegeven op het moment van deatheterplaatsing bij patiënten die peritoneale dialyse ondergaan, bacteriële peritonitis voorkomen.Een alternatief voor vancomycine is een enkelvoudige dosis cefazoline 1 G IV. 11e secundaire bacteriële peritonitis profylaxe moet worden overwogen bij patiënten met cirrose die worden opgenomen voor een bloeding in het bovenste deel van het maag-darmkanaal.,12in het verleden was 400 mg norfloxacine per dag het middel bij uitstek in de setting van een bloeding in het bovenste deel van het maag-darmkanaal; sindsdien is echter alternatieve antimicrobiële middelen overwogen vanwege epidemiologische veranderingen van bacteriële infecties bij cirrose.Ceftriaxon 1 G IV is een effectief alternatief gebleken.
conclusie
Peritonitis, een acute ontsteking van het peritoneum, kan optreden als gevolg van pathogenen of andere oorzaken, zoals chemische blootstelling.Klinische presentatie van primaire peritonitis is vaak niet-specifiek en kan gebrek aan initiële tekenen en symptomen., Omgekeerd, secundaire peritonitisvaak presenteert met prominente symptomen, waaronder ernstige pijn. Onbehandelde peritonitis kan leiden tot sepsis en eind-orgaan schade; daarom, onmiddellijke behandeling van bacteriële peritonitis moet worden geleid door specifieke etiologie en comorbiditeiten.
vaak gebruikte antimicrobiële middelen voor in de gemeenschap verworvenperitonitis zijn cefalosporinen en fluorochinolonen. In de gezondheidszorg verworven peritonitis kan behandeling met breedspectrumantimicrobials zoals carbapenems vereisen., Bij doseringsbeslissingen moet rekening worden gehouden met de kenmerken van de patiënt, en bepaalde subgroepen van de patiënt, zoals ernstig ziek en/of zwaarlijvig, kunnen een aanpassing van de dosering nodig maken vanwege variaties in farmacokinetische parameters. In gevallen van non-respons op empirische therapie, moeten bronnen van infectie buiten de buik worden overwogen. In alle gevallen van peritonitis dient ondersteunende zorg te worden toegediend zoals aangegeven om complicaties te minimaliseren.
1. Dipiro JT, Howdieshell TR. Intraabdominale Infecties. In: Dipiro JT, Talbert RL, Yee GC, et al, eds. Farmacotherapie: Een Pathofysiologische Benadering. 8e ed., New York, NY: McGraw-Hill; 2011.
2. Ordonez CA, Carlos J. Management van peritonitis in de kritisch zieke patiënt. Surg Clin North Am. 2006;86:1323-1349.
3. Solomkin JS, Mazuski JE, Bradley JS, et al. Diagnostiek en beheer van gecompliceerde intra-abdominale infectie bij volwassenen enkinderen: richtlijnen van de Surgical Infection Society en de Infectious Diseases Society of America. Clin Infecteert Dis. 2010;50:133-164.
4. Marshall JC, Maier RV, Jimenez M, Dellinger EP. Broncontrole in het beheer van strenge sepsis en septic shock: anevidence-gebaseerd overzicht. Crit Care Med., 2004; 32 (suppl): S513-S526.
5. Friswell A. Surviving Sepsis Campaign previews updated guidelines for 2012. Pulmonale Rev. 2012; 17: 1,5. www.pulmonaryreviews.com/Article.aspx?ArticleId=sC3JHu + 0hSA=. Geraadpleegd op 7 September 2012.
6. Klevens RM, Morrison MA, Nadle J, et al. Invasieve methicilline-resistente Staphylococcus aureus infecties in de Verenigde Staten. JAMA. 2007;208:1763-1771.
7. Rybak MJ, Lomaestro BM, Rotschafer JC, et al.,Vancomycine therapeutische richtlijnen: een samenvatting van consensusaanbevelingen van de Infectious Diseases Society of America, theAmerican Society of Health-System Pharmacists, en de Society of Infectious Diseases Pharmacists. Clin Infecteert Dis. 2009;49:325-327.
8. Scheetz MH, Hurt KM, Noskin GA, Oliphant CM. Antimicrobiële farmacodynamiek toepassen op resistente gramnegatieve pathogenen. Am J Health Syst Pharm. 2006;63:1346-1360.
9. Murphy JE, Gillespie de, Bateman CV. Voorspelbaarheid vanvancomycine dalconcentraties met zeven benaderingen voor het schatten van farmacokinetische parameters., Am J Health Syst Pharm. 2006;63:2365-2370.
10. Owens RC Jr, Shorr AF. Rationele dosering van antimicrobiële middelen: farmacokinetische en farmacodynamische strategieën. Am J Health Syst Pharm. 2009; 66(suppl 4):S23-S30.
11. Piraino B, Bailie GR, Bernardini J, et al. Peritoneale dialyse-gerelateerde infectie aanbevelingen: 2005 update. Perit Dial Int. 2005;25:107-131.
12. Alaniz C, Regal RE. Spontane bacteriële peritonitis: een overzicht van de behandelingsopties. P T. 2009; 34: 204-210.
13. Sort P, Navasa M, Arroyo V, et al., Effect van intraveneuze albumine op nierinsufficiëntie en mortaliteit bij patiënten metcirrhose en spontane bacteriële peritonitis. N Engl J Med. 1999;341:403-409.
14. Sigal sh, Stanca CM, Fernandez J, et al. Beperkt gebruik van albumine voor spontane bacteriële peritonitis. Darm. 2007;56:597-599.
15. EASL klinische praktijk richtlijnen voor de behandeling van ascites, spontane bacteriële peritonitis, en hepatorenal syndroom incirrhosis. J Hepatol. 2010;53:397-417.
16. Fernandez J, Ruiz del Arbol L, Gomez C, et al.,Norfloxacin vs ceftriaxone in the prophylaxis of infections in patientswith advanced cirrhosis and hemorrhage. Gastroenterology. 2006;131:1049-1056.