In the previous post we introduced orto -, para – and meta – directors in electrophilic aromatic substitution. Antes disso, cobrimos o mecanismo de substituição eletrofílica aromática, e mostramos que o mecanismo procede através de um intermediário de carbocação.,
hoje, nós vamos amarrar esses dois conceitos juntos, e tentar mostrar que se um substituinte é um orto -, para – ou meta – diretor depende de como o substituinte afeta a estabilidade do intermediário de carbocação.
e também veremos por que um nome alternativo para meta – diretor pode ser, “orto-, para – avoider”. :–)
tabela de conteúdos
- As Carbocações são estabilizadas por átomos adjacentes com pares solitários
- estudo de Caso #1: um orto-,para – Director (OCH3)
- Sim, o oxigénio é Electronegativo., Mas A Doação Do Seu Par Solitário Compensa Mais Do Que Isso!estudo de caso # 2: um meta-director (CF3).o que chamamos de “meta– Directores” são mais como “Orto-, para– Avoiders”
- O diagrama de energia de reacção para um meta – Director
- Então porque são os halogéneos para-Directores?perguntas a ti próprio!, (Advanced) References and Further Reading
Carbocations Are Stabilized By Adjacent Atoms With Lone Pairs
Let’s think back to which factors increase the stability of carbocations. Carbocações são espécies pobres de elétrons com seis elétrons em sua camada de Valência. Então, qualquer substituinte que possa doar densidade de elétrons para o carbocation estará estabilizando. Isto inclui:
- substituintes Libertadores de electrões que podem actuar como “dadores de sigma” (e.g., muitos grupos alquilo, que doam densidade de elétrons através de efeitos indutivos)
- átomos adjacentes com pares solitários que podem atuar como” doadores de pi”para a carbocação
- ligações C–C adjacentes que podem estabilizar a carbocação através da deslocalização de carga (“estabilização de ressonância”, em outras palavras).e factores que desestabilizam as carbocações?
- qualquer substituinte que remova a densidade de elétrons de um carbocation, tais como grupos fortes que retiram elétrons.
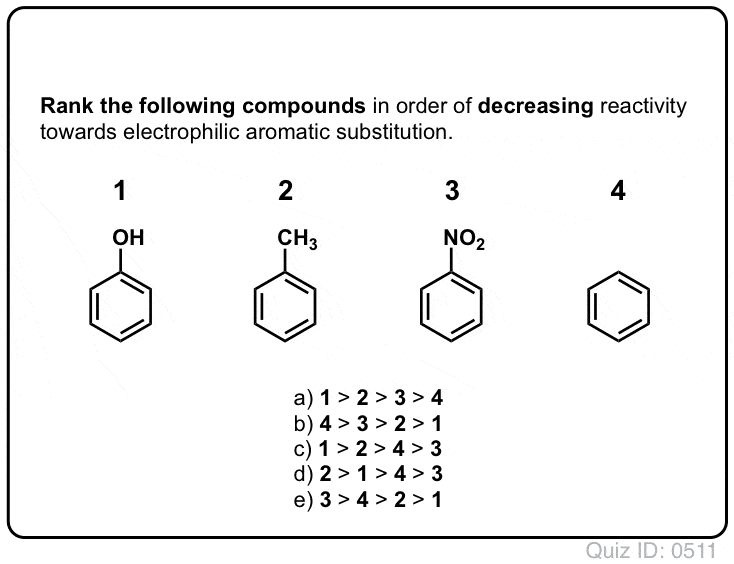
então aqui está um quiz rápido., Dado tudo o que está escrito acima, qual das duas carbocações abaixo será mais estável?
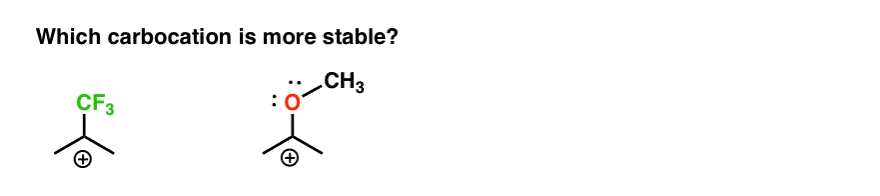
Se você pode responder bem a esta pergunta, você é a maior parte do caminho para entender a diferença entre orto-, para – e meta – diretores.vamos examinar dois casos. Vamos olhar para uma reação de substituição eletrofílica aromática genérica do benzeno com um orto-, para – diretor (metoxibenzeno) e examinar os intermediários que são obtidos a partir de ataque nas posições Orto, meta e para., Então faremos o mesmo exercício com um meta-diretor (trifluorometilbenzeno).
no processo, esperamos entender por que o metoxibenzeno favorece ortopédicos e para– produtos, enquanto o trifluorometilbenzeno favorece o meta-produto.
estudo de Caso # 1: uma substituição electrofílica aromática do metoxibenzeno por orto-,para – Director (OCH3)
tende a dar ortoprodutos e para – produtos com muito pouco meta -., Aqui está o que acontece na nitração, por exemplo:
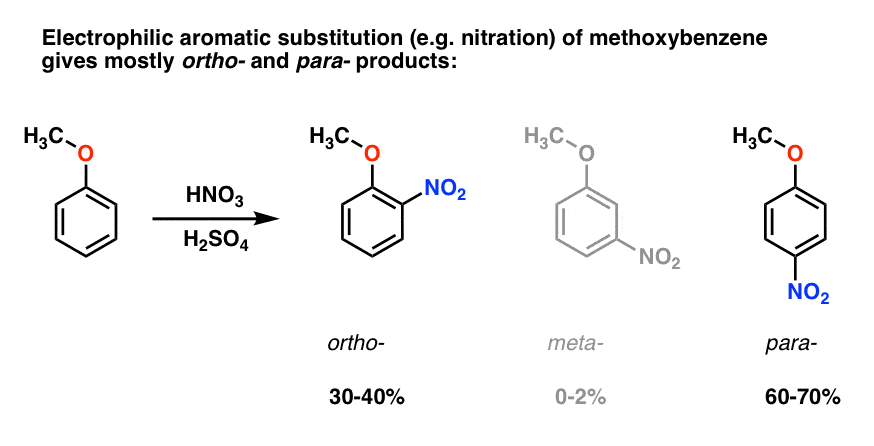
o para – produto domina (60-70%), com orto – perto atrás (30-40%) e apenas um traço do meta– .porquê?
3. Sim, O Oxigénio É Eletronegativo. Mas A Doação Do Seu Par Solitário Compensa Mais Do Que Isso!
Aqui está a via que conduz ao Orto-produto., Quebramos um C–C pi bond e formar um novo C–E bond (onde E é a intenção de representar um genérico electrophile), gerando uma ressonância estabilizada carbocation:
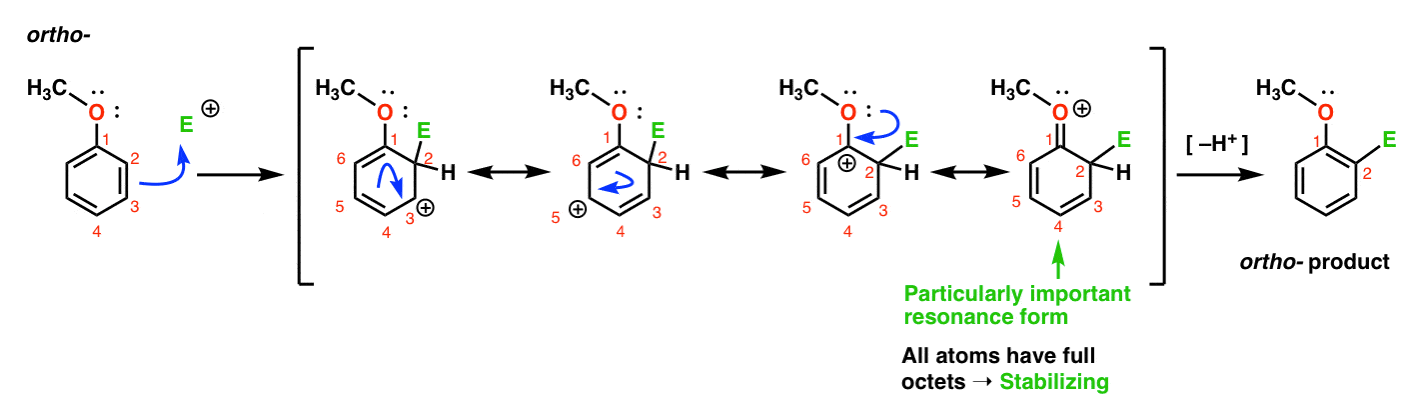
Se você olhar de perto, você deve observar que podemos formar quatro formas de ressonância . Três deles carregam carbocações completas (em C1, C3 e C5), mas é a quarta – a forma de ressonância onde há uma ligação C=o pi – que é particularmente importante. Por quê? Nesta forma de ressonância, todos os átomos de carbono têm um octeto completo de elétrons., Isso é porque o oxigênio diretamente ligado ao anel pode doar um par solitário para a carbocação adjacente, formando uma ligação pi. Este é um exemplo de doação de pi.
Aqui está o caminho para o ataque do eletrófilo na meta – posição. Repara na diferença!
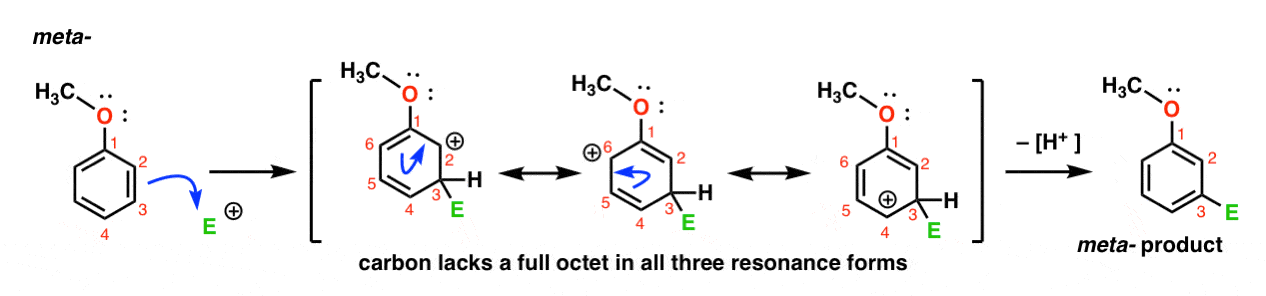
Attack of the electrophile at C-3 results in a carbocation which can be delocalized via resonance to C2, C4, and C6. No entanto, não há maneira de” mover ” o carbocação para C1, o que significa que não há nenhuma forma de ressonância razoável onde todos os átomos têm octetos completos.,
Isto torna o intermediário de meta-carbocação muito menos estável do que o intermediário de Orto – carbocação.
Finalmente, aqui está a reação do líder para o para – produto:
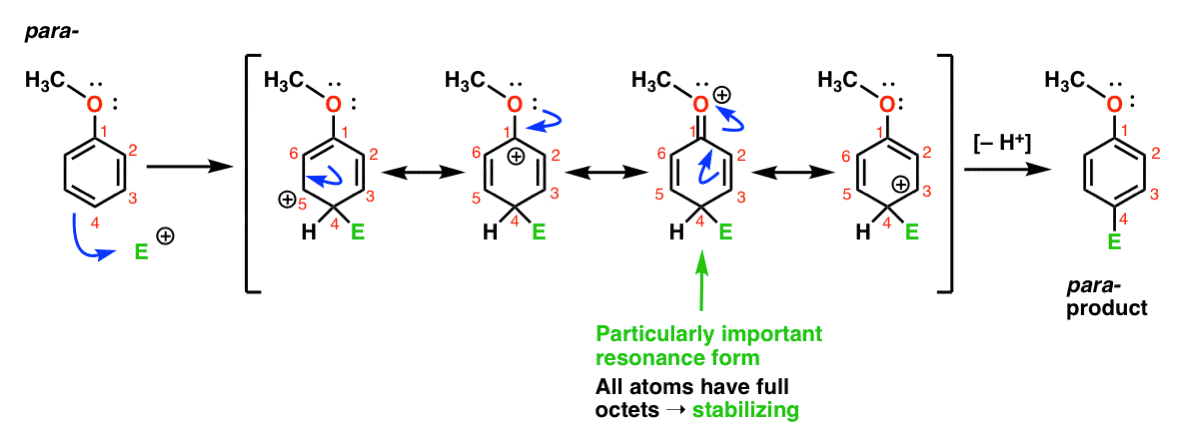
Aqui podemos voltar a desenhar formas de ressonância com carbocations em C1, C3 e C5, bem como um quarto de ressonância formulário onde o átomo de oxigênio ligado doa um par de elétrons para o carbocation em C1, resultando em um total de octetos em carbono. Esta é uma situação essencialmente a mesma que a Orto-intermediária.,
Assim, pela análise das formas de ressonância (e marcar a minha palavra, você pode ser solicitado a fazer o mesmo em um teste em um futuro próximo), podemos ver que o intermediário carbocations resultantes de orto – e para– além de são consideravelmente mais estável do que o intermediário de um meta– adição.
isto explica por que os ortho – e para – produtos dominam, e o meta – produto é menor. pode ser útil visualizar isto desenhando um diagrama de energia de reacção.4., O diagrama de reação-energia para um diretor Orto para
o estado de transição que leva aos produtos Orto – e para – adição é muito menor em energia do que o meta– .
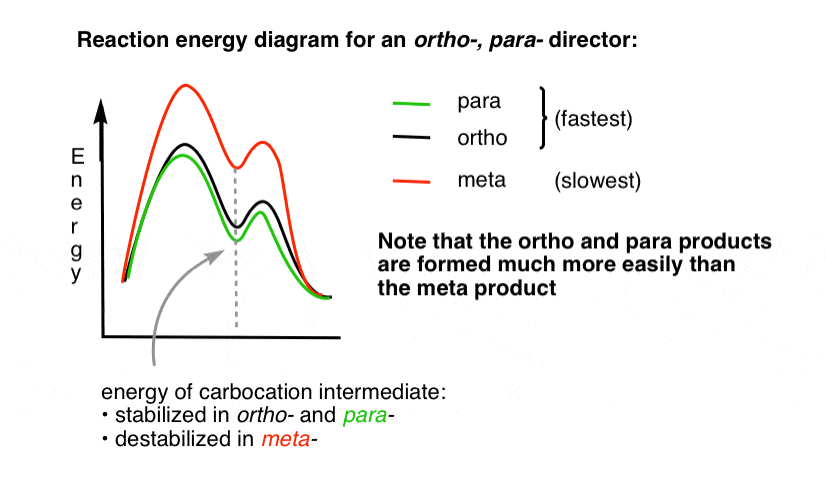
uma questão – por que você acha que para – pode ser favorecido (por exemplo, 60% -70% de rendimento para– produto de nitração, acima, versus 30-40% para Orto -), apesar de existirem duas posições Orto e apenas uma para -?pense nisso por um minuto, e vamos abordá-lo abaixo.
5. Estudo de caso n. o 2: meta-director (CF3).
então e o CF3?, Porque dá meta-produtos? Vamos fazer o mesmo tipo de análise.
Aqui está a via que conduz ao Orto-produto. Como com o Orto-intermediário acima, podemos desenhar três formas de ressonância colocando o carbocation em C1, C3 e C5, respectivamente.
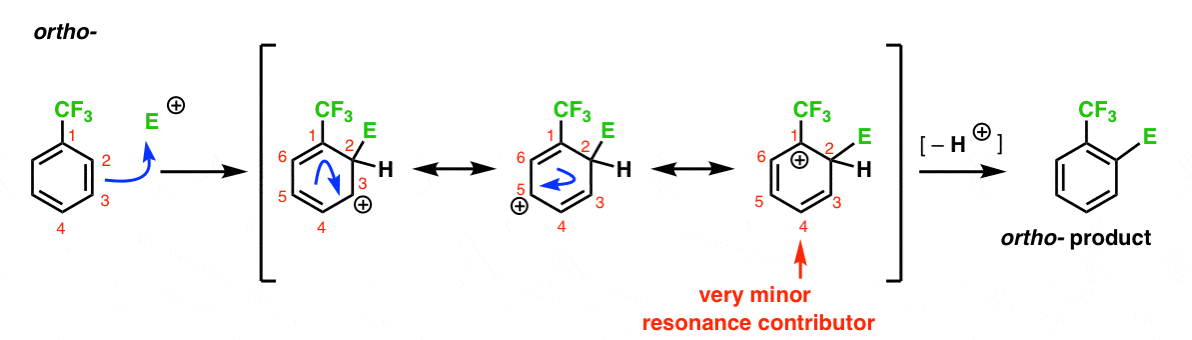
então o que é diferente neste caso?
O que é diferente é a presença de um forte grupo de retirada de elétrons (CF3) em C1, e isso muda completamente o jogo de bola.como dissemos, as carbocações são desestabilizadas por vizinhos que retiram a densidade de elétrons., Portanto, seria de esperar que este seja um contribuinte de ressonância muito menor, com o resultado de que a carga positiva é apenas deslocalizada sobre C3 e C5.notámos que o CF3 é um meta – director. É razoável pensar que há algo no meta que o torna particularmente estável. Analisando o intermediário para o meta– produto abaixo, consegue ver porquê?
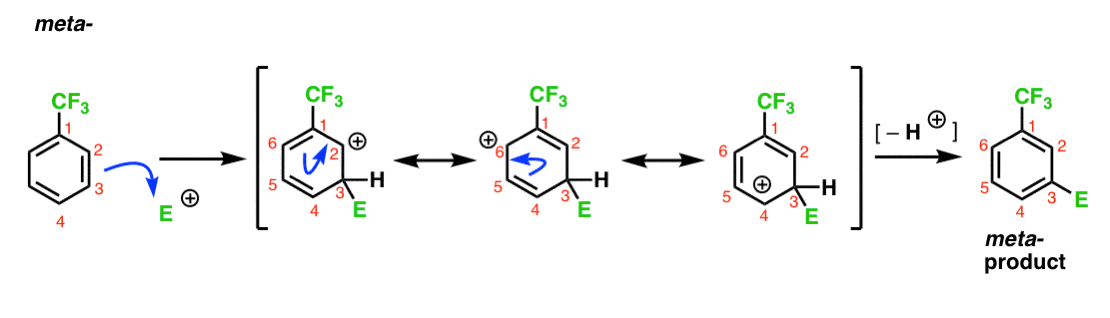
Hmmm. Não há intermediário onde um carbono tenha um octeto completo. Não existem formas de ressonância particularmente estáveis.é meio “meh”, não é?
6., O que chamamos de “meta– diretores” são mais como “Orto-, para– Avoiders”
por outro lado, também não existem quaisquer formas de ressonância particularmente instáveis. Uma vez que a carga positiva é localizada em C2, C4 e C6, uma situação em que a carga positiva é diretamente adjacente ao grupo CF3 de retirada de elétrons é evitada. E a carga positiva é, portanto, deslocalizada bem ao longo do anel, ao contrário da ortopedia, acima.
então é um intermediário” menos ruim ” do que o Orto-.,
finalmente, o para-intermediário tem o mesmo problema que o Orto- ; um intermediário com uma carga positiva em C1, adjacente ao CF3.
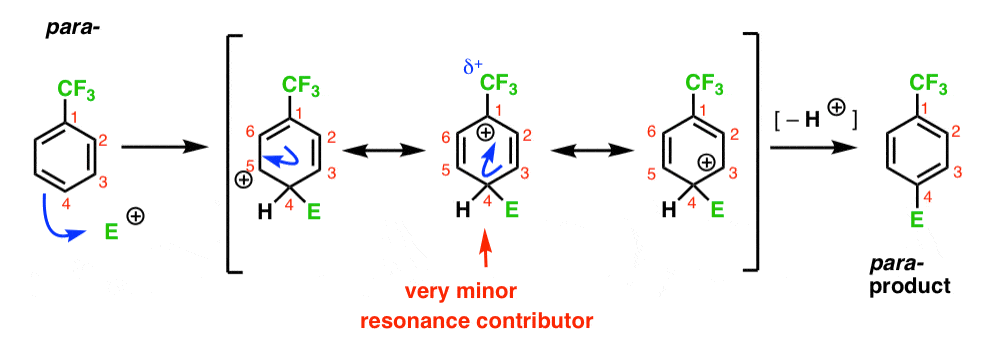
Isso resulta em apenas duas importantes formas de ressonância, o que leva a uma menor deslocalizados (e, portanto, menos estável) carbocation intermediário.
Bottom line: the meta carbocation intermediate is more stable than either the Orto– or the para – intermediates.
mas não é porque o substituinte em si tem qualquer efeito estabilizador sobre o meta– intermediário. .,eu diria que é mais útil pensar no meta como menos instável que o Orto – e para– .
desta forma, não é tanto que CF3 é um meta – diretor , tanto que é um “orto–, para– avoider. “
7. O diagrama de energia de reação para um meta-Diretor
Aqui está um esboço do diagrama de energia de reação:
tudo bem.de volta à nossa pergunta original. Qual carbocação é mais estável?,
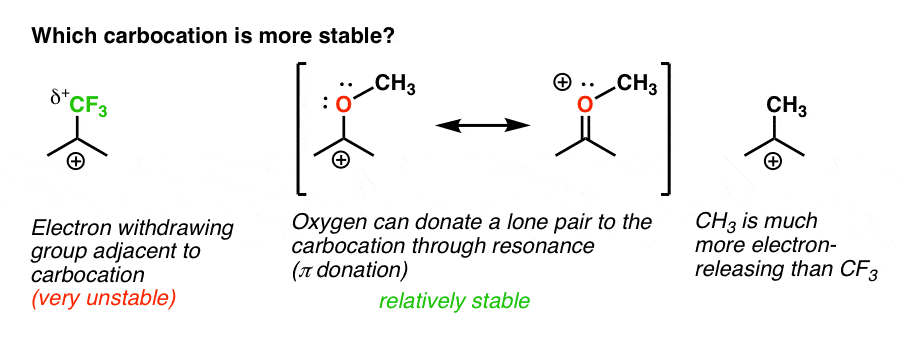
claramente, a carbocação com um oxigênio adjacente que suporta um par solitário é muito mais estável do que uma carbocação adjacente a um grupo de electrões como CF3.
E que compreende a diferença entre um orto-, para – director como OCH3 e um meta – director como CF3.
vale a pena notar que a maioria dos grupos alquilos (como CH3 ) não têm um par solitário, mas ainda são orto-, para – diretores., Isto é consistente com tudo o que aprendemos antes sobre como grupos alquilo são geralmente de estabilização para carbocations – lembre-se que carbocation estabilidade, geralmente, aumenta com a substituição de
Então, sobre os para– produtos…
Por que são para – produtos produzidos a uma taxa maior do que ortho- ?a resposta é um obstáculo estérico.
O ataque na posição para é menos onerado pelo substituinte do que o ataque nas posições Orto são.então, porque são os halogéneos Orto -, Para-Directores?
isto deixa-nos com o exemplo algo complicado de halogéneos.,por que razão o flúor, o cloro, o bromo e o orto-para – diretores de iodo, apesar de estarem a desactivar grupos?
A resposta não deve ser surpresa se você tem vindo a acompanhar, mas vamos deixar isso até o próximo post, porque este já é longo o suficiente.seguinte post: Por que os halogéneos ortho-, para – diretores?
notas
Nota 1. É mais correto dizer que os Orto – e para – produtos dominam porque os estados de transição que conduzem a esses produtos são mais baixos em energia do que as energias dos próprios intermediários., Afinal, é a energia dos estados de transição que determina a barreira de ativação e, portanto, a taxa de reação.Nota 2: Or hyperconjugation, which most textbooks (with the notable exception of Maitland Jones) generally avoid.pergunta a ti próprio!,/div>
 Clique para Virar
Clique para Virar 
 Clique para Virar
Clique para Virar 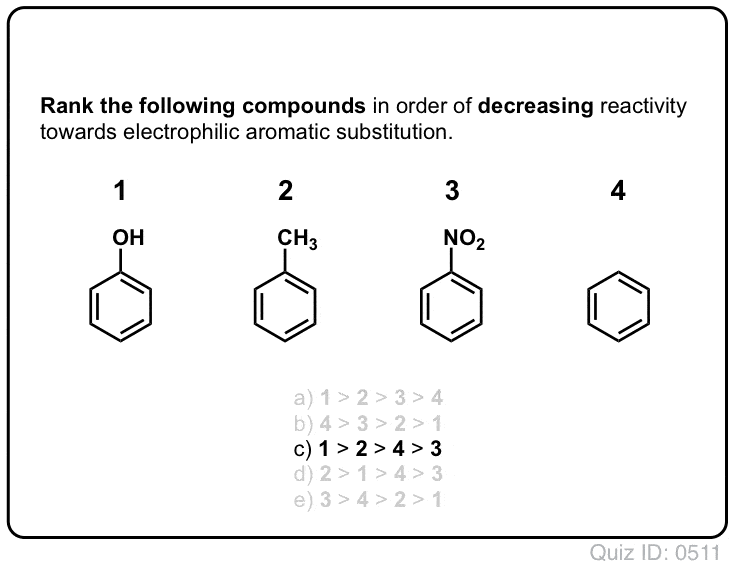
 Clique para Virar
Clique para Virar 
(Avançado) Referências e leituras Adicionais
- A., F. Holleman, Die direkte Einführung von Substituenten in den Benzolkern
Rec. Trav. Chim. Pays-Bas 1910, 12, 455-456
DOI: 10.1002/recl.19100291205
A. F Holleman from 1910 said that orto-para orientation is associated with activation and meta orientation with desactivation. - – a natureza do efeito alternado nas cadeias de carbono. Part XXIII. Anomalous orientation by halogens, and its being on the problem of the Orto–para ratio, in aromatic substitution
Christopher Kelk Ingold and Charles Cyril Norrey Vasss
J. Chem. Soc. 1928, 417-425
DOI: 10.,1039 / JR9280000417
This paper discusses directing effects in 1,2-dihalobenzenes. - Some observations concerning steric hindrance and the effects of substituents on the Orto : para ratio in aromatic substitution
P. B. D. De la Mare
J. Chem. Soc. 1949, 2871-2874
DOI: 10.1039/JR9490002871
este papel, o de la Mare discute vários fatores que podem contribuir para uma predominância do pará sobre ortho seletividade, depois de dividir o rendimento de ortho produto por 2 (uma vez que existem 2 ortho posições, mas apenas 1 par de posição em monosubstituted benzenos).,efeitos volumétricos dos grupos alquilo em compostos aromáticos. Part V. The monosulfonation of p-cymene
R. J. W. Le Fèvre
J. Chem. Soc. 1934, 1501-1502
DOI: 10.1039/JR9340001501
In p-cymene, the major product obtained upon electrophilic sulfonation is the 2-product (Orto to the methyl group), likely due to sterics. - efeitos de grupos alquilo em adições e substituições Eletrofilicas
COHN, H., HUGHES, E., JONES, M. and PEELING, M. G.
Nature 1952, 169, 291
DOI: 1038/169291a0
Este artigo tem dados comparando a nitração de T-butilbenzeno e tolueno., O T-butilbenzeno é muito mais diretivo p do que o tolueno (79,5% para o T-butilbenzeno vs. 40% para o tolueno), o que é provável devido aos estéricos (a aproximação Orto é bloqueada pelo grupo t-butil bulkier).distribuição dos isómeros na Mononitração do etil-e Isopropilbenzeno. Further Evidence for a Steric Effect in Isomer Distribution
Herbert C. Brown and W. Hallam Bonner
Journal of the American Chemical Society 1954, 76 (2), 605-606
DOI: 10.,1021 / ja01631a084
A Tabela II neste artigo ilustra que o produto Orto obtido a partir da nitração de monoalquilbenzenos diminui à medida que o grupo alquilo se torna maior (por exemplo, o T-butilbenzeno produz muito pouco produto Orto após a nitração em comparação com o tolueno). - – a natureza do efeito alternado nas cadeias de carbono. Part XXII. An attempt further to definite the probable mechanism of orientation in aromatic substitution
Christopher Kelk Ingold and Florence Ruth Shaw
J. Chem. Soc. 1927, 2918-2926
DOI: 10.,1039/JR9270002918
Um livro precoce pela influente Físico, Orgânico, Químico, Prof. C. K. Ingold, afirmando que halogenobenzenes são indutivamente elétron-retirada, mas, simultaneamente, com ressonância de estabilização. - the Anomalous Reactivity of Fluorobenzene in Electrophilic Aromatic Substitution and Related Phenomena
Joel Rosenthal and David I., Schuster
Jornal de Química Ensino de 2003, 80 (6), 679
DOI: 1021/ed080p679
muito interessante papel, apropriado para o curioso undergrads, e descreve algo que a maioria praticando químicos orgânicos vai saber empiricamente – fluorobenzene é quase como reativa como benzeno no EAS ou Friedel-Crafts reações, o que é contraditório quando se considera efeitos eletrônicos! - Organic chemistry
N. Haworth, C. K. Ingold, T. A. Henry
Ann. Rep. Prog. Chem. 1926, 23, 74-185
DOI: 10.1039/AR9262300074
An early paper discussing directing effects in EAS. P., 136 e 137 contêm figuras que retratam o fluxo de elétrons. Pg. 140 discusses meta-direction, which occurs for the’ opposite ‘ reasons as o/p-direction by alkyl groups.