în postarea anterioară am introdus Orto -, para – și meta-directori în substituția aromatică electrofilă. Anterior, am acoperit mecanismul de substituție aromatică electrofilă și am arătat că mecanismul trece printr-un intermediar de carbocare.,astăzi, vom lega aceste două concepte împreună și vom încerca să arătăm că dacă un substituent este un Orto-, para – sau meta – director depinde de modul în care substituentul afectează stabilitatea intermediarului carbocation.
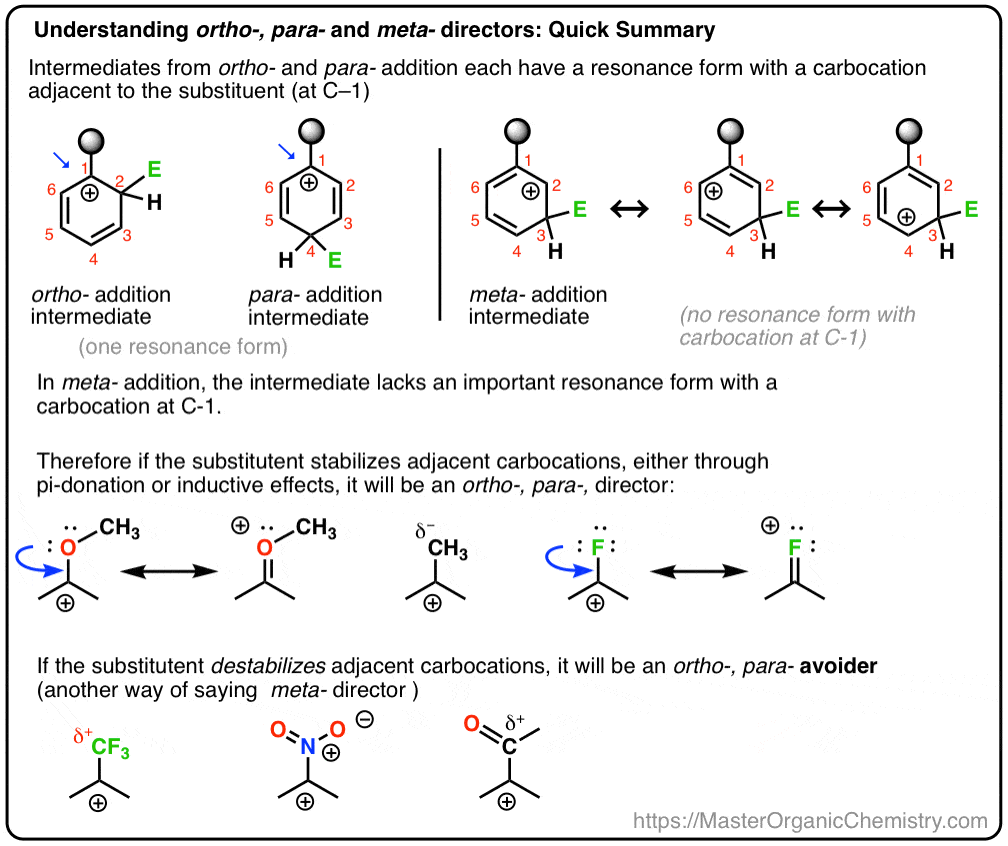
și vom vedea, de asemenea, de ce un nume alternativ pentru meta – director ar putea fi,”ortho -, para – avoider”. : – )
Cuprins
- Carbocations Sunt Stabilizate Prin Adiacent Atomi Cu Lone Perechi
- Studiu de Caz #1: Un orto-,para – Director (OCH3)
- Da, Oxigenul Este Electronegativ., Dar Donarea Perechii Sale Singuratice Mai Mult Decât Face Pentru Ea!
- diagrama energiei de reacție pentru un director Orto Para
- studiu de caz #2: un meta – director (CF3).
- ceea ce numim „meta– directori” sunt mai mult ca „Orto-, para– Avoiders”
- diagrama energiei de reacție pentru un meta – Director
- deci de ce sunt halogeni Orto-, Para – directori?
- Note
- Quiz-te!,
- (Avansat) Referințe și lecturi Suplimentare
Carbocations Sunt Stabilizate Prin Adiacent Atomi Cu Lone Perechi
să ne gândim înapoi la factorii care crește stabilitatea carbocations. Carbocațiile sunt specii sărace de electroni cu șase electroni în carcasa lor de valență. Deci, orice substituent care poate dona densitatea electronilor către carbocație se va stabiliza. Aceasta include:
- substituenți cu eliberare de electroni care pot acționa ca „donatori de sigma” (de ex., multe grupe alchil, care doneaza densitate de electroni prin efecte inductive )
- adiacente atomi cu lone perechi, care pot acționa ca „pi donatori” la carbocationul
- adiacente C–C pi obligațiuni care pot stabiliza carbocationul prin taxa de delocalizare („rezonanță stabilizare”, cu alte cuvinte).
și factorii care destabilizează carbocațiile?
- orice substituent care elimină densitatea electronilor dintr-o carbocație, cum ar fi grupuri puternice de retragere a electronilor.
deci, aici este un test rapid., Având în vedere tot ce este scris mai sus, care dintre cele două carbocații de mai jos va fi mai stabilă?
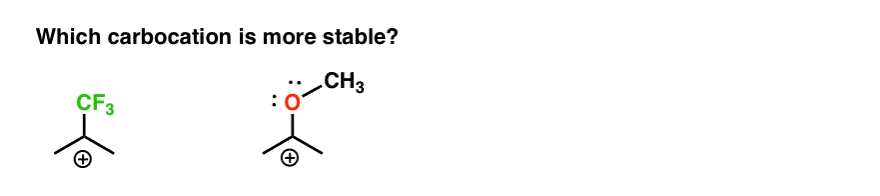
Dacă puteți răspunde la această întrebare, ei bine, esti cel mai de calea spre înțelegerea diferenței dintre orto-, para – și meta – administrație.să examinăm două studii de caz. Vom analiza o reacție generică de substituție aromatică electrofilă a benzenului cu un Orto-, para – director (metoxibenzen) și vom examina intermediarii care sunt obținuți din atacul la pozițiile Orto, meta și para., Apoi vom efectua același exercițiu cu un meta-director (trifluormetilbenzen).în acest proces, sperăm să înțelegem de ce metoxibenzenul favorizează orto – și para– produsele, în timp ce trifluormetilbenzenul favorizează meta – produsul.
Studiu de Caz #1: Un orto-,para – Director (OCH3)
Electrofile aromatice substituirea dimetoxibenzen tinde să dea orto – și para – produse cu foarte puțin meta- ., Iată ce se întâmplă în nitrarea, de exemplu:
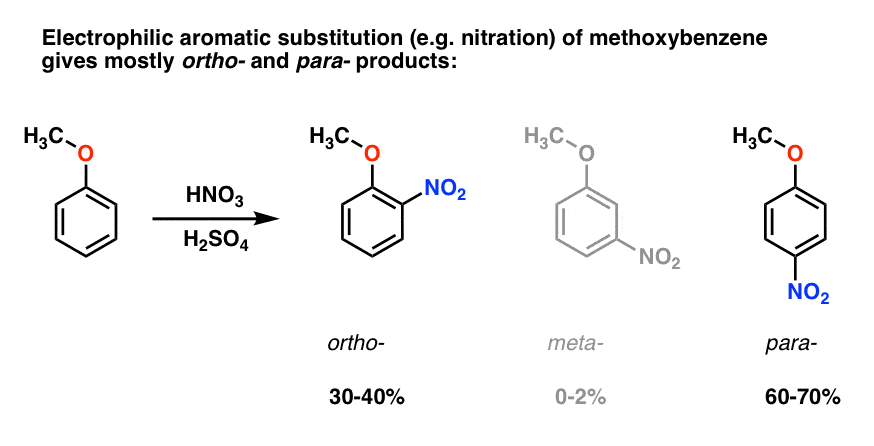
para – produs domină (60-70%), cu orto – aproape de spatele (30-40%) și doar o urmă de meta– .
De ce?
3. Da, Oxigenul Este Electronegativ. Dar Donarea Perechii Sale Singuratice Mai Mult Decât Face Pentru Ea!
iată calea care duce la produsul Orto., Rupem o legătură C–C pi și formăm o nouă legătură C-E (Unde E este destinat să reprezinte un electrofil generic), generând o carbocație stabilizată prin rezonanță:
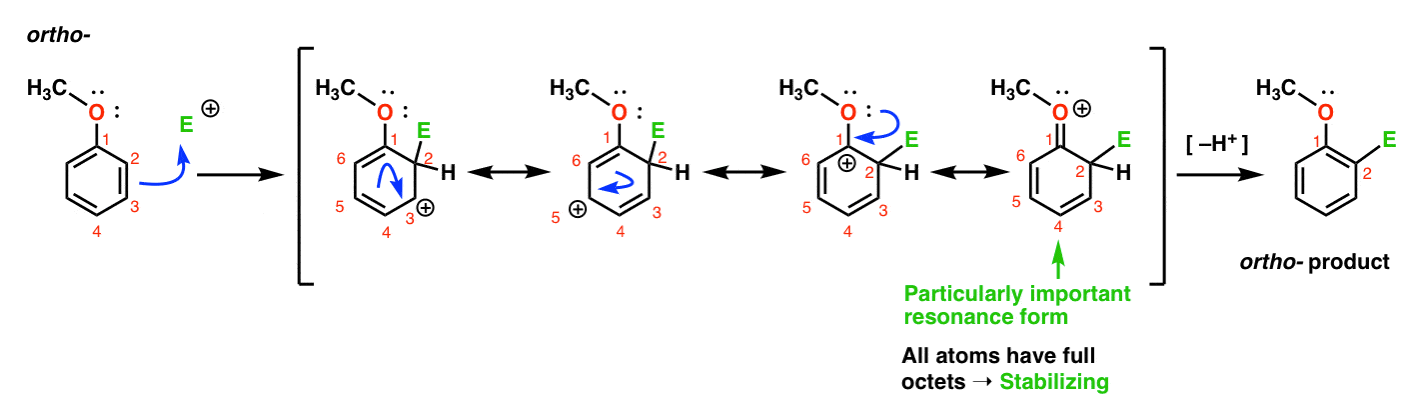
Dacă vă uitați atent, trebuie să rețineți că putem forma patru forme de rezonanță . Trei dintre ele poartă carbocații complete (pe C1, C3 și C5), dar este cea de – a patra – forma de rezonanță în care există o legătură C=O pi-ceea ce este deosebit de important. De ce? În această formă de rezonanță, toți atomii de carbon au un octet complet de electroni., Asta pentru că oxigenul legat direct de inel poate dona o pereche singuratică carbocării adiacente, formând o legătură pi. Acesta este un exemplu de donație pi.
iată calea pentru atacul electrofilului la meta-poziție. Rețineți diferența!
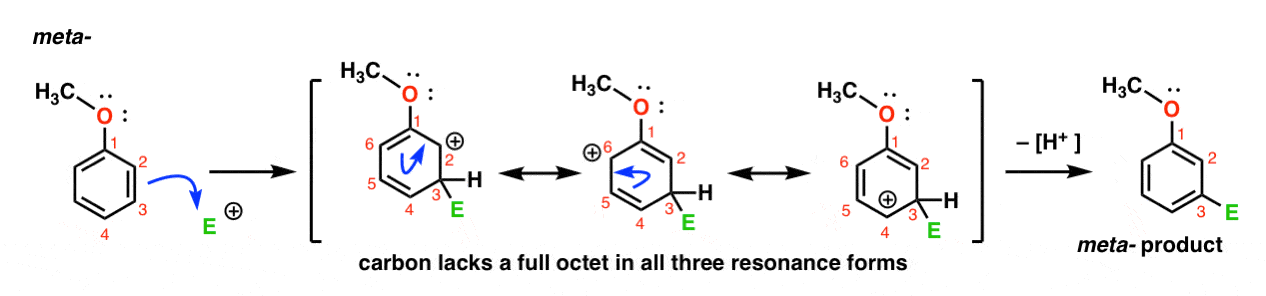
Atacul electrofil la C-3 rezultate într-un carbocationul care poate fi delocalizat prin rezonanță, C2, C4 și C6. Cu toate acestea, nu există nicio modalitate de a „muta” carbocația la C1, ceea ce înseamnă că nu există o formă de rezonanță rezonabilă în care toți atomii au octeți plini.,acest lucru face ca intermediarul meta – carbocation să fie mult mai puțin stabil decât intermediarul Orto – carbocation.
în cele din Urmă, aici este reacția care conduce la para – produs:
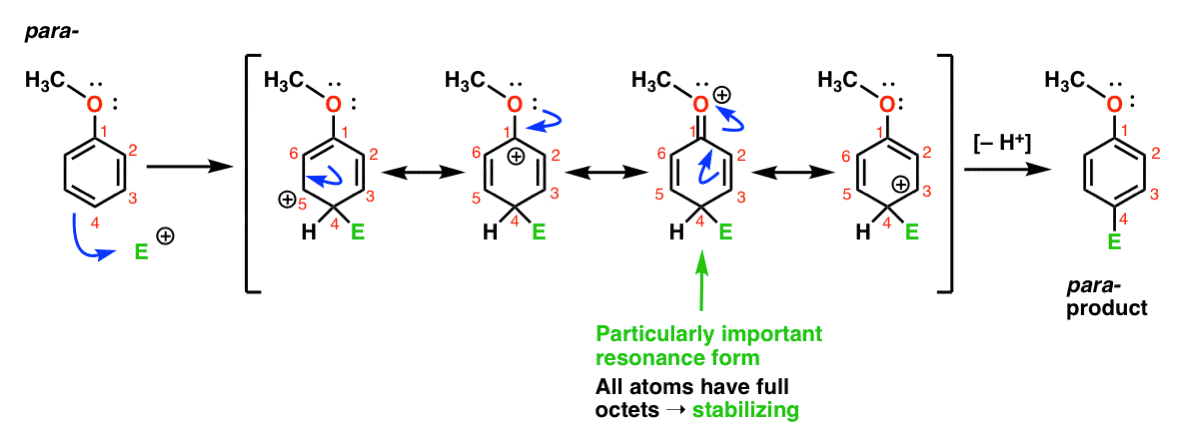
Aici putem trage din nou de rezonanță forme cu carbocations pe C1, C3 și C5, precum și un al patrulea de rezonanță de formă în cazul în care atașat atom de oxigen donează o pereche de electroni la carbocationul pe C1, rezultând într-o deplină octet la carbon. Aceasta este o situație în esență aceeași cu cea Orto-intermediară.,
Astfel, prin analiza de rezonanță forme (și pe cuvântul meu, ați putea fi rugat să facă același lucru pe un test in viitorul apropiat), putem vedea că intermediare carbocations rezultă din orto – și para– plus sunt mult mai stabile decât cele intermediare din meta– plus.acest lucru explică de ce domină produsele orto și para, iar meta – produsul este minor.
ar putea fi util să vizualizați acest lucru desenând o diagramă a energiei de reacție.
4., Diagrama energiei de reacție pentru un director Orto-Para
starea de tranziție care duce la produsele orto – și para – adiție este mult mai scăzută în energie decât meta– .
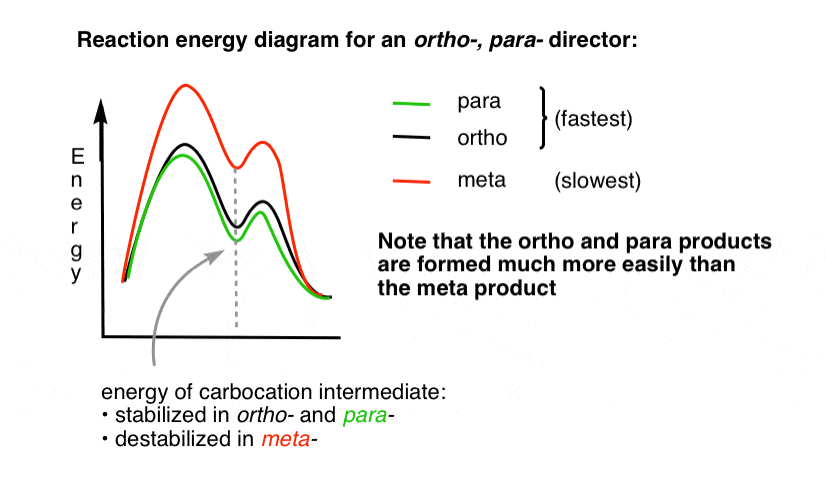
O intrebare – de ce crezi că para – ar fi favorizat (de exemplu, 60%-70% randament pentru para– produs de nitrarea, de mai sus, față de 30-40% pentru orto-) chiar dacă există două orto – poziții și numai una para- ?
gândiți-vă la asta pentru un minut și o vom aborda mai jos.
5. Studiu de caz #2: un meta – director (CF3).
deci, ce zici de CF3?, De ce dă meta – produse? Să facem același tip de analiză.
iată calea care duce la produsul Orto. Ca și în cazul Orto-intermediarului de mai sus, putem desena trei forme de rezonanță care plasează carbocația pe C1, C3 și, respectiv, C5.
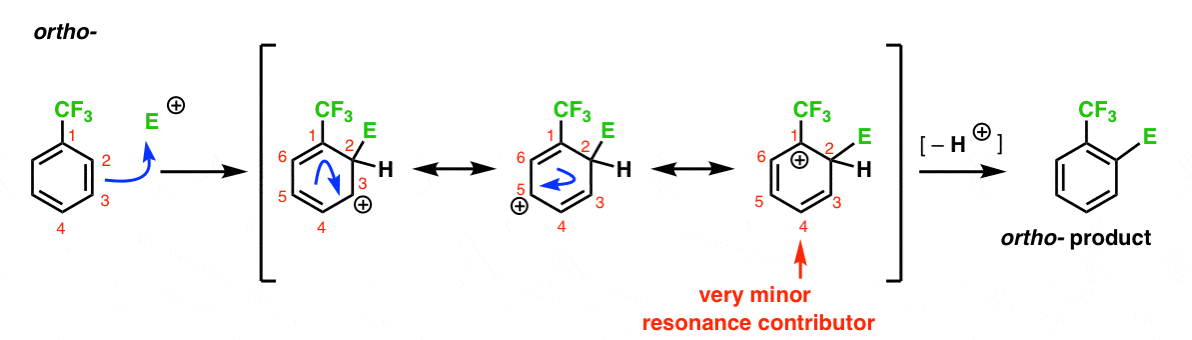
Deci, ce este diferit în acest caz?ceea ce este diferit este prezența unui grup puternic de retragere a electronilor (CF3) la C1, iar acest lucru schimbă complet jocul.după cum am spus, carbocațiile sunt destabilizate de vecinii care retrag densitatea electronilor., Prin urmare, ne-am aștepta ca acesta să fie un contribuitor de rezonanță foarte minor, astfel încât sarcina pozitivă este delocalizată doar peste C3 și C5.
am observat că CF3 este un meta – director. Este rezonabil să credem că există ceva despre meta– care o face deosebit de stabilă. Analizând intermediarul pentru meta-produsul de mai jos, puteți vedea de ce?
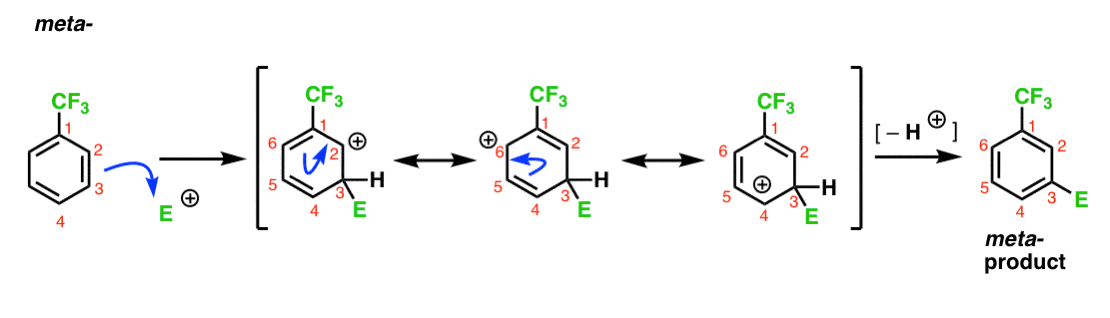
Hmmm. Nu există nici un intermediar în cazul în care un carbon are un octet plin. Nu există forme de rezonanță deosebit de stabile.
este un fel de „meh”, nu-i așa?
6., Ceea ce numim „meta– directori” sunt mai mult ca „Orto-, para– Avoiders”
pe de altă parte, nu există nici o formă de rezonanță deosebit de instabilă. Deoarece sarcina pozitivă este localizată pe C2, C4 și C6, se evită o situație în care sarcina pozitivă este direct adiacentă grupului CF3 de retragere a electronilor. Iar sarcina pozitivă este astfel delocalizată frumos pe tot parcursul inelului, spre deosebire de orto – situația de mai sus.deci, este un intermediar „mai puțin rău” decât Orto-., în cele din urmă, para – intermediarul are aceeași problemă ca și Orto- ; un intermediar cu o sarcină pozitivă pe C1, adiacent CF3.
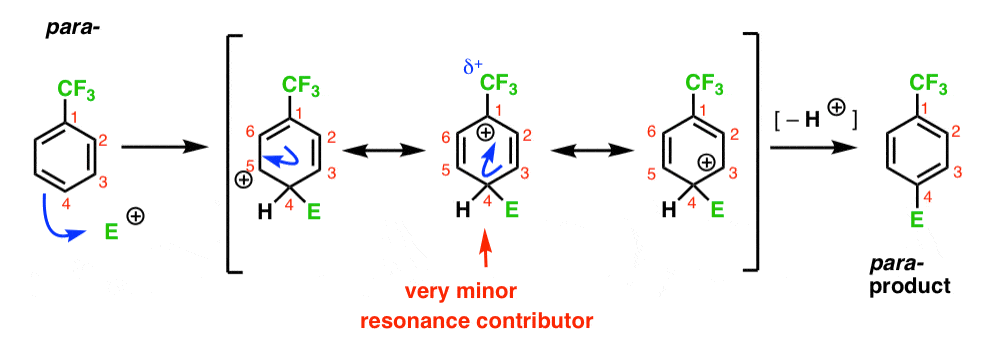
Acest lucru duce în doar două importante forme de rezonanță, ceea ce duce la o mai puțin delocalizați (și, prin urmare, mai puțin stabile) carbocationul intermediar.
linia de fund: intermediarul meta carbocation este mai stabil decât Orto – sau para-intermediarii.dar nu pentru că substituentul în sine are vreun efect stabilizator asupra meta– intermediarului. .,
aș argumenta că este mai util să ne gândim la meta-ca fiind mai puțin instabil decât orto – și para -.în acest fel, nu este atât de mult că CF3 este un meta-director, atât de mult încât este un ” Orto–, para-avoider. „
7. Diagrama energiei de reacție pentru un meta-Director
Iată o schiță a diagramei energiei de reacție:
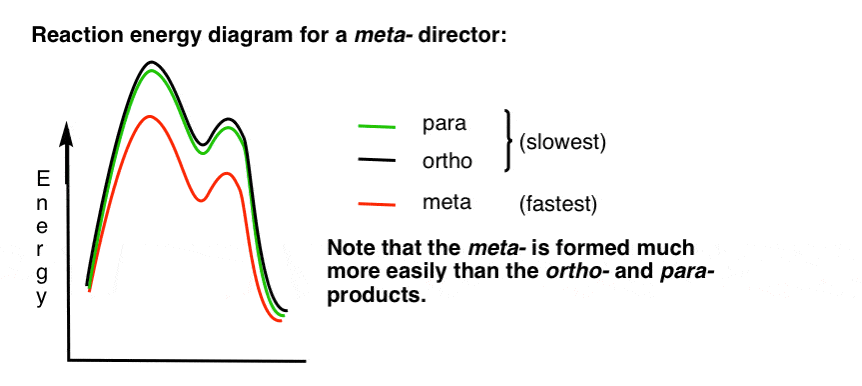
în regulă.
înapoi la întrebarea noastră inițială. Deci, care carbocație este mai stabilă?,
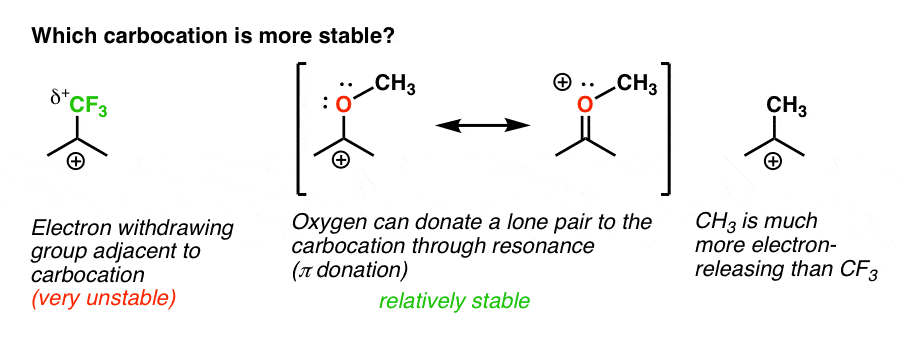
în mod Evident, carbocationul cu un teren de oxigen care poartă o singur pereche este mult mai stabil decât un carbocationul adiacente pentru un electron-retragerea de grup ca CF3.
și care cuprinde diferența dintre un Orto -, para-director ca OCH3 și un meta – director ca CF3.este demn de remarcat faptul că majoritatea grupărilor alchil (cum ar fi CH3 ) nu au o pereche singură, dar sunt încă Orto-, para – directori., Acest lucru este în concordanță cu tot ceea ce am invatat pana acum despre cum alchil grupuri sunt, în general, pentru stabilizarea carbocations – amintesc că carbocationul stabilitate, în general, crește cu substituție
Deci, despre aceste para– produse…
de Ce sunt para – produse fabricate la o rată mai mare decât orto- ?răspunsul este o piedică sterică. atacul la poziția para este mai puțin grevat de substituent decât atacul la pozițiile Orto.
deci, de ce sunt halogeni Orto -, Para – directori?
Acest lucru ne lasă cu exemplul oarecum complicat de halogeni.,de ce sunt Orto -, para – directori de fluor, clor, brom și iod, chiar dacă dezactivează grupurile?
răspunsul nu ar trebui să fie o surpriză dacă ați urmărit de-a lungul, dar vom lăsa acest lucru până la următoarea postare, deoarece acesta este deja suficient de lung.
Next post: de ce sunt halogeni Orto-, para – directori?
Note
Nota 1. Este mai corect să spunem că orto-și para – produsele domină, deoarece stările de tranziție care conduc la aceste produse sunt mai scăzute în energie decât energiile intermediarilor înșiși., La urma urmei, energia stărilor de tranziție determină bariera de activare și, prin urmare, rata de reacție.
Nota 2. Sau hiperconjugare, pe care majoritatea manualelor (cu excepția notabilă a lui Maitland Jones) o evită în general.
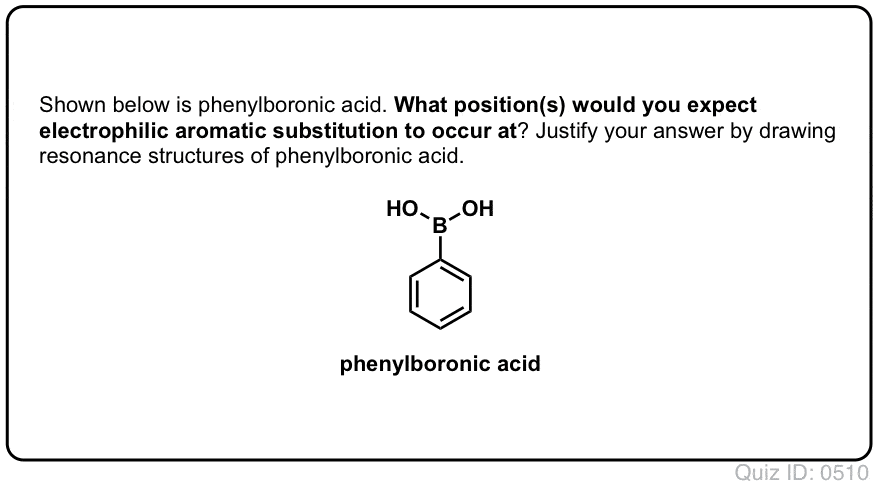
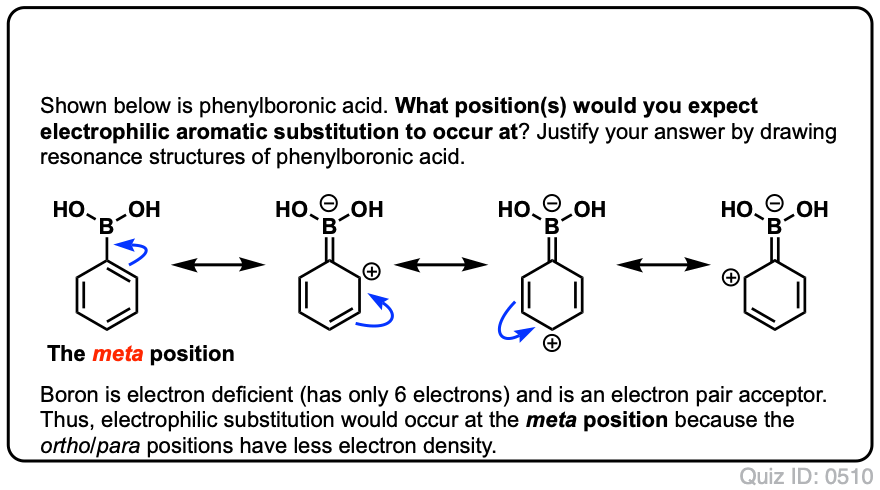
Testează-te!,/div>
 Click pentru a Flip
Click pentru a Flip
 Click pentru a Flip
Click pentru a Flip 
 Click pentru a Flip
Click pentru a Flip 
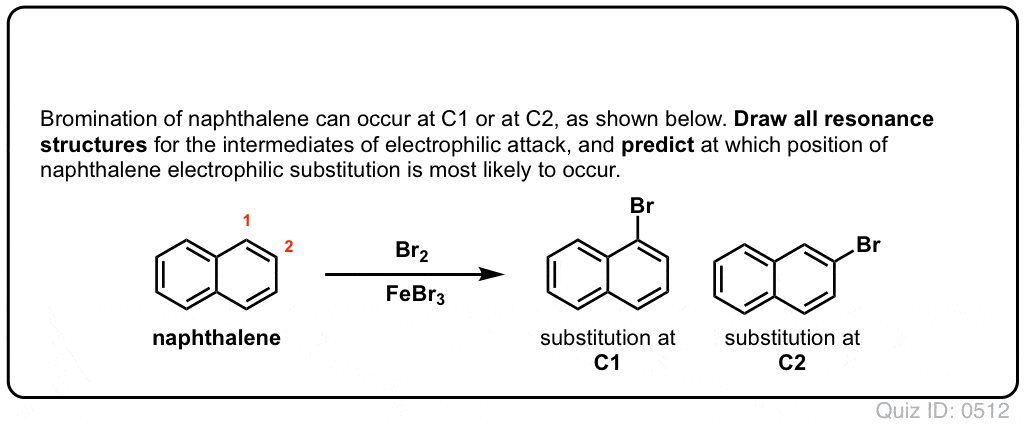 Click pentru a Flip
Click pentru a Flip 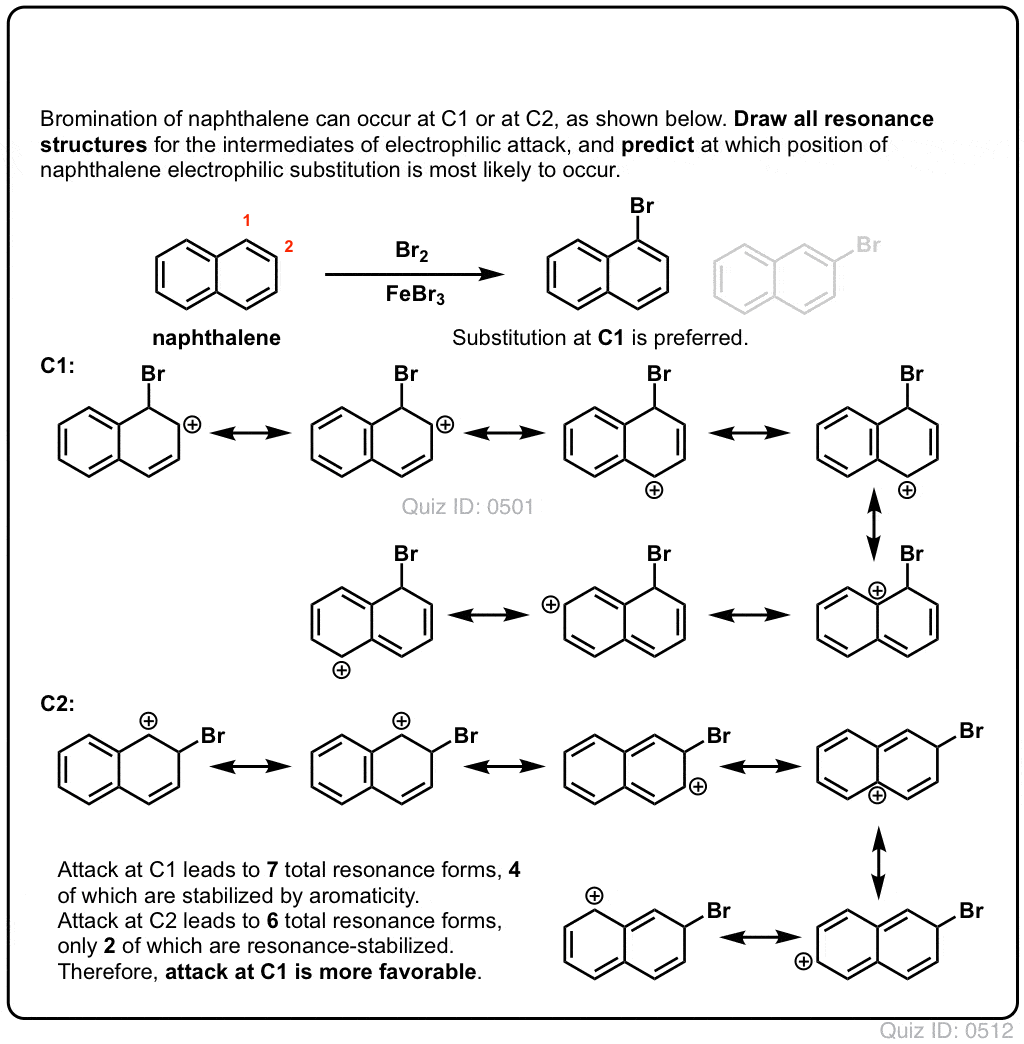
(Avansat) Referințe și lecturi Suplimentare
- A., F. Holleman, Die direkte Einführung von Substituenten in den Benzolkern
Rec. Trav. Chim. Pays-Bas 1910, 12, 455-456
DOI: 10.1002/recl.19100291205
A. F Holleman din 1910 a spus că ortho–para orientare este asociat cu activarea și meta orientare cu dezactivarea. - – natura efectului alternativ în lanțurile de carbon. Partea XXIII. Anormale orientare către halogeni, și poartă cu privire la problema de orto–para raport, în aromatic de substituție
Christopher Kelk Ingold și Charles Cyril Norrey Vass
J. Chem. Soc. 1928, 417-425
DOI: 10.,1039 / JR9280000417
această lucrare discută efectele direcționării în 1,2-dihalobenzeni. - unele observații privind impedanța sterică și efectele substituenților asupra raportului Orto: para în substituția aromatică
P. B. D. de la Mare
J. Chem. Soc. 1949, 2871-2874
DOI: 10.1039/JR9490002871
În această lucrare, de la Mare, discută diverse factori care ar putea cont pentru o predominanță de para peste orto selectivitate, după împărțirea randament de ortopedie produs de 2 (deoarece sunt 2 ortopedie poziții, dar numai 1 alin poziția în monosubstituiti benzene)., - efectele volumului grupărilor alchil în compușii aromatici. Partea V. monosulfonarea lui p-cymene
R. J. W. Le Fèvre
J. Chem. Soc. 1934, 1501-1502
DOI: 10.1039/JR9340001501
In p-cimen, cel mai important produs obținut de la electrofile sulfonarea este 2-produs (ortho la gruparea metil), probabil din cauza sterics. - Efecte de Grupe Alchilice în Electrofile Adăugiri și Substituiri
COHN, H., HUGHES, E., JONES, M. și PEELING, M. G.
Natura 1952, 169, 291
DOI: 1038/169291a0
Această lucrare a datelor compararea nitrarea de t-butylbenzene și toluen., T-butylbenzene este mult mai mult p-regie decât toluenul (79.5% para pentru t-butylbenzene vs 40% para pentru toluen), care este probabil din cauza sterics (ortho abordare este blocat de mai consistente de t-butil-grup). - distribuția izomerilor în Mononitrarea etil-și Izopropilbenzenului. Dovezi suplimentare pentru un efect Steric în distribuția izomer
Herbert C. Brown și W. Hallam Bonner
Journal of the American Chemical Society 1954, 76 (2), 605-606
DOI: 10.,1021/ja01631a084
Tabelul II în această lucrare ilustrează faptul că ortopedie produs obținut la nitrarea de monoalkylbenzenes scade ca alchil grup devine mai mare (de exemplu, t-butylbenzene randamente foarte puțin orto produs la nitrarea comparativ cu toluen). - – natura efectului alternativ în lanțurile de carbon. Partea XXII. o încercare de a defini în continuare mecanismul probabil de orientare în substituție aromatică
Christopher Kelk Ingold și Florence Ruth Shaw
J. Chem. Soc. 1927, 2918-2926
DOI: 10.,1039/JR9270002918
devreme hârtie de influente Fizice Chimist Organic, Prof. dr. C. K. Ingold, care să ateste că halogenobenzenes sunt inductiv electron-retragere, dar în același timp rezonanță-de stabilizare. - reactivitatea anormală a Fluorobenzenului în substituția aromatică electrofilă și fenomenele conexe
Joel Rosenthal și David I., Schuster
Jurnal al Învățământului Chimic 2003, 80 (6), 679
DOI: 1021/ed080p679
Un foarte interesant hartie, potrivit pentru curios studenți, și discută despre ceva care cele mai multe practicarea organic va ști empiric – fluorobenzene este aproape la fel de reactive ca benzen în EAS sau Friedel-Crafts reacții, care este contraintuitiv, atunci când se consideră efecte electronice! - Chimie Organică
N. Haworth, CK Ingold,T. A. Henry
Ann. Rep. Prog. Chem. 1926, 23, 74-185
DOI: 10.1039/AR9262300074
O mai devreme lucrarea despre regie efecte in AE. Pp., 136 și 137 conțin cifre care descriu fluxul de electroni. Pg. 140 discută despre meta-direcție, care apare din motive „opuse” ca o/p-direcție de grupări alchil.