introducere
leucemia cu celule păroase (HCL) este o neoplazie limfoidă cu celule B. HCL se diferențiază de alte neoplasme ale celulelor B datorită caracteristicilor sale morfologice, imunofenotipice și moleculare. Caracteristica sa principală este acumularea de celule B monoclonale, cu proiecții asemănătoare părului pe suprafața sa, care se găsesc în principal în sângele periferic, măduva osoasă și splina. A fost descrisă în 1958 de Bournoncle et al. Cu toate acestea, ei au numit-o reticuloendotelioză leucemică.,1 termenul „celule păroase” a fost inventat în 1996 de Schrek et al.2 Astăzi este clasificat de Organizația Mondială a Sănătății ca limfom non-Hodgkin cu celule B.3
definiție
HCL este o afecțiune rară, cronică, limfoproliferativă a celulelor B. Caracteristicile sale principale sunt prelungirile citoplasmatice care conferă celulelor un aspect păros.
etiologie
deși există diferite studii care arată o legătură între expunerea la anumiți agenți și HCL, etiologia sa nu a fost clar stabilită, ceea ce ar putea fi explicat datorită incidenței sale scăzute., Printre agenții care s-au dovedit a fi o legătură pozitivă sunt: expunerea la pesticide,4 erbicide, uleiuri minerale, care lucrează ca tâmplar sau fermier.4-7 recent,a fost descrisă o legătură pozitivă cu dimensiunea, 5 în timp ce fumatul are o asociere inversă, în special la bărbați.8 nu se cunoaște mecanismul specific care conferă protecția; cu toate acestea, s-a sugerat că fumatul reduce severitatea mecanismelor inflamatorii9 și că nicotina induce apoptoza în limfocite.10
Epidemiologie
HCL reprezintă 2-3% din toate leucemiile. Există 600 de cazuri noi raportate pe an în SUA (3.,2 cazuri la un milion de locuitori). Vârsta mediană la diagnostic este de 52 de ani și este mai frecventă la bărbați decât la femei, cu un raport 4:1; cu o incidență mai mare în populația albă, în special în rândul evreilor Ashkenazi.3 în Mexic, HCL reprezintă 1, 12% din toate leucemiile. Cu toate acestea, în partea de nord a țării reprezintă până la 1.83%, similar cu informații de la U. S. 11,12
Fiziopatologie
HCL este o boala cronica, limfoproliferative B-celule tulburare. Cu toate acestea, celulele sale nu au aspectul unei sub-populații de celule B, iar originea sa a fost o chestiune de dezbatere., Analiza genelor regiunilor variabile ale imunoglobulinelor (Ig) este un instrument folosit pentru a descoperi originea clonală a celulelor limfoide.13 în peste 85% din cazuri, suntem capabili să găsim mutații somatice în genele Ig regiuni variabile ale celulelor HCL,14,15, ceea ce este un indiciu că celulele implicate au trecut prin Centrul germinal sau organele periferice limfoide.Aproximativ 40% din celulele HCL co-exprimă mai multe izotipuri Ig legate de clonare.17
dovezile sugerează un centru de origine post germinal în memoria celulelor B, datorită profilului lor de Expresie genomică.,18,19 originea celulelor B de memorie este compatibilă cu lipsa de translocare reciprocă cromozomică a HCL.20 absența CD27 este tipică în HCL. Aceasta reprezintă un punct împotriva ipotezei originii sale în celulele B de memorie.21 cu toate acestea, au fost observate celule B cu memorie CD27 negativă.22 deoarece afecțiunea ganglionilor limfatici este rară, s-a sugerat că celula de origine a HCL este probabil localizată în măduva osoasă sau splină, deoarece acestea sunt de obicei locurile mai afectate. Celulele HCL prezintă un profil de Expresie similar cu zona marginală a splinei.,Aspectul caracteristic al HCL se datorează expresiei beta-actinei, care este polimerizată la F-actină, localizată în citoscheletul cortical.24 PP52 fosfoproteina, care este specifică leucocitelor, este legată de F-actină și este responsabilă pentru susținerea proiecțiilor asemănătoare părului.25 pe de altă parte, secvențierea genelor HCL a identificat recent prezența unei mutații BRAF V600E la aproape fiecare pacient cu boala, absent în alte malignități limfoide cu celule B.Mutațiile 26,27 BRAF activează calea MAPK, promovând creșterea, supraviețuirea și diferențierea celulelor HCL.,28
prezentare clinică și constatări de laborator
evoluția clinică a bolii este indolentă. Majoritatea pacienților prezintă de obicei slăbiciune și oboseală ca simptome predominante în timpul debutului bolii.29 uneori, există un istoric de infecții repetate. Constatările examenului fizic sunt: splenomegalie în 96%, hepatomegalie în 58% și limfadenopatie în doar 35%. Aceste ganglioni limfatici umflați sunt rareori observați la periferie; cu toate acestea, ele sunt în general prezente în abdomen și detectate prin studii imagistice.,30
într-un stadiu avansat al bolii suntem capabili de a găsi durere în cadranul superior stâng, infecții, febră, și hemoragii și/sau pierdere în greutate. Cu toate acestea, acest lucru este neobișnuit din cauza disponibilității și eficacității tratamentului.30,31 manifestări clinice sunt produse ale acumulării de celule păroase în splină, ficat și măduvă osoasă (Tabelul 1).32
manifestări clinice.,
| Splina | Ficat | măduvă Osoasă | ganglionii Limfatici |
|---|---|---|---|
| celule se acumulează în pulpa roșie și atrofie pulpa alba. Ele formează mai târziu așa-numitele „pseudo-sinusoide” prin înlocuirea celulelor endoteliale ale pulpei roșii prin canale vasculare îmbunătățite, contribuind la anemie. aici se acumulează atât în sinusoidele hepatice, cât și în tractul portal., Există fibroză în acesta din urmă datorită acidului hialuronic abundent, care stimulează celulele păroase să producă fibronectină, cu fibroza corespunzătoare. | în acest domeniu, există o producție extinsă de fibroză și suprimarea hematopoiezei. Factorul cheie este interacțiunea celulelor păroase cu acidul hialuronic din matricea extracelulară, generând factori de creștere fibroblastici (FGF) și stimulând celulele malign să producă și să secrete fibronectina. | în general, absent al bolii. Lipsa receptorilor pentru intrarea celulelor păroase., |
Respect to lab studies, it is frequent to observe anemia in 85%, thrombocytopenia in 60.80% and leukopenia in 60% due to hypersplenism and bone marrow infiltration.30
Differential diagnosis
HCL must be differentiated from other indolent lymphoid malignancies such as prolymphocytic leukemia, splenic marginal zone lymphoma, mantle cell lymphoma and HCL variant (HCL-v)., Ultima apare în 10% din cazuri, cu o medie de vârstă de 70 de ani, și în ciuda asemănărilor cu clasic cu celule păroase leucemie, ele diferă în absența CD25 și CD123 immunophenotypic markeri. Un alt mod de a face un diagnostic diferențial este lipsa răspunsului la tratamentul standard cu HCL și inexistența mutațiilor genei BRAF V600F.30
metode de diagnosticare
diagnosticul HCL se face în mod obișnuit cu o biopsie și aspirație a măduvei osoase combinate cu caracterizarea imunofenotipică prin citometrie în flux.,33 este important să subliniem că această patologie este de obicei sub-diagnosticată și necesită suspiciune clinică și utilizarea tehnologiei adecvate pentru a rezolva această problemă. După cum s-a menționat anterior, majoritatea pacienților (70-90%) prezintă pancitopenie, cu leucopenie (
×109/l), anemie (g/dL), neutropenie (×109/l), monocitopenie (×109/L) și trombocitopenie (×109/l). Numai între 10% și 20% prezintă leucocitoză moderată (>10×109/L). Pacienții cu HCL prezintă niveluri serice crescute ale IL-2R (CD25), care se corelează cu gradul de activitate al bolii.,34 alte teste care trebuie luate în considerare la stabilirea diagnosticului sunt nivelurile serice de imunoglobulină, precum și mutațiile somatice ale genei IgVH și BRAF V600E.32 Unele HCL histopatologic și immunophenotypic caracteristicile sunt următoarele:
- •
Limfocite citometrie în flux în sânge periferic sau măduvă osoasă cu CD19, CD20, FMC7, CD11c, CD103, CD25, HC2, CD22, sIg, CD79a și CD123 expresii, cu patru fiind principalul și markeri specifici: CD11c, CD103, CD25 și CD123.34 Frecvent negative markeri sunt CD5, CD23, CD10, CD79b și CD27.,32
- •
o expresie puternică pentru CD200 este caracteristică HCL și poate fi utilă în diagnosticarea cazurilor dificile.Aspirația măduvei osoase cu un ac poate fi dificil de obținut și este adesea neproductivă sau „uscată”. Într-o biopsie a măduvei osoase, putem observa fibroza, cu un aspect celular „ou prăjit” cauzat de spațiile largi dintre nuclee și citoplasma abundentă. Sunt efectuate analize imunohistochimice pentru CD20 și TRAP (fosfatază acidă rezistentă la tartrat), DBA-4 și anexa A1, care sunt caracteristice pozitive.,32
Andrulis și colab. a condus un studiu în care a fost raportată eficiența anticorpului VE1 pentru detectarea BRAF V600E, împreună cu identificarea HCL în alte entități. Mai mult, un studiu realizat de Uppal și colab. s-a găsit o sensibilitate de 88% și o specificitate de 97% pentru a detecta această mutație cu anticorpul menționat.34
tratamentul curent
HCL are în mod regulat o evoluție indolentă. Așteptarea și observarea reprezintă o opțiune bună pentru pacienții asimptomatici, deoarece tratamentul precoce nu oferă niciun fel de beneficiu în ratele de supraviețuire ale acestor cazuri., Oricum, progresia bolii la majoritatea pacienților va duce la complicații ca urmare a citopeniilor și splenomegaliei; adică anemie, hemoragii, infecții recurente etc. În practica generală, tratamentul trebuie început dacă apare oricare dintre criteriile enumerate în tabelul 2.35 când se ia decizia de a nu începe tratamentul, monitorizarea clinică și de laborator trebuie efectuată o dată la trei luni în primul an și o dată la șase luni după aceea.,35 tratamentul cu HCL nu este considerat vindecător; dar strategiile actuale de tratament sunt capabile să atingă remisiuni prelungite, crescând astfel ratele de supraviețuire globală (algoritmul 1).36-39
criterii pentru a începe tratamentul.
1. Splenomegalie simptomatică
2. Citopenie care implică cel puțin una dintre următoarele:
-hemoglobină g/dL
-trombocite ×109/L
-neutrofile ×109/l
3., Infecții Severe
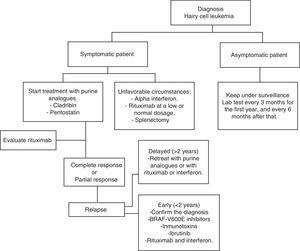
grafic pentru managementul unui pacient cu leucemie cu celule păroase.
analogi Purinici
În 1960, s-a constatat că 30% dintre copiii cu imunodeficiență combinată severă sindromul lipsit de adenozin dezaminază enzimă (ADA).,40 mai mult, au descoperit că acumularea formei de deoxiadenozin trifosfat a fost responsabilă pentru scăderea limfocitelor.41 ținând cont de aceste observații, s-au dezvoltat medicamente capabile să se lege ireversibil de ADA sau să antagonizeze acțiunea sa. După tratamentul cu analogi purinici, acumularea de deoxiadenozin trifosfat are ca rezultat ruperea și inhibarea reparării ADN-ului, ceea ce se traduce în apoptoza celulară.,42
Pentostatin
de Asemenea, cunoscut sub numele de 2′-deoxycoformycin (dcF), un produs de Streptomyces antibioticus și ADA inhibitori, introdus pentru prima dată în 1980 ca prima analogi purinici pentru HCL tratament. În tabelul 3,37,39,43,44 studiile specifice arată ratele de răspuns la pentostatină. Administrare intravenoasă de pentostatin la 4 mg/m2 raport o dată la fiecare două săptămâni până la atingerea răspunsul complet a fost aprobat în SUA Pentostatin este în siguranță la pacienții cu clearance-iluminat >60mL/min. Cu toate acestea, este necesară o reducere a dozei dacă această epurare este cuprinsă între 40 și 60 ml/min.,32 se recomandă hidratarea pacientului cu 1,5 L soluție intravenoasă la fiecare ciclu de pentostatină.Răspunsul Global variază între 88% și 96%, în timp ce răspunsul complet este cuprins între 44% și 81%. Flinn și colab. a estimat o rată de supraviețuire de 5 și 10 ani de 90% și, respectiv, 81%, cu o durată medie de urmărire de 9,3 ani.45 Pentostatina este în general bine tolerată, iar cele mai frecvente efecte adverse sunt anemia, trombocitopenia și neutropenia.,46 Totuși, pentostatin a fost raportată să scadă CD4+ și CD8+ limfocite contează în mod semnificativ, care ar putea crește tumori maligne secundare și incidența infecțiilor.47,48
cladribină
este cunoscut sub numele de 2-clorodeoxiadenozină (CdA). În tabelul 4,49-52 studiile indică eficacitatea acestuia. Schema cea mai utilizată constă în administrarea a 0,1 mg/kg/zi într-o perfuzie continuă timp de 7 zile. Într-un studiu non-randomizat, au existat dovezi care să demonstreze că nu a existat nicio diferență semnificativă statistic în ceea ce privește răspunsul și intervalele de toxicitate între perfuzii (24h și 2h).,Un alt studiu randomizat a comparat administrarea zilnică față de administrarea săptămânală de cladribină; nu au existat rezultate semnificative în ceea ce privește răspunsul, supraviețuirea, ratele globale și de toxicitate.54 un studiu diferit a arătat că programul săptămânal a redus riscul de infecții.55 unul dintre avantajele administrării subcutanate este faptul că în majoritatea cazurilor nu necesită spitalizare. 0,14 mg/zi timp de 5 zile are o rată de răspuns de 95%, 56 similară administrării intravenoase. Programele subcutanate săptămânale au rate de răspuns și toxicitate similare cu cele zilnice.,57 cu un singur ciclu de cladribină, se poate obține un răspuns global de până la 100%, iar ratele totale de răspuns diferă de la 77% la 95%.49-52 Jehn et al. a raportat o supraviețuire globală la 12 ani de 79%.În general, cladribina este bine tolerată, citopeniile și febra fiind cele mai frecvente efecte adverse.
| Study | Patients | Follow-up | Plan | % CR | % PR | % GR | Outcome |
|---|---|---|---|---|---|---|---|
| Robak (1999) | 97 | 36 months | 2h infusion IV 0.12mg/kg/d 5 days |
77.3 | 18.,6 | 95.9 | Progression-free survival: 37.4 months |
| Rosenberg (2014) | 83 | NA | Continuous infusion IV 0.1mg/kg/d 7 days |
88 | 12 | 100 | Average global survival: 231 months |
| Goodman (2003) | 207 | 7 years | Continuous infusion IV 0.1mg/kg/d 7 days |
95 | 5 | 100 | Global survival at 108 months: 97% |
| Chadha (2005) | 86 | 9.7 years | Continuous infusion IV 0.,1mg/kg/d 7 days |
79 | 21 | 100 | Global survival at 12 years: 87% |
RC: complete response, RP: partial response, RG: global response.
Until now, there are no randomized prospective studies comparing pentostatin versus cladribine, in part because of the great efficiency of both drugs and due to low HCL incidence., Chiar și așa, există studii retrospective care dovedesc faptul că ambele medicamente au o eficacitate similară, în ceea ce privește răspunsul complet și supraviețuirea fără boală.analogii purinici rămân prima linie de tratament, dar noi descoperiri în ceea ce privește fiziopatologia HCL au dus la crearea de medicamente cu obiective terapeutice diferite. Aceste medicamente sunt în curs de cercetare și unele au arătat rezultate promițătoare.deoarece HCL este o malignitate a celulelor B, este logic să se utilizeze un anticorp monoclonal împotriva CD20,cum ar fi rituximab., Utilizat ca medicament autonom, rituximab poate atinge rate totale de răspuns de 10-54% la pacienții cu recidivă de HCL, la o doză de 375 mg/m2 o dată pe săptămână timp de 4-8 săptămâni.58,59 Else și colab. retrospectiv revizuite 18 pacienți care au fost tratați cu analogi purinici în combinație cu rituximab ca o a doua linie de tratament, după ce au fost tratați cu analogi purinici ca agenți unici. Toți pacienții au răspuns, cu o rată de răspuns complet de 89%.60
Rituximab la 375 mg / m2 pe săptămână timp de 8 săptămâni ca terapie inițială după administrarea 5.,6mg / m2 cladribină prin perfuzie 2-h IV timp de 5 zile generează un răspuns total de 100%.61 în situații speciale sau nefavorabile, 100mg de rituximab pe săptămână poate fi utilizat timp de 4-6 săptămâni. Acest lucru este mai puțin costisitor și este de obicei eficient, mai ales atunci când este combinat cu interferon.în timp ce analogii purinici pot să nu fie capabili să elimine HCL, deoarece boala reziduală minimă (MRD) detectată după administrarea cladribinei este întotdeauna puternic CD20+, eradicarea MRD poate fi obținută utilizând rituximab. Rivandi și colab., s-a dovedit într-un studiu preliminar că rituximab la doze convenționale pentru o perioadă de 8 săptămâni are o activitate mare, eliminând MRD la 13 pacienți, când este utilizat la 4 săptămâni după administrarea cladribinei.După cum s-a descris anterior, mutația BRAF V600E este cheia genetică în HCL. Prin urmare, este o țintă terapeutică care a fost studiată în ultimii ani. Vemurafenib este un inhibitor Oral BRAF V600E. Tiacci și colab., a efectuat un studiu pentru a măsura activitatea și siguranța Vemurafenib la pacienții cu HLC care au recidivat după tratamentul cu analogi purinici sau care au fost refractari la administrarea analogilor purinici. Rata globală de răspuns a fost de 96%, iar rata completă de răspuns a fost de 35%, cu o medie de supraviețuire fără recidivă de 19 luni. Reacțiile adverse au fost erupțiile cutanate, artralgia și artrita.Deoarece s-a observat o relație pozitivă între utilizarea Vemurafenib și apariția afecțiunilor maligne dermatologice, se recomandă explorări frecvente ale pielii.,Ibrutinib un inhibitor selectiv și ireversibil al tirozin kinazei Burton intervine în calea semnalizării celulelor B.Un test clinic de ibrutinib la pacienții cu recidivă a HCL a început recent. Datele preliminare privind eficacitatea și siguranța arată efecte adverse cum ar fi erupții, diaree și artralgie. Acest test clinic are loc în prezent în mai multe centre din SUA (NCT01841723).pentru a crește citotoxicitatea anticorpilor monoclonali, au fost create tehnici care facilitează producerea de conjugate anticorp–toxină sau anticorp–medicament., O imunotoxină este fuziunea dintre o toxină bacteriană (adică Pseudomonas exotoxină sau difterie) și fracția variabilă a unui anticorp monoclonal, a cărui țintă specifică se găsește pe suprafața celulelor neoplazice precum CD25 sau CD22. Această toxină este eliberată în interiorul celulei neoplazice și interferează cu sinteza proteinelor.65
BL22 este un immunotoxin împotriva CD22 fuzionat cu un trunchi de forma P. exotoxină PE38. Într-un test clinic de fază II, BL22 a fost testat în 36 de cazuri de recidivă a HCL sau de boală refractară., După un ciclu (40 mg / kg la fiecare două zile, trei doze), rata de răspuns complet a fost de 25%, iar rata de răspuns global a fost de 50%. Aceste răspunsuri s-au îmbunătățit până la o rată de răspuns totală de 47% și o rată de răspuns globală de 72% după reluarea tratamentului (numai la pacienții cu citopenii). Doi pacienți au dezvoltat sindrom hemolitic uremic fără a fi necesară repetarea plasmaferezei.66 Ulterior, moxetumomab pasudotox a fost dezvoltat ca o versiune modificată a BL22, cu o afinitate mai mare și citotoxicitate., Într-un test de fază I, care a inclus 28 de pacienți cu recidivă și rezistență la HCL, s-a obținut o rată de răspuns global de 86%, incluzând o rată de răspuns complet susținut la 46% dintre pacienți.67
opțiuni Terapeutice în circumstanțe nefavorabile
Chiar dacă HCL este tratată în cele mai dezvoltate țări cu cladribină și pentostatin, este o realitate faptul că aceste medicamente nu sunt doar scumpe, acestea nu sunt disponibile în Mexic și în multe țări cu resurse limitate., Deci, în aceste tipuri de circumstanțe, există și alte opțiuni terapeutice accesibile, cu rezultate favorabile
interferonul alfa pentru tratamentul pacientului cu HCL a fost introdus pentru prima dată în 1984. Astăzi, utilizarea sa este limitată, în principal datorită eficacității deosebite a analogilor purinici. Pe de altă parte, în țările cu resurse economice reduse, este o opțiune ieftină și una care a dovedit rezultate similare cu cele ale cladribinei în ceea ce privește supraviețuirea globală. Ruiz-Delgado și colab., a efectuat un studiu comparativ între interferon alfa (n=18) și cladribină (n=11), în care diferența de supraviețuire globală între cele două grupuri nu a fost semnificativă statistic; 94% la 217 luni în grupul cu interferon și 91% la 133 luni în grupul cu cladribină.68 într-un studiu realizat în centrul nostru, nouă pacienți cu HCL au primit trei mega-unități IFN de trei ori pe săptămână timp de 12 săptămâni, ulterior au primit din nou tratament timp de 8 săptămâni când a existat o reactivare a leucemiei sau după 10 luni de observație în fiecare an., Toți pacienții au avut o remisiune hematologică înainte de 12 săptămâni de tratament. Această opțiune terapeutică este mai ieftină, eficientă și comparabilă cu alte forme de terapie cu IFN în tratamentul și întreținerea pacienților cu acest tip de leucemie.Este posibilă combinarea interferonului cu rituximab fără creșterea efectelor toxice și îmbunătățirea eficacității.splenectomia a fost prima intervenție care a schimbat semnificativ supraviețuirea la pacienți. Astăzi, este rar folosit., Poate fi recomandată la pacienții cu splenomegalie masivă dureroasă (>10cm sub marginea costală) și cu infiltrare minimă a măduvei osoase sau la pacienții refractari la tratamentul cu interferon și analogi purinici.33 de studii Retrospective arată o rată de răspuns completă de 40-62% și o rată medie de supraviețuire la 5 ani până la 68%.70,71 Lad și colab. a publicat un studiu retrospectiv, care a inclus 24 de pacienți cu diagnostic de HCL, au fost împărțiți în două grupuri: 17 pacienți au primit cladribină și 7 au fost splenectomizați., 75% dintre pacienții din grupul cu splenectomie au prezentat remisiune totală, 94% au făcut acest lucru în grupul cu cladribină. O constatare interesantă la compararea ambelor grupuri a fost că nu s-au observat diferențe semnificative statistic în ceea ce privește supraviețuirea fără leucemie și supraviețuirea globală.72
prognostic
timpul de supraviețuire la pacienți după diagnostic a fost de 4 ani înainte de a fi cunoscut un tratament, din cauza complicațiilor derivate din citopenii, inclusiv hemoragii și infecții. După aceea, cu splenectomie ca tratament de primă linie, a existat un răspuns complet de 40-62% și o rată de supraviețuire de 5 ani la 61-68%., Apoi, interferonul alfa a fost utilizat ca primul medicament cu beneficii în tratamentul HCL. Totuși, rata completă de răspuns a fost scăzută, la 10%.Astăzi, cu analogi purinici (pentostatină și cladribină), răspunsul complet este indus până la 80% dintre pacienții cu o supraviețuire mediană de 10 ani. Ratele de răspuns Global sunt de 96-100%, cu o rată de răspuns completă de 80% și o rată de supraviețuire de 10 ani cuprinsă între 85% și 100%.În ciuda acestui fapt, o proporție semnificativă de pacienți cu HCL nu reușesc să răspundă la tratament sau devin rezistenți., Până la 48% dintre pacienți recidivează în următorii 15 ani.75 viitorul pacienților cu HCL este foarte favorabil. Provocarea este de a identifica această malignitate cât mai curând posibil și de a o trata în mod corespunzător folosind resursele disponibile.
Conflict de interese
autorii nu au conflicte de interese de declarat.