Obiectivele de Învățare
- Compara mutații punctiforme și mutații frameshift
- să Descrie diferențele între missense, prostii, și tăcut mutații
- să Descrie diferențele între lumină și întuneric de reparare
- Explica modul în care diferite agenții mutageni act
- Explica de ce Ames test poate fi folosit pentru a detecta agenți cancerigeni
- Analiza secvențelor de ADN și de a identifica exemple de tipuri de mutații
O mutație este o ereditare schimbare în secvența de ADN a unui organism., Organismul rezultat, numit mutant, poate avea o schimbare recunoscută a fenotipului în comparație cu tipul sălbatic, care este fenotipul cel mai frecvent observat în natură. O modificare a secvenței ADN este conferită ARNm prin transcriere și poate duce la o secvență de aminoacizi modificată într-o proteină la traducere. Deoarece proteinele îndeplinesc marea majoritate a funcțiilor celulare, o modificare a secvenței de aminoacizi într-o proteină poate duce la un fenotip modificat pentru celulă și organism.,efectele mutațiilor asupra secvenței ADN există mai multe tipuri de mutații care sunt clasificate în funcție de modul în care molecula ADN este modificată. Un tip, numit mutație punctuală, afectează o singură bază și apare cel mai frecvent atunci când o bază este înlocuită sau înlocuită cu alta. Mutațiile rezultă, de asemenea, din adăugarea uneia sau mai multor baze, cunoscute sub numele de inserție sau din îndepărtarea uneia sau mai multor baze, cunoscute sub numele de ștergere.
gândiți-vă
- ce tip de mutație apare atunci când o genă are două nucleotide mai puține în secvența sa?,
efectele mutațiilor asupra structurii și funcției proteice
mutațiile punctuale pot avea o gamă largă de efecte asupra funcției proteice (Figura 1). Ca o consecință a degenerării codului genetic, o mutație punctuală va duce în mod obișnuit la încorporarea aceluiași aminoacid în polipeptida rezultată, în ciuda schimbării secvenței. Această modificare nu ar avea niciun efect asupra structurii proteinei și se numește astfel mutație tăcută. O mutație missense are ca rezultat încorporarea unui aminoacid diferit în polipeptida rezultată., Efectul unei mutații missense depinde de cât de diferit chimic este noul aminoacid de aminoacidul de tip sălbatic. Locația aminoacidului modificat în cadrul proteinei este, de asemenea, importantă. De exemplu, dacă aminoacidul modificat face parte din situsul activ al enzimei, atunci efectul mutației missense poate fi semnificativ. Multe mutații missense au ca rezultat proteine care sunt încă funcționale, cel puțin într-o anumită măsură. Uneori, efectele mutațiilor missense pot fi evidente numai în anumite condiții de mediu; astfel de mutații missense sunt numite mutații condiționate., Rareori, o mutație missense poate fi benefică. În condițiile corecte de mediu, acest tip de mutație poate oferi organismului care îl adăpostește un avantaj selectiv. Un alt tip de mutație punctuală, numită mutație nonsens, transformă un codon care codifică un aminoacid (un codon sens) într-un codon stop (un codon nonsens). Mutațiile nonsens au ca rezultat sinteza proteinelor care sunt mai scurte decât tipul sălbatic și de obicei nu sunt funcționale.ștergerile și inserțiile provoacă, de asemenea, diverse efecte., Deoarece codonii sunt tripleți de nucleotide, inserțiile sau ștergerile în grupuri de trei nucleotide pot duce la inserarea sau ștergerea unuia sau mai multor aminoacizi și nu pot provoca efecte semnificative asupra funcționalității proteinei rezultate. Cu toate acestea, mutațiile frameshift, cauzate de inserțiile sau ștergerile unui număr de nucleotide care nu sunt un multiplu de trei sunt extrem de problematice, deoarece rezultă o schimbare în cadrul de citire (Figura 1). Deoarece ribozomii citesc ARNm în codonii tripleți, mutațiile frameshift pot schimba fiecare aminoacid după punctul mutației., Noul cadru de citire poate include, de asemenea, un codon de oprire înainte de sfârșitul secvenței de codificare. În consecință, proteinele obținute din gene care conțin mutații frameshift sunt aproape întotdeauna nefuncționale.
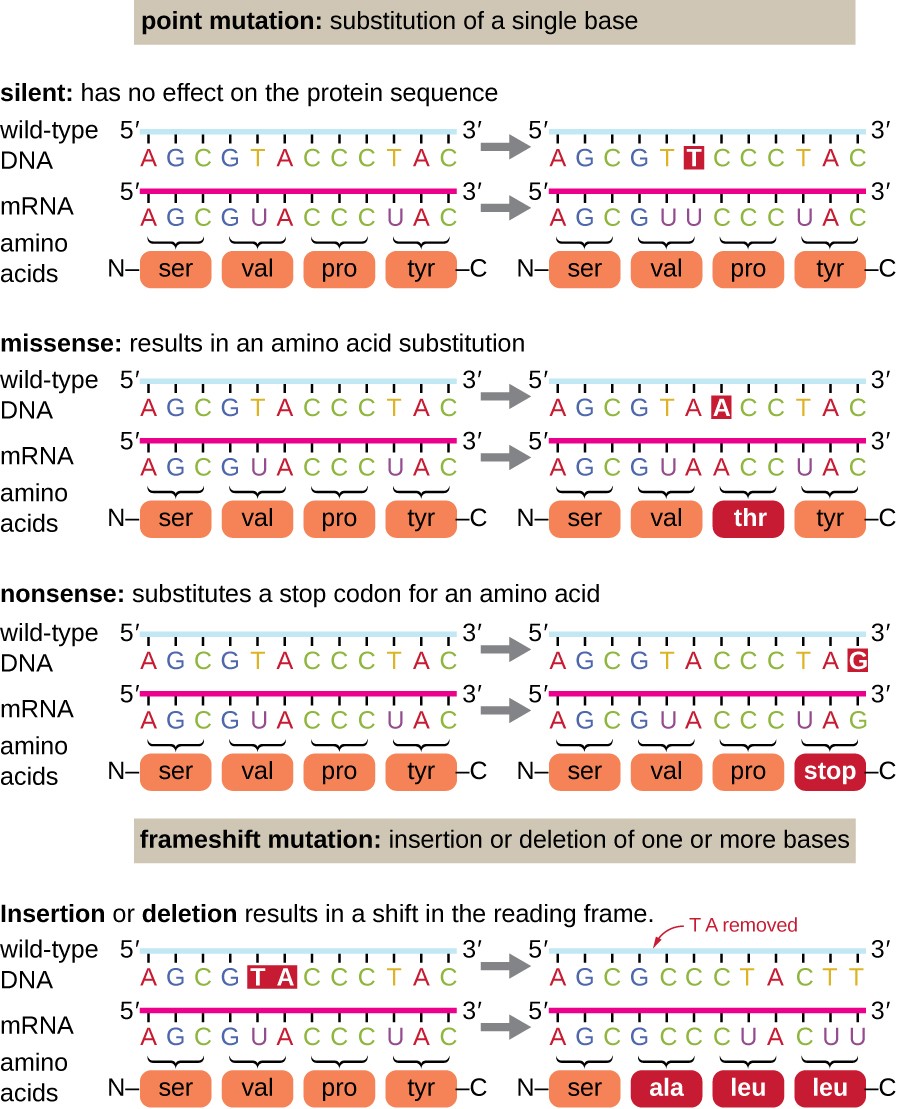
Figura 1. Faceți clic pentru o imagine mai mare. Mutațiile pot duce la modificări ale secvenței proteice codificate de ADN.
gândiți-vă
- care sunt motivele pentru care o modificare nucleotidică a unei gene pentru o proteină ar putea să nu aibă niciun efect asupra fenotipului acelei gene?,
- este posibil ca o inserție a trei nucleotide împreună după a cincea nucleotidă într-o genă care codifică proteinele să producă o proteină mai scurtă decât în mod normal? Cum sau cum nu?
o mutație benefică
deoarece primul caz de infecție cu virusul imunodeficienței umane (HIV) a fost raportat în 1981, aproape 40 de milioane de oameni au murit din cauza infecției cu HIV, virusul care provoacă sindromul imunodeficienței dobândite (SIDA)., Virusul vizează celulele T helper care joacă un rol-cheie în reducerea răspunsului imun înnăscut și adaptiv, infectând și ucigând celulele implicate în mod normal în răspunsul organismului la infecție. Nu există nici un remediu pentru infecția cu HIV, dar multe medicamente au fost dezvoltate pentru a încetini sau bloca progresia virusului. Deși indivizii din întreaga lume ar putea fi infectate, cea mai mare prevalență în rândul persoanelor de 15-49 ani este în Africa sub-Sahariană, unde aproape o persoană din 20 este infectat, reprezentând mai mult de 70% din infecții la nivel mondial (Figura 2)., Din păcate, aceasta este, de asemenea, o parte a lumii în care strategiile de prevenire și medicamentele pentru tratarea infecției lipsesc cel mai mult.

Figura 2. HIV este foarte răspândit în Africa Subsahariană, dar prevalența sa este destul de scăzută în alte părți ale lumii.în ultimii ani, interesul științific a fost stârnit de descoperirea câtorva persoane din Europa de Nord care sunt rezistente la infecția cu HIV. În 1998, geneticianul american Stephen J., O ‘ Brien de la National Institutes of Health (NIH) si colegii sai au publicat rezultatele analizei genetice a mai mult de 4.000 de persoane. Acestea au indicat că mulți indivizi de origine Eurasiatică (până la 14% în unele grupuri etnice) au o mutație de ștergere, numită CCR5-delta 32, în gena care codifică CCR5. CCR5 este un coreceptor găsit pe suprafața celulelor T care este necesar pentru ca multe tulpini ale virusului să intre în celula gazdă. Mutația duce la producerea unui receptor la care HIV nu se poate lega eficient și astfel blochează intrarea virală., Oamenii homozigoți pentru această mutație au redus foarte mult susceptibilitatea la infecția cu HIV, iar cei care sunt heterozigoți au o anumită protecție împotriva infecției.nu este clar de ce oamenii de origine nord-europeană, în special, poartă această mutație, dar prevalența ei pare să fie cea mai mare în Europa de Nord și scade constant în populații pe măsură ce se mișcă spre sud. Cercetările indică faptul că mutația a fost prezentă înainte de apariția HIV și este posibil să fi fost selectată la populațiile europene ca urmare a expunerii la ciumă sau variolă., Această mutație poate proteja indivizii de ciumă (cauzată de bacteria Yersinia pestis) și variolă (cauzată de virusul variola), deoarece acest receptor poate fi implicat și în aceste boli. Vârsta acestei mutații este o chestiune de dezbatere, dar estimările sugerează că a apărut între 1875 ani și 225 ani în urmă și ar fi putut fi răspândită din nordul Europei prin invazii vikinge.această descoperire interesantă a dus la noi căi în cercetarea HIV, inclusiv căutarea de medicamente care să blocheze legarea CCR5 la HIV la persoanele care nu au mutația., Deși testarea ADN pentru a determina care indivizi poartă mutația CCR5-delta 32 este posibilă, există cazuri documentate de indivizi homozigoți pentru mutația contractantă HIV. Din acest motiv, Testarea ADN pentru mutație nu este recomandată pe scară largă de către oficialii din domeniul sănătății publice, pentru a nu încuraja comportamentul riscant la cei care poartă mutația. Cu toate acestea, inhibarea legării HIV la CCR5 continuă să fie o strategie valabilă pentru dezvoltarea terapiilor medicamentoase pentru cei infectați cu HIV.,
cauzele mutațiilor
greșelile în procesul de replicare a ADN-ului pot determina apariția mutațiilor spontane. Rata de eroare a ADN polimerazei este o bază incorectă per miliard de perechi de baze replicate. Expunerea la mutageni poate provoca mutații induse, care sunt diferite tipuri de agenți chimici sau radiații (Tabelul 1). Expunerea la un mutagen poate crește rata mutației de peste 1000 de ori. Mutagenii sunt adesea și cancerigeni, agenți care provoacă cancer. Cu toate acestea, în timp ce aproape toți agenții cancerigeni sunt mutageni, nu toți mutagenii sunt în mod necesar cancerigeni.,
| Tabelul 1., to AT base pair | Point | |||
|---|---|---|---|---|
| Intercalating agents | ||||
| Acridine orange, ethidium bromide, polycyclic aromatic hydrocarbons | Distorts double helix, creates unusual spacing between nucleotides | Introduces small deletions and insertions | Frameshift | |
| Ionizing radiation | ||||
| X-rays, γ-rays | Forms hydroxyl radicals | Causes single- and double-strand DNA breaks | Repair mechanisms may introduce mutations | |
| X-rays, γ-rays | Modifies bases (e.,g., deaminating C a U) | Convertește GC de LA baza pereche | Punct | |
| Nonionizing | ||||
| Ultraviolete | Forme de pirimidină (de obicei, timină) dimerilor | Provoacă erori de replicare a ADN-ului | Frameshift sau punct | |
Mutageni Chimici
Diferite tipuri de substanțe chimice mutagene de a interacționa direct cu ADN-ul, fie acționând ca analogi nucleozidici sau prin modificarea de baze azotate., Substanțele chimice numite analogi nucleozidici sunt similare structural cu bazele nucleotidice normale și pot fi încorporate în ADN în timpul replicării (Figura 3). Acești analogi de bază induc mutații deoarece au adesea reguli diferite de împerechere a bazei decât bazele pe care le înlocuiesc. Alte mutagene chimice pot modifica bazele ADN normale, rezultând reguli diferite de împerechere a bazei. De exemplu, acidul azotic deaminează citozina, transformând-o în uracil. Uracilul se împerechează apoi cu adenina într-o rundă ulterioară de replicare, rezultând conversia unei perechi de baze GC într-o pereche de baze AT., Acidul azotic deaminează, de asemenea, adenina la hipoxantină, care se împerechează cu citozină în loc de timină, rezultând conversia unei perechi de bază TA într-o pereche de bază CG.

Figura 3. Faceți clic pentru o imagine mai mare. (a) 2-aminopurine nucleozidici (2AP) din punct de vedere structural este un analog nucleozidic de adenină nucleozidici, întrucât 5-bromouracil (5BU) este un analog nucleozidic cu timină nucleozidici. 2AP perechi de baze cu C, convertind o pereche de baze AT la o pereche de baze GC după mai multe runde de replicare., 5BU perechi cu G, convertind o pereche de bază AT la o pereche de bază GC după mai multe runde de replicare. (B) acidul azotic este un alt tip de mutagen chimic care modifică bazele nucleozidice deja existente, cum ar fi C, pentru a produce U, care perechi de baze cu A. Această modificare chimică, așa cum se arată aici, are ca rezultat transformarea unei perechi de baze CG într-o pereche de baze TA.mutagenii chimici cunoscuți ca agenți de intercalare funcționează diferit., Aceste molecule alunecă între bazele azotate stivuite ale helixului dublu al ADN-ului, distorsionând molecula și creând distanțe atipice între perechile de baze nucleotidice (Figura 4). Ca urmare, în timpul replicării ADN-ului, ADN polimeraza poate sări peste replicarea mai multor nucleotide (creând o ștergere) sau poate introduce nucleotide suplimentare (creând o inserție). Oricare dintre rezultate poate duce la o mutație frameshift. Produsele de ardere precum hidrocarburile aromatice policiclice sunt agenți de intercalare deosebit de periculoși care pot duce la cancere cauzate de mutații., Agenții de intercalare bromură de etidiu și acridină portocalie sunt frecvent utilizați în laborator pentru a colora ADN-ul pentru vizualizare și sunt potențiali mutageni.

Figura 4. Agenții de intercalare, cum ar fi acridina, introduc spațierea atipică între perechile de baze, rezultând ADN polimeraza introducând fie o deleție, fie o inserție, ducând la o potențială mutație de schimbare a cadrelor.expunerea la radiații ionizante sau neionizante poate induce mutații în ADN, deși prin mecanisme diferite., Radiațiile ionizante puternice, cum ar fi razele X și razele gamma, pot provoca rupturi monocatenare și duble în coloana vertebrală a ADN-ului prin formarea radicalilor hidroxil la expunerea la radiații (Figura 5). Radiațiile ionizante pot modifica, de asemenea, bazele; de exemplu, dezaminarea citozinei la uracil, analogă acțiunii acidului azotic. Expunerea la radiații ionizante este utilizată pentru a ucide microbii pentru a steriliza dispozitivele medicale și alimentele, datorită efectului său dramatic nespecific în deteriorarea ADN-ului, a proteinelor și a altor componente celulare (vezi Utilizarea metodelor fizice pentru controlul microorganismelor).,radiațiile neionizante, cum ar fi lumina ultravioletă, nu sunt suficient de energice pentru a iniția aceste tipuri de modificări chimice. Cu toate acestea, radiațiile neionizante pot induce formarea dimerilor între două baze pirimidinice adiacente, de obicei două timine, într-o catenă nucleotidică. În timpul formării dimerului timinei, cele două timine adiacente devin legate covalent și, dacă sunt lăsate nereparate, atât replicarea ADN-ului, cât și transcripția sunt blocate în acest moment. ADN polimeraza poate continua și reproduce dimerul incorect, ceea ce poate duce la mutații de schimbare a cadrelor sau a punctelor.,

Figura 5. (a) radiația ionizantă poate duce la formarea de rupturi monocatenare și dublu catenare în coloana vertebrală zahăr-fosfat a ADN-ului, precum și la modificarea bazelor (nu este prezentată). (b) radiații neionizante ca lumina ultravioleta poate duce la formarea de dimeri timină, care poate bloca replicarea și transcrierea și să introducă frameshift sau mutații punctuale.
gândiți-vă
- cum introduce un analog de bază o mutație?,
- cum introduce un agent intercalant o mutație?
- ce tip de mutagen provoacă dimeri de timină?procesul de replicare a ADN-ului este foarte precis, dar greșelile pot apărea spontan sau pot fi induse de mutageni. Greșelile necorectate pot duce la consecințe grave asupra fenotipului. Celulele au dezvoltat mai multe mecanisme de reparare pentru a minimiza numărul de mutații care persistă.,majoritatea greșelilor introduse în timpul replicării ADN sunt corectate prompt de majoritatea polimerazelor ADN printr-o funcție numită corectură. În corectură, ADN polimeraza citește baza nou adăugată, asigurându-se că este complementară bazei corespunzătoare din firul șablonului înainte de a adăuga următoarea. Dacă a fost adăugată o bază incorectă, enzima face o tăietură pentru a elibera nucleotida greșită și se adaugă o nouă bază.,
repararea nepotrivirii
unele erori introduse în timpul replicării sunt corectate la scurt timp după mutarea echipamentului de replicare. Acest mecanism se numește reparație nepotrivire. Enzimele implicate în acest mecanism recunosc nucleotida adăugată incorect, o accizează și o înlocuiesc cu baza corectă. Un exemplu este repararea nepotrivirii direcționate de metil în E. coli. ADN-ul este hemimetilat. Aceasta înseamnă că firul parental este metilat, în timp ce firul fiicei nou sintetizat nu este. Este nevoie de câteva minute înainte ca noul fir să fie metilat., Proteinele MutS, MutL și MutH se leagă de locul hemimetilat unde se găsește nucleotida incorectă. MutH taie firul nemetilat (noul fir). O exonuclează o porțiune din catenă (inclusiv nucleotida incorectă). Decalajul format este apoi completat de ADN pol III și ligază.deoarece producția de dimeri de timină este frecventă (multe organisme nu pot evita lumina ultravioletă), mecanismele au evoluat pentru a repara aceste leziuni., În repararea exciziei nucleotidelor (numită și reparație întunecată), enzimele elimină dimerul pirimidinic și îl înlocuiesc cu nucleotidele corecte (Figura 6). În E. coli, ADN-ul este scanat de un complex enzimatic. Dacă se constată o distorsiune în spirala dublă care a fost introdusă de dimerul pirimidinic, complexul enzimatic taie coloana vertebrală zahăr-fosfat mai multe baze în amonte și în aval de dimer, iar segmentul ADN între aceste două tăieturi este apoi îndepărtat enzimatic. ADN pol i înlocuiește nucleotidele lipsă cu cele corecte, iar ligaza ADN sigilează golul din coloana vertebrală a fosfatului de zahăr.,repararea directă (numită și repararea luminii) a dimerilor de timină are loc prin procesul de fotoreactivare în prezența luminii vizibile. O enzimă numită fotoliază recunoaște distorsiunea în helixul ADN cauzată de dimerul timinei și se leagă de dimer. Apoi, în prezența luminii vizibile, care photolyase enzimei de modificări de conformație și rupe în afară timină dimer, care să permită thymines din nou corect pereche de bază cu adenines pe complementar strand., Fotoreactivarea pare să fie prezentă în toate organismele, cu excepția mamiferelor placentare, inclusiv a oamenilor. Fotoreactivarea este deosebit de importantă pentru organismele expuse cronic la radiațiile ultraviolete, cum ar fi plantele, bacteriile fotosintetice, algele și coralii, pentru a preveni acumularea de mutații cauzate de formarea dimerului de timină.

Figura 6. Faceți clic pentru o imagine mai mare. Bacteriile au două mecanisme pentru repararea dimerilor de timină., (a) în repararea exciziei nucleotidelor, un complex enzimatic recunoaște distorsiunea complexului ADN din jurul dimerului timinei și taie și îndepărtează catena ADN deteriorată. Nucleotidele corecte sunt înlocuite cu ADN pol i, iar Catena nucleotidică este sigilată de ligaza ADN. (b) În photoreactivation, enzima photolyase se leagă de timină dimer și, în prezența luminii vizibile, se desface dimerul, restaurarea bazei de asociere a thymines complementare adenines pe partea opusă strand ADN-ului.,
gândiți-vă la asta
- În timpul reparației nepotrivirii, cum recunoaște enzima care este noua și care este vechea componentă?
- cum introduce un agent intercalant o mutație?
- ce tip de mutație Repară fotoliaza?
identificarea mutanților bacterieni
o tehnică comună utilizată pentru identificarea mutanților bacterieni se numește placare replică., Această tehnică este utilizată pentru a detecta nutritive mutanți, numit auxotrophs, care au o mutație într-o genă codifică o enzimă în biosinteza cale de un anumit nutrient, cum ar fi un aminoacid. Ca rezultat, în timp ce celulele de tip sălbatic păstrează capacitatea de a crește în mod normal pe un mediu lipsit de nutrienți specifici, auxotrofele nu sunt în măsură să crească pe un astfel de mediu. În timpul placării replicilor (Figura 7), o populație de celule bacteriene este mutagenizată și apoi placată ca celule individuale pe o placă completă nutrițional complexă și lăsată să crească în colonii., Celulele din aceste colonii sunt îndepărtate de pe această placă principală, adesea folosind catifea sterilă. Această catifea, care conține celule, este apoi presată în aceeași orientare pe plăci de diferite medii. Cel puțin o placă trebuie, de asemenea, să fie completă din punct de vedere nutrițional pentru a se asigura că celulele sunt transferate corespunzător între plăci. Celelalte plăci nu au nutrienți specifici, permițând cercetătorului să descopere diferiți mutanți auxotrofici incapabili să producă nutrienți specifici. Celulele din colonia corespunzătoare de pe placa completă nutrițional pot fi folosite pentru a recupera mutantul pentru studii ulterioare.,

Figura 7. Identificarea mutanților auxotrofici, cum ar fi auxotrofele histidinei, se face folosind placarea replică. După mutageneză, coloniile care cresc pe mediu complet nutrițional, dar nu pe mediu lipsit de histidină sunt identificate ca auxotrofe de histidină.
gândiți-vă
- De ce sunt celulele placate pe o placă completă din punct de vedere nutrițional, pe lângă plăcile cu deficit de nutrienți atunci când căutați un mutant?,
testul Ames
testul Ames, dezvoltat de Bruce Ames (1928–) în anii 1970, este o metodă care folosește bacteriile pentru screeningul rapid și ieftin al potențialului carcinogen al noilor compuși chimici. Testul măsoară rata de mutație asociată cu expunerea la compus, care, dacă este ridicată, poate indica faptul că expunerea la acest compus este asociată cu un risc mai mare de cancer., Testul Ames folosește ca organism de testare o tulpină de Salmonella typhimurium care este un auxotroph de histidină, incapabil să-și sintetizeze propria histidină din cauza unei mutații într-o genă esențială necesară sintezei sale. După expunerea la un potențial mutagen, aceste bacterii sunt placate pe un mediu lipsit de histidină, iar numărul de mutanți recapătă capacitatea de a sintetiza histidină este înregistrată și în comparație cu numărul de astfel de mutante care apar în absența potențialului mutagen (Figura 8)., Chimicalele care sunt mai mutagene vor aduce mai mulți mutanți cu sinteza histidinei restaurată în testul Ames. Deoarece multe substanțe chimice nu sunt direct mutagene, ci sunt metabolizate în forme mutagene de enzimele hepatice, extractul de ficat de șobolan este inclus în mod obișnuit la începutul acestui experiment pentru a imita metabolismul hepatic. După efectuarea testului Ames, compușii identificați ca mutageni sunt testați în continuare pentru proprietățile lor potențiale cancerigene prin utilizarea altor modele, inclusiv modele animale, cum ar fi șoarecii și șobolanii.
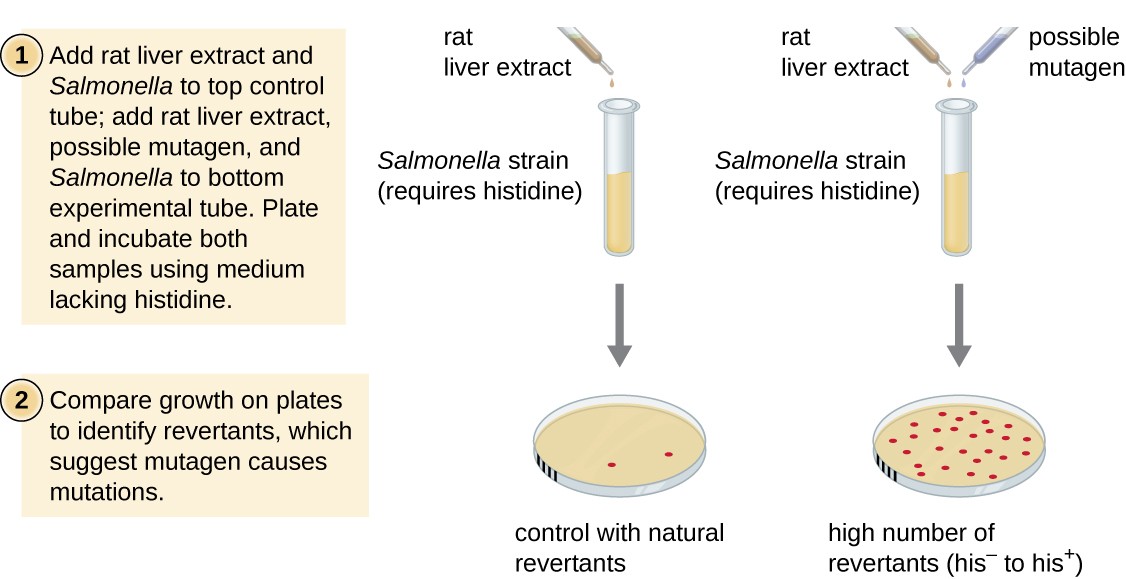
Figura 8., Testul Ames este utilizat pentru a identifica substanțele chimice mutagene, potențial cancerigene. O Salmonella histidină auxotroph este utilizat ca tulpina de testare, expuse la un potențial mutagen / cancerigen. Numărul de mutanți de reversiune capabili să crească în absența histidinei furnizate este numărat și comparat cu numărul de mutanți naturali de reversiune care apar în absența mutagenului potențial.
gândiți-vă
- ce mutație este utilizată ca indicator al ratei de mutație în testul Ames?
- De ce testul Ames poate funcționa ca un test pentru carcinogenitate?,
concepte cheie și rezumat
- o mutație este o schimbare ereditară în ADN. O mutație poate duce la o modificare a secvenței de aminoacizi a unei proteine, posibil afectând funcția acesteia.
- o mutație punct afectează o singură pereche de bază. O mutație punctuală poate provoca o mutație silențioasă dacă codonul ARNm codifică același aminoacid, o mutație missense dacă codonul ARNm codifică un aminoacid diferit sau o mutație nonsens dacă codonul ARNm devine un codon stop.,
- mutațiile Missense pot păstra funcția, în funcție de chimia noului aminoacid și localizarea acestuia în proteină. Mutațiile nonsens produc proteine trunchiate și frecvent nefuncționale.
- o mutație frameshift rezultă dintr-o inserție sau ștergere a unui număr de nucleotide care nu este un multiplu de trei. Modificarea cadrului de citire modifică fiecare aminoacid după punctul mutației și are ca rezultat o proteină nefuncțională.
- mutațiile spontane apar prin erori de replicare a ADN-ului, în timp ce mutațiile induse apar prin expunerea la un mutagen.,agenții mutageni sunt frecvent carcinogeni, dar nu întotdeauna. Cu toate acestea, aproape toți agenții cancerigeni sunt mutageni.
- Mutagenii chimici includ analogi de bază și substanțe chimice care modifică bazele existente. În ambele cazuri, mutațiile sunt introduse după mai multe runde de replicare a ADN-ului.
- radiațiile ionizante, cum ar fi razele X și razele γ, conduc la ruperea coloanei vertebrale fosfodiesterice a ADN-ului și, de asemenea, pot modifica chimic bazele pentru a modifica regulile de împerechere a bazei.,
- Nonionizing ca lumina ultravioleta poate introduce pirimidinice (timina) dimeri, care, în timpul ADN de replicare și transcriere, poate introduce frameshift sau mutații punctiforme.
- celulele au mecanisme pentru a repara mutațiile care apar în mod natural. ADN polimeraza are activitate de corectură. Repararea nepotrivirii este un proces de reparare a bazelor încorporate incorect după ce replicarea ADN-ului a fost finalizată.dimerii de pirimidină pot fi, de asemenea, reparați., În repararea exciziei nucleotidelor (repararea întunecată), enzimele recunosc distorsiunea introdusă de dimerul pirimidinei și înlocuiesc firul deteriorat cu bazele corecte, folosind ca șablon firul ADN nedeteriorat. Bacteriile și alte organisme pot utiliza, de asemenea, reparații directe, în care enzima fotoliazei, în prezența luminii vizibile, rupe pirimidinele.
- prin compararea creșterii pe placa completă și lipsa creșterii pe medii lipsite de nutrienți specifici, pot fi identificați mutanți specifici de pierdere a funcției numiți auxotrofe.,
- testul Ames este o metodă ieftină care utilizează bacterii auxotrofice pentru a măsura Mutagenitatea unui compus chimic. Mutagenitatea este un indicator al potențialului carcinogen.
alegere multiplă
care dintre următoarele este o modificare a secvenței care duce la formarea unui codon stop?
- mutatie missense
- mutație nonsens
- tăcut mutație
- eliminarea mutație
Arată Răspunsulcompletați martorul
un mutagen chimic care este similar structural cu o nucleotidă, dar are reguli diferite de împerechere a bazei se numește ________.,
Arată Răspunsulenzima utilizată în repararea luminii pentru a împărți dimerii timinei se numește________.
Arată Răspunsulfenotipul unui organism care este cel mai frecvent observat în natură se numește ________.,
Arată RăspunsulTrue/False
carcinogenii sunt de obicei mutagene.
Arată RăspunsulCred că despre Asta
Ce este mult mai probabil ca inserții sau deleții va fi mai dăunătoare pentru o celulă decât mutații punctiforme?,de ce credeți că testul Ames este preferabil utilizării modelelor animale pentru a analiza compușii chimici pentru mutagenitate?
gândirea critică
mai jos sunt câteva secvențe de ADN care sunt mutate în comparație cu secvența de tip sălbatic: 3′-T A C T G A C T G A C G A T C C-5′. Imaginați-vă că fiecare este o secțiune a unei molecule de ADN care s-a separat în pregătirea transcrierii, așa că vedeți doar firul șablonului., Construi secvențe ADN complementare (indicând 5′ și 3′ capete) pentru fiecare secvență de ADN-ul mutant, apoi transcrie (indicând 5′ și 3′ capete) modelul fire, și traduce arnm molecule folosind codul genetic, înregistrând rezultate secvență de aminoacizi (indicând N și C termini). Ce tip de mutație este fiecare?,>
Mutații ADN Șablon Strand #3: 3′-T O C T G C T a G C T O T C-5′ ADN Complementare secvența:
secvență de arnm transcris din șablon:
secvență de Aminoacizi al peptidelor:
Tip de mutație:
Mutații ADN Șablon Strand #4: 3′-T O C G C T a G C T O T C-5′ Complementare secvența ADN:
secvență de arnm transcris din șablon:
secvență de Aminoacizi din peptide:
Tip de mutație: