Cyclohexen Chemische Eigenschaften, Verwendungen, Produktion
Chemische Eigenschaften
Cyclohexen(C6H10, CAS-Register-Nr. Es ist in Wasser unlöslich. Inhalation von hohen Konzentrationen kann eine narkotische Wirkung haben. Cyclohexen ist leicht entflammbar und sollte daher von Hitze und offener Flamme ferngehalten werden. Es kann bei der Lagerung Peroxide bilden, daher sollte es in Abwesenheit von Luft gelagert werden. Es kann toxische Wirkungen verursachen, wenn es eingeatmet oder durch die Haut absorbiert wird., Einatmen oder Kontakt mit Material kann Haut und Augen reizen oder verbrennen. Feuer erzeugt reizende, ätzende und / oder giftige Gase.
Cycloolefin
Cyclohexen ist ein zyklisches Olefin und eine farblose, brennbare Flüssigkeit mit einem speziellen stechenden Geruch bei Raumtemperatur. Langfristige Platzierung in der Luft Es kann durch Luft zu Peroxid oxidiert werden. Natürlich vorhanden in Kohlenteer, löslich in Aceton, Tetrachlorkohlenstoff, Benzol, Ether, Hexan, Ethanol und anderen organischen Lösungsmitteln, kann binäres Azeotrop mit niedrigeren Alkoholen, Essigsäure usw. bilden., Cyclohexen hat die allgemeine Natur von Olefin, zersetzt sich schnell in Gegenwart von Uransalzen unter Sonnenlicht oder ultravioletten Strahlen, ist konstant wie in einem versiegelten Rohr bei 200 ℃ für eine lange Zeit erhitzt wird, bildet Benzol und Naphthalin bei 400~500 ℃.
Es wird durch Dehydrierung von Cyclohexanol bei hoher Temperatur in Gegenwart eines Säurekatalysators in der Industrie erhalten. Es wird durch sulfatierte Dehydratation von Cyclohexanol im Labor erhalten.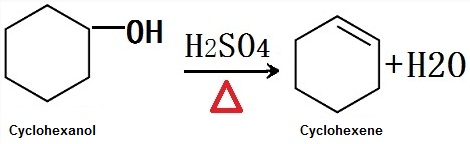
Abbildung 1 ist die chemische Reaktionsgleichung der sulfatierten Dehydratation von Cyclohexanol, um Cyclohexen zu erhalten.,
Cyclohexen ist ein wichtiger chemischer Rohstoff, der für die Herstellung von Adipinsäure, Adipinaldehyd, Maleinsäure, Cyclohexansäure, Cyclohexanaldehyd, Maleinsäure, Cyclohexylcarbonsäure, Cyclohexanecarboaldehyd in der Industrie verwendet wird. Es wird auch als Extraktionsmittel verwendet, wobei der Stabilisator ein Benzin mit hoher Oktanzahl aufweist. Inhalation kann leichte Vergiftungen verursachen.
Hier sind einige dieser wichtigen Verbindungen hergestellt durch Cyclohexen, (1)chloriertes Cyclohexan hergestellt wird, nützlich als pharmazeutische Zwischenprodukte, ein Lösungsmittel und Gummizusätze., (2) Cyclohexanon wird aus Cyclohexen hergestellt und kann als Zwischenprodukte für Arzneimittel, Pestizide, Parfums und Farbstoffe sowie als Polymermodifikatoren verwendet werden. (3) Cyclohexylacetat wird hergestellt und als Kunststofflösungsmittel verwendet. (4) cyclohexanon Phenol wird hergestellt, kann als Rohstoffe Medizin und Pestizide verwendet werden. (5) Aminocyclohexanol wird hergestellt, kann als Tenside und Emulgatoren verwendet werden. (6) Das Produkt kann auch direkt als organische Zwischenprodukte, Lösungsmittel und Zusatzstoffe verwendet werden, wenn Gewürze hergestellt werden. Es kann bei der Herstellung von Butadien im Labor verwendet werden.,
Die oben genannten Informationen wurden bearbeitet und zusammengestellt von Yan Yanyong von Chemicalbook.
Zubereitung
Cyclohexen kann auf verschiedene Arten synthetisiert werden, z. B. Dehydrierung von Cyclohexan, Dehydrierung von Cyclohexanol, Dehydrohalogenierung von halogeniertem Cyclohexan, chemische Reduktion oder teilweise Hydrierung von Benzol. Verglichen mit anderen Methoden ist die Technologie der Teilhydrierung von Benzol zu Cyclohexen von Vorteil der Sicherheit, der hohen Atomökonomie und der Umweltfreundlichkeit. Die Teilhydrierung von Benzol zu Cyclohexen ist seit mehr als 100 Jahren bekannt.,
Chemische Eigenschaften
Farblose brennbare Flüssigkeit. Unlöslich in Wasser, löslich in äther.
Selektive Oxidation
Cyclohexen kann mit starken Oxidationsmitteln stark reagieren., Obwohl es in seiner chemischen Struktur einfach ist, gibt es zwei potentielle Oxidationsstellen in Cyclohexen, und die üblichen Oxidationsreaktionen führen im Allgemeinen zu einer Mischung von Produkten mit unterschiedlichen Oxidationszuständen und funktionellen Gruppen: Die Oxidation der C=C-Bindung (Site a) kann zu 7-Oxabicycloheptan, trans/cis-Cyclohexan-1,2-diol oder Adipinsäure führen; Oxidation an der Allyl-C-H-Position (Site b) kann Cyclohex-2-en-1-ol oder Cyclohex-2-en-1-one erzeugen., Diese Produkte sind nützliche industrielle Zwischenprodukte, die in der organischen Synthese, medizinischen Chemie, Pestizidchemie, Materialwissenschaft usw. weit verbreitet sind. Daher sind steuerbare Oxidationsreaktionen für Cyclohexen, die sich die Zielprodukte selektiv leisten können, synthetisch wertvoll für Anwendungen sowohl in der Industrie als auch in der Industrie und werden so zum Ziel synthetischer und katalytischer Chemiker auf dem Gebiet.
Verwendet
- In der organischen Synthese wird es auch als Lösungsmittel verwendet.,
- Cyclohexen wird als organische synthetische Rohstoffe verwendet, wie synthetische Rohstoffe für Lysin, Cyclohexanon, Phenol, Polycycloolefinharz, chloriertes Cyclohexan, Kautschukadditive, Cyclohexanol usw. Es wird auch als Katalysatorlösungsmittel und Erdölextraktionsmittel, Benzinstabilisator mit hoher Oktanzahl verwendet.
- Cyclohexen wird zur Herstellung von Adipinsäure, Maleinsäure, Hexahydrobenzoesäure und Acetaldehyd, Herstellung von Butadien im Labor verwendet. Es wird als Benzinstabilisator mit hoher Oktanzahl verwendet.,
Herstellungsverfahren
Cyclohexanol wird erhitzt, um Cyclohexen in Gegenwart von Schwefelsäurekatalysator zu erzeugen, destilliert, um Rohprodukte zu erhalten. Gewaschen mit einer feinen gesättigten Salzlösung, dann wird Natriumsulfatlösung verwendet, um Spuren von Säure zu neutralisieren, dann mit Wasser gewaschen, geschichtet, getrocknet, Filtration, Destillation, Sammeln von 82-85 ℃ Destillatprodukten, um Cyclohexen zu erhalten.
Entflammbarkeit hazard characteristics
Im Brandfall, hohe Temperatur, Oxidationsmittel, es ist brennbar, Brennen erzeugt reizenden Rauch.,
Lagereigenschaften
– Belüftung Tieftemperaturtrocknung, getrennt von Oxidationsmitteln und Säuren gelagert. Nicht lange lagerung zu verhindern polymerisation.
Chemische Eigenschaften
Cyclohexen ist eine farblose Flüssigkeit (Cyclicalken) mit einem süßlichen Geruch.
Physikalische Eigenschaften
Klare, farblose Flüssigkeit mit süßem Geruch. Die Geruchsschwellenkonzentration beträgt 0,18 ppm (zitiert,Amoore und Hautala, 1983).
Verwendet
Es kommt in Kohlenteer vor und wird durch katalytische Hydratation von Cyclohexanol und Dehydrierung von Cyclohexan erhalten., Cyclohexen wird bei der Herstellung von Adipinsäure, Maleinsäure und Butadien verwendet.in der Ölgewinnung; als Stabilisator für Benzin mit hoher Oktanzahl; und in der Biosynthese.
Verwendet
Alkylierungskomponente. Bei der Herstellung von Adipinsäure, Maleinsäure, Hexahydrobenzoesäure und Aldehyd. Zur Herstellung von Butadien im Labor. Wurde für die Synthese von Maleinsäure und als Stabilisator für Benzin mit hoher Oktanzahl vorgeschlagen.,
Verwendung
Herstellung von Adipinsäure, Maleinsäure, Hexahydrobenzoesäure und Aldehyd; Stabilisator für Benzin mit hoher Oktanzahl
Herstellungsverfahren
Cyclohexen wird durch Dehydratation von Cyclohexanol durch thermische Reaktion eines Ethylen-Propylen–Butadien–Gemisches hergestellt(1).
Definition
ChEBI: Ein Cycloalken, das Cylohexan mit einer einzigen Doppelbindung ist.
Allgemeine Beschreibung
Eine farblose Flüssigkeit. Unlöslich in Wasser und weniger dicht als Wasser. Flammpunkt 20°F. Dämpfe schwerer als Luft. Inhalation von hohen Konzentrationen kann eine narkotische Wirkung haben. Verwendet, um andere Chemikalien zu machen.,
Luft & Wasserreaktionen
Leicht entflammbar. Unlöslich in Wasser.
Reaktivitätsprofil
Cyclohexen kann mit starken Oxidationsmitteln stark reagieren. Kann exotherm mit Reduktionsmitteln reagieren, um Wasserstoffgas freizusetzen. In Gegenwart verschiedener Katalysatoren (wie Säuren) oder Initiatoren können exotherme Additionspolymerisationsreaktionen auftreten. Oxidiert leicht in Luft, um instabile Peroxide zu bilden, die spontan explodieren können .
Gesundheitsgefahr
Es gibt sehr wenige toxikologische Daten availableon Cyclohexen., Inhalation Produziertirritation der Augen und Atemwege. Es ist auch ein Reizmittel für die Haut. Seine akute toxityist niedrig; die toxischen Wirkungen sind ähnlich denen von Cyclohexan. Exposition gegenüber hoher Konzentrationoder Einnahme kann Schläfrigkeit verursachen.Eine einmalige Exposition gegenüber 15.000 ppm Cyclohexenec könnte für Ratten tödlich sein.
Feuer-Gefahr
leichtentzündlich: Wird leicht entzündet, durch Hitze, Funken oder Flammen. Dämpfe können mit Luft explosive Gemische bilden. Dämpfe können zur Zündquelle gelangen und zurückblitzen. Die meisten Dämpfe sind schwerer als Luft., Sie breiten sich auf dem Boden aus und sammeln sich in niedrigen oder beengten Bereichen (Abwasserkanäle, Keller, Tanks). Dampfexplosionsgefahr drinnen, draußen oder in Abwasserkanälen. Abfluss in die Kanalisation kann Feuer-oder Explosionsgefahr verursachen. Behälter können beim Erhitzen explodieren. Viele Flüssigkeiten sind leichter als Wasser.
Sicherheitsprofil
Mäßig toxisch durch Einatmen und Verschlucken. Eine sehr gefährliche Brandgefahr bei Flammenexposition; kann mit Oxidationsmitteln reagieren. Gefährlich; von Hitze und offener Flamme fernhalten. Um Feuer zu bekämpfen, verwenden Sie Schaum, CO2, trockene Chemikalie.,
Potentielle Exposition
Kann als Zwischenprodukt bei der Herstellung anderer Chemikalien (z. B. Adipinsäure, Maleinsäure, Hex-Ahydro-Benzoesäure), bei der Ölextraktion und als Katalysator verwendet werden.
Karzinogenität
Cyclohexen war nicht mutagen in Salmonellatyphimurium mit oder ohne metabolicactivation.
Umwelt-Schicksal
Biologische. Cyclohexen biologisch abbaubar zu Cyclohexanon – (Dugan, 1972; Verschueren, 1983).
Photolytischen. Folgende Ratenkonstanten wurden für die Reaktion von Cyclohexen mit Ohradikalen in der Atmosphäre berichtet: 6,80 x 10-11 cm3 / Molekül?Sek (Atkinson et al., 1979), 6.,75 x 10-11cm3 / Molekül?sec bei 298 K (Sablji? und Güsten, 1990), 5.40 x 10-11 cm3/molecule?sec at 298 K (Rogers, 1989), 1.0 x 10-10 cm3/molecule?sec at 298 K (Atkinson, 1990); mit Ozon in der gasphase:1.69 x 10-16 cm3/molecule?sek bei 298 K (Japar et al., 1974), 2.0 x 10-16 bei 294 K (Adeniji etal., 1981), 1.04 x 10-16 cm3/Moleküle?Sek (Atkinson et al., 1983), 1.04 x 10-16 bei 298 K (Atkinsonand Carter, 1984); mit NO3 in die Atmosphäre: 5.26 x 10-13 cm3/molecule?trocken (Sablji? und Güsten, 1990); 5.3 x 10-13 cm3/molecule?sek bei 298 K (Atkinson, 1990) und 5,28 x 10-13 cm3/Molekül?,secat 295 K (Atkinson, 1991). Cox et al. (1980) berichtete eine Ratenkonstante von 6,2 x 10-11cm3 / Molekül?sec für die Reaktion von gasförmigem Cyclohexen mit OH-Radikalen basierend auf einem Wert von 8x 10-12 cm3 / Molekül?sec für die Reaktion von Ethylen mit FREIEN Radikalen.
Chemisch / physikalisch. Gasförmige Produkte, die aus der Reaktion von Cyclohexen mit Ozon gebildet wurden, waren (%Ausbeute): Ameisensäure , Kohlenmonoxid , Kohlendioxid, Ethylen und Glyceraldehyd (Hatakeyama et al., 1987). In einem Smogkammerexperiment in derdark bei 25 °C reagierte Cyclohexan mit Ozon., The following products and their respective molaryields were: oxalic acid (6.16%), malonic acid (6.88%), succinic acid (0.63%), glutaric acid(5.89%), adipic acid (2.20%), 4-hydroxybutanal (2.60%), hydroxypentanoic acid (1.02%),hydroxyglutaric acid (2.33%), hydroxyadipic acid (1.19%), 4-oxobutanoic acid (6.90%), 4-oxopentanoic acid (4.52%), 6-oxohexanoic acid (4.16%), 1,4-butandial (0.53%), 1,5-pentanedial(0.44%), 1,6-hexanedial (1.64%), and pentanal (17.05%).
Grosjean et al., (1996) investigated the atmospheric chemistry of cyclohexene with ozone and anozone-nitrogen oxide mixture under ambient conditions. The reaction of cyclohexene and ozone inthe dark yielded pentanal and cyclohexanone. The sunlight irradiation of cyclohexene with ozonenitrogenoxide yielded the following carbonyls: formaldehyde, acetaldehyde, acetone, propanal,butanal, pentanal, and a C4 carbonyl.
Cyclohexene reacts with chlorine dioxide in water forming 2-cyclohexen-1-one (Rav-Acha etal., 1987).
Shipping
UN2256 Cyclohexene, Hazard Class: 3; Labels:3-Flammable liquid.,
Reinigungsmethoden
Freies Cyclohexen aus Peroxiden durch Waschen mit aufeinanderfolgenden Portionen verdünntem angesäuertem Eisensulfat oder mit NaHSO3-Lösung, dann mit destilliertem Wasser, Trocknen mit CaCl2 oder CaSO4 und Destillieren unter N2. Alternative Methoden zur Entfernung von Peroxiden umfassen die Passage durch eine Aluminiumoxidsäule, das Rückfluxen mit Natriumdraht oder Kupferstearat (dann Destillieren aus Natrium). Das Dien wird durch Rückfluxen mit Maleinsäureanhydrid entfernt, bevor es unter Vakuum destilliert wird. Die Behandlung mit 0,1 Mol MeMgI in 40 ml Diethylether entfernt Spuren von sauerstoffhaltigen Verunreinigungen., Andere Reinigungsverfahren umfassen das Waschen mit wässrigem NaOH, das Trocknen und Destillieren unter N2 durch eine Spinnbandsäule, das erneute Destillieren von CaH2, das Lagern unter Natriumdraht und das Durchlaufen einer Aluminiumoxidsäule unter N2 unmittelbar vor dem Gebrauch. Lagern Sie es bei
Inkompatibilitäten
Dampf kann explosive Mischung mit Luft bilden. Die Substanz kann explosive Peroxide bilden. Der Untergrund kann unter bestimmten Bedingungen polymerisieren.Unverträglich mit Oxidationsmitteln (Chlorate, Nitrate, Peroxide, Permanganate, Perchlorate, Chlor, Brom,Fluor, etc.); Kontakt kann zu Bränden oder Explosionen führen., Halten Sie wegvon alkalischen Materialien, starken Basen, starken Säuren, Oxoa-Cids, Epoxiden.
Abfallentsorgung
Das Material mit einem brennbaren Lösungsmittel auflösen oder vermischen und in einer mit einem Nachbrenner und Wäscher ausgestatteten chemischen Verbrennungsanlage verbrennen. Alle Bundes -, Landes-und lokalen Umweltvorschriften müssen beachtet werden.