US Pharm. 2012;37(12):HS1-HS8.
abstrakt: som lægemiddeleksperter er farmaceuterskulle give passende vejledning til behandling af akutbakteriel peritonitis i hospitalsindstillingen. Akut bakterielperitonitis er forbundet med en høj risiko for dødelighed. Umiddelbarintervention er nødvendig, da forsinkelse kan tillade den engang lokaliserede sygdomproces at skade andre organer i hele kroppen. Egnetidentifikation og behandling af akut bakteriel peritonitis er nøgler til bedre resultater., Ud over kirurgisk indgreb, farmakologiskbehandling er også nødvendig. Behandling eller forebyggelse af hypovolemiassocieret med peritonitis kan udføres i henhold til anbefalingerne fra de overlevende Sepsis-Kampagneretningslinjer. Endelig, da antibiotikabehandling er den tredje hjørnesten i behandlingen, er det vigtigt atovervej passende udvælgelse, dosering og varighed af antibiotika.
Peritonitis er en akut inflammation af peritoneallining på grund af bakteriel infektion samt andre årsager såsom aschemicals, bestråling, og udenlandske legemsbeskadigelse.,1 fornærmelse af peritonealforingen af et af disse midler kan føre til en inflammatorisk respons, kendt som akut peritonitis.1 tabel 1 viser fælles patogen ætiologi af akut bakteriel peritonitis.
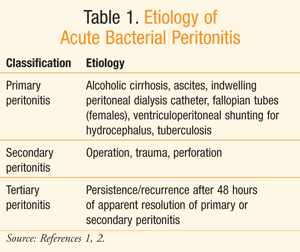
Dødelighed forbundet med peritonitis var around90% i begyndelsen af 1900-tallet. Disse priser er siden kommet ned toapproximately 30% ved anvendelse af passende medicinsk behandling andsupportive pleje.2
Sygdomsoversigt
klassificering af bakteriel peritonitis er baseret på kilden til de infektiøse bakterier.,2 primær eller spontan peritonitishenviser til en ekstraperitoneal etiologi, hvor den infektiøse bakterierindtast peritonealhulen gennem kredsløbs-eller lymfatiskesystemet.1,2 i disse tilfælde har patienten normalt en underliggende comorbiditet, der kan føre til bakteriel migration ind i bughinden.1sådanne comorbiditeter kan omfatte ascites og indbygget peritonealdialyse katetre. Primær peritonitis anslås at forekomme hos 10% til30% af patienterne med alkoholisk cirrose.,1 derudover har patienter i kronisk ambulant peritonealdialyse (CAPD) i gennemsnit en forekomst af peritonitis hver 33.måned.1
sekundær peritonitis, den mest almindelige ætiologi, er resultatet af infektiøse bakterier fra en kilde i peritoneum.1i betragtning af den overflod af mikroflora, der findes i mavenorganer, migration af bakterierne fra et hvilket som helst af organerne tilsteril peritoneum kan føre til en inflammatorisk respons, hvilket resulterer isekundær peritonitis. Spredning af bakterier fra deres værtsorganer kanresultatet af punktering på grund af traume, kirurgi eller perforering.,1 Ulceration, iskæmi eller obstruktion kan forårsage perforering af abdominale organer.1 endelig tertiær peritonitiser vedvarende eller tilbagevendende peritonitis, der vises igen mindst 48 timerefter tilsyneladende opløsning af en primær eller sekundær peritonitis.2 Data om forekomsten af sekundær og tertiær peritonitis er begrænsede.1 Klassificering af peritonitis er nyttig i klinisk praksis, da det kan hjælpe med at lette passende diagnose og behandling.,
klinisk præsentation og diagnose
bakteriel indføring i bughinden resulterer i en øjeblikkelig humoral og cellulær immunrespons.1denne reaktion udløser en inflammatorisk proces, hvilket resulterer i væskeskift i peritonealhulen. Denne væskeakkumulering sammen mednedsat tarmmotilitet fører ofte til abdominal afstand.Derudover væske forskydning i maven, kendt som tredje-afstand,kan resultere i nedsat blodvolumen, der fører til hypovolæmi i severecases., Feber, opkastning,og diarr.kan også ledsage peritonitis, blanding væske ubalancer og øge risikoen for hypovolæmi.Ubehandlet hypovolæmi kan resultere i nedsat hjerteproduktion og i sidste ende hypovolemisk chok.1
ud over flydende skift, fremmede stoffer, såsom asfeces og slim til stede i bughulen kan forværre peritonitisby svækkelse af immunforsvaret mekanismer såsom bakteriel fagocytose.1absorption af bakterier og endotoksiner i blodbanen lettes af en betændt peritoneum og kan resultere i sepsis., Døden kan skyldes negative virkninger på organsystemer som følge af alvorlige komplikationer såsom sepsis. Derudover, andre alvorlige komplikationer, såsom ashypoalbuminemia forårsaget af protein tab samt pulmonarycomplications som lungebetændelse som følge af diafragma hæmning dueto fiksering, kan forværre prognosen. Sammen med værten immunitet andtreatment tilstrækkelighed, mængden og virulens af inficere organismer ogkommissionens tilstedeværelsen af fremmede stoffer i bughulen har stor indflydelse på den resulterende resultatet af bughindebetændelse.,1
Den uspecifikke kliniske præsentation af primaryperitonitis varierer drastisk fra den iøjnefaldende præsentation ofsecondary peritonitis.1 i modsætning til sekundær peritonitis kan primærperitonitis udvikle sig over flere uger uden tegn på akutdistress. Selv om patienten kan klage abdominal ømhed,kvalme, opkastning eller diarré, primære peritonitis er normalt firstsuspected når-dialysatet vises overskyet i patienter undergoingperitoneal dialyse, eller når encephalopati forværres hos patienter withcirrhosis., Laboratoriefund efter mistanke om primærperitonitis kan vise mild forhøjelse af antallet af hvide blodlegemer (bcbc) og en positiv kultur af peritoneal dialysat eller asketisk væske.1
I modsætning til patienter med sekundær peritonitis oftenpresent med en boardlike maven, abdominal udspiling, svag bowelsounds, at aftage over tid, og ulidelig mavesmerter thatleads til ufrivillig guarding, med de små bevægelser som breathingor vuggende af sengen forårsager alvorlige smerter., Som tidligere nævnt kan hypovolemi forekomme i mangel af behandling, hvilket kan ultimattresultere i hypotension og chok. Andre tegn og symptomer omfattertachypnø, takykardi, kvalme og opkastning, nedsat urinproduktion ogforhøjet temperatur.1 ved sekundær peritonitis kan laboratorieundersøgelser vise leukocytose med dominerende neutrofiler og forhøjede bånd.1
behandling af Peritonitis
de ønskede resultater i peritonitis omfatter opløsning af den underliggende ætiologi og dræning af abscesser.,1sekundære mål for behandling omfatter eliminering af infektion ogbeskyttelse mod bivirkninger samt end-organskader, herunder AT til lungerne, lever, hjerte og nyrer.1elementer af passende intervention består af væskeoplivning, kildekontrolprocedure (kirurgi) og empirisk antimikrobiel terapi.3de fleste tilfælde af primær peritonitis kræver brug af antimikrobielleagenter som grundpille i terapi, og dræningsprocedurer er normaltikke påkrævet.1
sekundær peritonitis kræver kirurgisk behandling, kendt som kildekontrol, for at korrigere den underliggende patologi.,1 Sourcecontrol har til hensigt at korrigere anatomiske derangements, fjerne infectiousfoci og kontrollere de faktorer, der fremmer igangværende infektion.4Specific faktorer, der er tilbøjelige til hinder for, at en vellykket kilde controlinclude en forsinkelse på mere end 24 timer, før den nævnte procedure; en AcutePhysiology og Kroniske Evaluering (APACHE) score mindst 15;alder >70 år; tilstedeværelsen af komorbiditet; lav albumin niveau; poornutritional status; diffus peritonitis; og tilstedeværelse af malign.,3 mislykket kildekontrol indikeres ved tilbagevendende infektion på stedet, anastomotisk svigt eller fisteldannelse.3 perkutan, billedstyret dræning foretrækkes frem for kirurgisk dræning, især når infektionen er godt lokaliseret.1,3
hypovolemi i indstillingen af peritonitis kan føre tilorgansvigt. Uanset tilstedeværelsen af septisk shock er hurtig væskeoplivning derfor berettiget hos alle patienter med peritonitisfor at fremme fysiologisk stabilitet.,3 Mere aggressiverestoration af intravaskulære volumen bør gives til dem, withseptic stød og organsvigt i den måde, der er beskrevet i SurvivingSepsis Kampagne retningslinjer for håndtering af septisk shock.3 de 2012 opdateringer af retningslinjerne for overlevende Sepsis vil angiveligt angive, at den indledende væskeudfordring skal være mindst 1 L krystalloid og mindst 30 mL / kg i de første 4 til 6 timer. Inkrementel fluidbolus kan følge, så længe patientens vitale tegn fortsætter med at viseforbedring.,5 noradrenalin er den foretrukne vasopressor, og dobutamin inotropisk terapi kan tilsættes til patienter medhjertedysfunktion.5 kontinuerlig hydrocortisoninfusiontotaling 200 mg / 24 timer anbefales til dem medvasopressor-ildfast septisk shock. Feber, takypnø, kvalme ogopkastning og reduceret væskeindtag kan føre til dehydrering hos patientermed peritonitis.3
empirisk antibiotikabehandling bør påbegyndes ved mistanke om peritonitis.,3Practice retningslinjer fra Infectious Diseases Society of America(IDSA) anbefaler, at empiriske antimikrobiel terapi indledes inden forkildeni første time af anerkendelse af peritonitis hos patienter withcompromised hæmodynamisk eller organers funktion; ellers terapi bør beinitiated inden for 8 timer af præsentation.3 Selv om der erbegrænset værdi for blodkulturer i behandlingen af erhvervet peritonitis, er Gram-pletter til påvisning af tilstedeværelsen af gram-positiv cocciorgær berettiget hos personer med høj risiko såvel som hos dem medsundhedspleje-erhvervet peritonitis.,3 antibiotikabehandling kan baseres på resultater af kultur-og følsomhedsdata. I første omgang,men, IV empirisk antibiotisk udvalg bør målrette sandsynligt organismspresent på det websted, hvorfra peritonitis stammer, som vist i TABEL 2.1
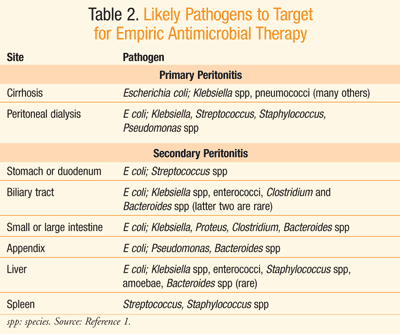
Der er forskelle mellem sundheds–forbundet og eu-associerede infektioner (TABEL 3).,3,6 Aminoglycosider er blandt de agenter, der anbefales til brug i empiricalantimicrobial terapi for health care–forbundet complicatedintra-abdominale infektioner, især dem, der skyldes byEnterobacteriaceae organismer, der producerer udvidet spectrumbeta-lactamases (ESBLs).3 Vancomycin anbefales i samme situation, når methicillinresistent Staphylococcus aureus (MRSA) er den forårsagende organisme af den sundhedsassocierede infektion.3 oprindelsen af infektionen med hensyn til anatomisk sted samt assetting (dvs .,, hospital eller samfund) hjælper guide udvælgelse af de mestrimelig empirisk antibiotikabehandling.

TABEL 4 viser den anbefalede empirisk antibiotisk behandlingsregimer for patienter med peritonitis, der har normal nyre-og lever-function3,6 eller en kreatinin-clearance mellem 70 og 100 mg/dL.7 i Betragtning af den stigende modstand af Escherichia coli til at quinoloner, sådanne lægemidler bør kun anvendes på et hospital, hvis undersøgelsen angiver >90% modtagelighed af E coli at quinoloner.,3 Der er også en bekymring over den hyppige brug af ertapenem, der fører til fremkomsten af carbapenem-resistente Enterobakterier organismer og Pseudomonas og Acinetobacter arter.3 Ampicillin-sulbactam bør undgås, når man målretter mod E coli, i betragtning af forekomsten af resistens over for lægemidlet.,3,8 Når en sundhedspleje–forbundet med infektion er et problem, at der er en højere risiko for infektion på grund af Candida og Enterococcusspecies, Fluconazol er berettiget til patienter, der har en malignitet,transplantation, inflammatorisk sygdom, tilbagevendende intra-abdominal infektion,mavesår på syre undertrykkelse, eller er på immunosuppressive therapyfor neoplasi.3 Ampicillin eller vancomycin kan tilsættes tilempirisk terapi for at målrette enterokokker hos dem med sundhedsassocieret infektion, især når det er en postoperativinfektion.,3 patienter, der vides at være koloniseret med Mrsaog dem med sundhedspleje–associeret peritonitis bør behandles medet antimikrobielt middel, der dækker MRSA, såsom vancomycin.3
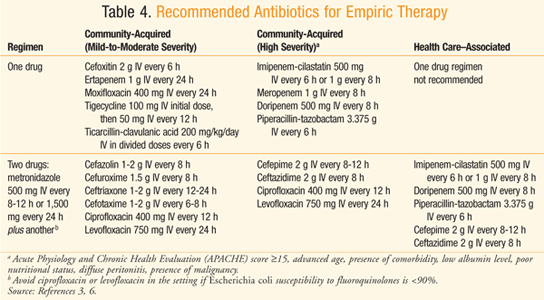
Der er særlige antimikrobielle dosering overvejelser for patienter, der er alvorligt syge og/eller overvægtige.9på grund af fysiologiske ændringer hos disse patienter kan visse farmakokinetiske faktorer ændres, såsom tilsyneladende fordelingsvolumen og/eller clearance.,3 hvis dosen er afhængig af nyrefunktionen, kan kreatininclearance desuden være nødt til at blive målt direkte på grund af vanskeligheden ved estimering, der kan henføres til den gennemsnitlige kropsvægt.3 kritisk syge patienter kan også opleve ændringer i visse farmakokinetiske parametre. For eksempel kan patienter i de tidlige stadier af sepsis opleve enhypermetabolisk tilstand og væskeskift, der kan forårsage øget volumen affordeling og clearance.3 sådanne skift kan resultere i lavere serumkoncentrationer af antimikrobielle stoffer, såsom beta-lactamer.,3på en lignende note er der observeret reducerede serumkoncentrationer af antimikrobielle stoffer som cephalosporiner og carbapenemer hos overvægtige patienter.3som følge af sådanne farmakokinetiske ændringer kan justeringer som højere doser og/eller hyppigere administration være påkrævet i dissesubgrupper af patienter.3 i tilfælde, hvor vancomycin er etpassende middel til kritisk syge og/eller overvægtige patienter, skal total kropsvægt anvendes til beregning af den indledende dosis.3 Desuden skal disse patienter have serum vancomycinkoncentration overvåget for at tilvejebringe individualiseret dosering.,3,10
Intraperitoneal dosering foretrækkes frem for IV-dosering til patienter i peritonealdialyse for at tilvejebringe højere lokale niveauer afantibiotika. Empirisk terapi bør dække både gram-positiv oggram-negative organismer, der vides at forårsage peritonitis. Intraperitonealantibiotika kan gives ved kontinuerlig dosering eller intermitterende dosering. Doseringsregimer bør tage hensyn til resterende nyfunktion, defineret som >100 mL/dag urinproduktion, i hvilket tilfældeanbefalede doser bør øges empirisk med 25%.,11dellell-time udveksling bør være mindst 6 timer, hvis du bruger intermitterende dosering. Den anbefalede behandlingsvarighed er 2 uger eller 3 uger tilmere alvorlige tilfælde. Behandlingen er afhængig af klinisk respons, sombør ses inden for 72 timer efter påbegyndelse af antibiotikabehandling.Patienter med uklar spildevand efter 4 til 5 dages passende antibiotisk behandling menes at have ildfast peritonitis og bør have deres kateter fjernet.11
akut nyresvigt er den vigtigste forudsigelse for død blandt patienter med spontan bakteriel peritonitis (SBP).,12Albumin er blevet anvendt i SBP til at forårsage plasmavolumenudvidelse for at mindske forekomsten af nyresvigt hos patienter med cirrose undergår storvolumenparacentese.13 En undersøgelse, der evaluererbrugen af IV-albumin ud over antimikrobiel terapi versusantimikrobiel terapi alene hos patienter med cirrose og SBP resulterede i en nedsat forekomst af nyresvigt og nedsat dødelighed.,13It blev fundet, at patienter, der blev behandlet, var mest tilbøjelige til at benefitfrom albumin, hvis de havde serum bilirubin-niveauer >4 mg/dL, serumcreatinine >1 mg/dL, og en blod urea nitrogen (BOLLE) koncentration>30 mg/dL.13 En anden undersøgelse bekræftede previouslyreported resultater og anvendte den samme dosering på 1,5 g/kg administreret på første dag, og 1 g/kg administreret på den tredje dag.,14Presently, der er ikke nok data til at understøtte brugen af albumin indlagte patienter med komplicerede SBP, eller med en serum bilirubin <4 mg/dL anda kreatinin af <1 mg/dL. Den Europæiske Sammenslutning til undersøgelse af leveren fastslår, at der er behov for yderligere undersøgelser for at vurdere albumin og andre volumenudvidelser i forvaltningen af SBP.15
antimikrobiel behandling bør begrænses til 4 til 7 dage.3 hvis tegn og symptomer på peritonitis er løst på dette tidspunkt, anbefales antibiotika ikke længere.,3hvis patienten er ved at komme sig på dette tidspunkt, kan tolerere en oral diæt og ikke demonstrerer modstand, er step-do .n-terapi med oralantibiotika berettiget.3 Antibiotika anbefales i thissetting omfatter moxifloxacin, en kombination af metronidazol med eitherlevofloxacin eller en mundtlig cephalosporin eller amoxicillin-clavulanate.Disse orale midler kan også bruges til dem, der behandles i ambulant indstilling, men blev indledt på indlæggelse IV-behandling.,3
behandlingssvigt efter 4 til 7 dages behandling bør undersøges ved hjælp af passende billeddannelsesteknikker, såsom CT-scanning ellerultralyd.3 antimikrobiel terapi, der er effektiv mod initialorganismer, bør fortsættes, og ekstra-abdominale infektionskilder bør udelukkes hos patienter, der ikke reagerer på terapi.Aerobe og anaerobe kulturer anbefales til patienter medinfektion tilbage efter indledende behandling.3
visse patientpopulationer bør overvejes tilprofylakse af bakteriel peritonitis., Primær bakteriel peritonitis kanforebygges ved anvendelse af antibiotika, hvis der er en kendt risikofaktor. For eksempel kan en enkelt IV-dosis vancomycin 1 g givet på tidspunktet forkateterplacering hos patienter, der gennemgår peritonealdialyse, hjælpeforhindre bakteriel peritonitis.11 Et alternativ til vancomycin er en enkelt dosis af cefazolin 1 g IV.11Secondary bakterielle peritonitis profylakse bør overvejes indlæggelser med skrumpelever, der er optaget til øvre GI-blødning.,12i fortiden, norfloxacin 400 mg dagligt havde været det foretrukne stof inthe indstilling af øvre GI-blødning; dog, alternative antimicrobialshave siden blevet betragtet som følge af epidemiologiske ændringer af bacterialinfections i en levercirrose (skrumpelever).12 ceftria .on 1 g IV har vist sig at være et effektivt alternativ.16
konklusion
Peritonitis, en akut betændelse i peritoneum, kanforekommer på grund af patogener eller andre årsager, såsom kemisk eksponering.Klinisk præsentation af primær peritonitis er ofte uspecifik ogkan mangle indledende tegn og symptomer., Omvendt sekundær peritonitisofte præsenterer med fremtrædende symptomer, herunder alvorlig smerte. Ubehandletperitonitis kan resultere i sepsis og endeorganskader; derfor bør hurtig behandling af bakteriel peritonitis styres af specificetiology og comorbiditeter.
almindelige antimikrobielle stoffer, der vælges til erhvervet i lokalsamfundet, omfatter cephalosporiner og fluorquuinoloner. Healthcare-erhvervet peritonitis kan kræve behandling med bredspektrantimikrobielle stoffer såsom carbapenemer., Patientkarakteristika skal overvejes i doseringsbeslutninger, og visse patientundergrupper som de kritisk syge og/eller overvægtige kan kræve dosisjustering på grund af variationer i farmakokinetiske parametre. I tilfælde af nonresponse tilempirisk terapi, kilder til infektion uden for maven bør værebetragtes. I alle tilfælde af peritonitis bør understøttende pleje væreordineret som angivet for at minimere komplikationer.
1. Dipiro JT, Ho ,dieshell TR. Intraabdominale Infektioner. I: Dipiro JT, Talbert RL, Yee GC, et al, eds. Farmakoterapi: En Patofysiologisk Tilgang. 8. udgave., Ne, York, NY: Mcgra.-Hill; 2011.
2. Ordone.CA, Carlos J. håndtering af peritonitis hos den kritisk syge patient. Surg Clin Nord Am. 2006;86:1323-1349.
3. Solomkin JS, Mazuski JE, Bradley JS, et al. Diagnostics and management of complicated intra-abdominal infektion hos voksne ogbørn: retningslinjer fra Surgical Infectious Diseases Society of America. Clin Inficere Dis. 2010;50:133-164.
4. Marshall JC, Maier RV, Jimene.M, Dellinger EP. Sourcecontrol i forvaltningen af alvorlig sepsis og septisk chok: anevidence-baseret gennemgang. Crit Pleje Medith., 2004; 32 (suppl): S513-s526.
5. Fris .ell A. overlevende Sepsis kampagne previe .s opdaterede retningslinjer for 2012. Pulmonal Rev. 2012; 17: 1,5. www.pulmonaryreviews.com/Article.aspx?ArticleId=sC3JHu + 0hSA=. åbnede 7. September 2012.
6. Klevens RM, Morrison MA, Nadle J, et al. Invasive methicillinresistente Staphylococcus aureus-infektioner i USA. JAMA. 2007;208:1763-1771.
7. Rybak MJ, Lomaestro BM, Rotschafer JC, et al.,Vancomycin terapeutiske retningslinjer: et resumé af consensusrecommendations fra Infectious Diseases Society of America, theAmerican Samfund af Sundheds-System, Farmaceuter, og det Samfund, ofInfectious Sygdomme Farmaceuter. Clin Inficere Dis. 2009;49:325-327.
8. Scheet m MH, Hurt KM, Noskin GA, Oliphant CM. Anvendelse af antimikrobielle farmakodynamik på resistente gram-negative patogener. Am J Sundhed Syst Pharm. 2006;63:1346-1360.
9. Murphy JE, Gillespie de, Bateman CV. Forudsigelighed for vancomycin gennem koncentrationer ved anvendelse af syv fremgangsmåder til vurdering af farmakologiske parametre., Am J Sundhed Syst Pharm. 2006;63:2365-2370.
10. O ,ens RC Jr, Shorr af. Rationel dosering af antimikrobielle stoffer: farmakokinetiske og farmakodynamiske strategier. Am J Sundhed Syst Pharm. 2009;66(suppl 4):S23-S30.
11. Piraino B, Bailie GR, Bernardini J, et al. Peritonealdialyserelaterede infektionsanbefalinger: 2005-opdatering. Perit Opkald Int. 2005;25:107-131.
12. Alani, C, Regal RE. Spontan bakteriel peritonitis: en gennemgang af behandlingsmuligheder. P T. 2009;34:204-210.
13. Sort P, Navasa m, Arroyo v, et al., Effekt afintravenøst albumin på nedsat nyrefunktion og dødelighed hos patienter medcirrhosis og spontan bakteriel peritonitis. N Engl J Med. 1999;341:403-409.
14. Sigal sh, Stanca CM, Fernande.J, et al. Begrænset brug af albumin til spontan bakteriel peritonitis. Tarm. 2007;56:597-599.
15. EASL klinisk praksis retningslinjer for håndtering afascites, spontan bakteriel peritonitis og hepatorenal syndrom incirrhosis. J Hepatol. 2010;53:397-417.
16. Fernande, J, Rui.del Arbol L, Gome, C, et al.,Norfloxacin vs ceftriaxone in the prophylaxis of infections in patientswith advanced cirrhosis and hemorrhage. Gastroenterology. 2006;131:1049-1056.