Licht hat sowohl Partikel-als auch Welleneigenschaften zur gleichen Zeit. Ebenso dachte de Broglie (Frankreich, 1892-1987), dass solche Dinge wie Elektronen, die bisher als Teilchen betrachtet worden waren, auch Wellennatur besitzen könnten (1932). Dies ist die Idee der de Broglie Wellen oder de Broglie Materie Wellen.,
Betrachten wir ein Wasserstoffatom mit Bohrs Quantentheorie. In dieser Theorie scheint die Quantenbedingung zur Bestimmung der stationären Zustände des Atoms zu behaupten, dass der Umfang der Umlaufbahn des Elektrons, das sich um den Kern dreht, ein integrales Vielfaches der Wellenlänge der De-Broglie-Welle des Elektrons sein sollte.
Diese Quantenbedingung besagt, dass die de Broglie-Welle des Elektrons eine kontinuierliche stehende Welle um den Kern sein muss.,
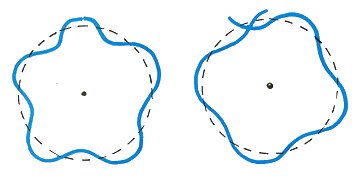
In der rechten Abbildung verbindet sich die de Broglie-Welle nicht reibungslos, da der Umfang kein integrales Vielfaches der Wellenlänge ist. Die richtige Zahl zeigt nämlich keine korrekte De-Broglie-Welle in einem Wasserstoffatom.