Cykloheksen właściwości chemiczne,zastosowania, produkcja
właściwości chemiczne
Cykloheksen (C6H10, Nr rejestru CAS 110-83-8) jest również nazywany tetrahydrobenzenem, który jest bezbarwną łatwopalną cieczą. Jest nierozpuszczalny w wodzie. Wdychanie wysokich stężeń może mieć działanie narkotyczne. Cykloheksen jest wysoce łatwopalny, więc powinien trzymać się z dala od ciepła i otwartego ognia. Może tworzyć nadtlenki w przechowywaniu, więc powinien być przechowywany pod nieobecność powietrza. Wdychanie lub wchłanianie przez skórę może powodować działania toksyczne., Wdychanie lub kontakt z materiałem może powodować podrażnienia lub oparzenia skóry i oczu. Ogień wytwarza drażniące, żrące i / lub toksyczne gazy.
Cykloolefina
Cykloheksen jest cykliczną olefiną i jest bezbarwną, łatwopalną cieczą o specjalnym ostrym zapachu w temperaturze pokojowej. Długotrwałe umieszczenie w powietrzu może być utleniane do nadtlenku przez powietrze. Naturalnie obecny w smole węglowej, rozpuszczalny w acetonie, czterochlorku węgla, benzenie, eterze, heksanie, etanolu i innych rozpuszczalnikach organicznych, może tworzyć binarną azeotropę z niższymi alkoholami, kwasem octowym itp., Cykloheksen ma ogólną naturę olefiny, szybko rozkłada się w obecności soli uranu pod wpływem światła słonecznego lub promieni ultrafioletowych, jest stały, ponieważ jest podgrzewany w zamkniętej rurze w temperaturze 200 ℃ przez długi czas, tworzy benzen i naftalen w temperaturze 400~500℃.
otrzymuje się go przez odwodnienie cykloheksanolu w wysokiej temperaturze w obecności katalizatora kwasowego w przemyśle. Otrzymuje się go przez siarczanowe odwodnienie cykloheksanolu w laboratorium.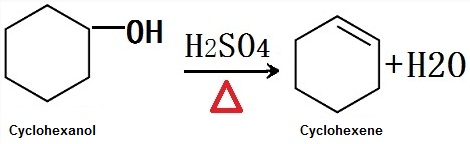
Rysunek 1 jest równaniem reakcji chemicznej siarczanowanego odwodnienia cykloheksanolu w celu uzyskania cykloheksenu.,
Cykloheksen jest ważnym surowcem chemicznym, stosowanym do produkcji kwasu adypinowego, aldehydu adypinowego, kwasu maleinowego, kwasu Cykloheksanowego, aldehydu cykloheksanowego, kwasu maleinowego, kwasu cykloheksylowego karboksylowego, aldehydu cykloheksanokarboksylowego w przemyśle. Jest również stosowany jako środek ekstrakcyjny, stabilizator posiadający wysokooktanową benzynę. Wdychanie może powodować łagodne zatrucie.
oto niektóre z tych ważnych związków przygotowanych przez cykloheksen, (1) chlorowany cykloheksan jest wytwarzany, przydatny jako półprodukty farmaceutyczne, rozpuszczalnik i Dodatki gumowe., (2) cykloheksanon jest wytwarzany z cykloheksenu, może być stosowany jako półprodukty surowców medycznych, pestycydów, perfum i barwników, jako modyfikatory polimerów. (3) octan cykloheksylu jest wytwarzany, stosowany jako rozpuszczalnik z tworzywa sztucznego. (4) fenol cykloheksanonowy jest wytwarzany, może być stosowany jako medycyna surowców i pestycydy. (5) aminocykloheksanol jest wytwarzany, może być stosowany jako środki powierzchniowo czynne i emulgatory. (6) produkt może być również stosowany bezpośrednio jako półprodukty organiczne, rozpuszczalniki i Dodatki podczas przygotowywania przypraw. Może być stosowany w przygotowaniu butadienu w laboratorium.,
powyższe informacje zostały zredagowane i zestawione przez Yan Yanyonga z Chemicalbook.
preparat
Cykloheksen można syntetyzować na kilka sposobów, takich jak dehydrogenacja cykloheksanu, dehydrohalogenacja cykloheksanu fluorowcowanego, redukcja brzozy lub częściowe uwodornienie benzenu. W porównaniu z innymi metodami, technologia częściowego uwodornienia benzenu do cykloheksenu ma zaletę bezpieczeństwa, wysokiej gospodarki atomowej, przyjaznej dla środowiska. Częściowe uwodornienie benzenu do cykloheksenu jest znane od ponad 100 lat.,
właściwości chemiczne
bezbarwna Łatwopalna ciecz. Nierozpuszczalny w wodzie, rozpuszczalny w eterze.
selektywne utlenianie
Cykloheksen może reagować energicznie z silnymi środkami utleniającymi., Chociaż jest prosty w swojej strukturze chemicznej, istnieją dwa potencjalne miejsca utleniania w cykloheksenie, a zwykłe reakcje utleniania prowadzą na ogół do mieszaniny produktów o różnych stanach utleniania i grupach funkcyjnych: utlenianie wiązania C=C (miejsce a) może prowadzić do 7-oksabicykloheptanu, trans/cis-cykloheksano-1,2-diolu lub kwasu adypinowego; utlenianie w pozycji allilowej C-H (miejsce b) może wytworzyć cykloheks-2-en-1-ol lub cykloheks-2-en-1-on., Produkty te są użytecznymi półproduktami przemysłowymi, które były szeroko stosowane w syntezie organicznej, chemii medycznej, chemii pestycydów, materiałoznawstwie itp. Dlatego kontrolowane reakcje utleniania dla cykloheksenu, które mogą selektywnie pozwolić sobie na docelowe produkty, są syntetycznie cenne dla zastosowań zarówno w Akademii, jak i przemyśle, stając się celem chemików syntetycznych i katalitycznych w tej dziedzinie.
wykorzystuje
- stosowany w syntezie organicznej, jest również stosowany jako rozpuszczalnik.,
- Cykloheksen jest stosowany jako organiczne surowce syntetyczne, takie jak syntetyczne surowce do lizyny, cykloheksanonu, fenolu, żywicy policykloolefinowej, chlorowanego cykloheksanu, dodatków gumowych, cykloheksanolu itp. Jest również stosowany jako rozpuszczalnik katalizatora i środek do ekstrakcji ropy naftowej, wysokooktanowy stabilizator benzyny.
- Cykloheksen stosuje się do wytwarzania kwasu adypinowego, kwasu maleinowego, kwasu heksahydro benzoesowego i aldehydu octowego, wytwarzania butadienu w laboratorium. Jest stosowany jako wysokooktanowy stabilizator benzyny.,
Metoda produkcji
cykloheksanol jest podgrzewany w celu wytworzenia cykloheksenu w obecności katalizatora kwasu siarkowego, destylowanego w celu uzyskania produktów surowych. Przemyte drobnym nasyconym roztworem soli, następnie roztwór siarczanu sodu stosuje się do neutralizacji śladów kwasu, a następnie przemywa się wodą, warstwuje, suszy, filtruje, destyluje, zbierając 82-85 ℃ produktów destylacyjnych w celu uzyskania cykloheksenu.
charakterystyka zagrożenia palności
w przypadku pożaru, wysokiej temperatury, utleniacza, jest łatwopalny, palenie wytwarza drażniący dym.,
charakterystyka przechowywania
wentylacja Skarbowa suszenie niskotemperaturowe, przechowywane oddzielnie od utleniaczy i kwasów. Niezbyt długie przechowywanie, aby zapobiec polimeryzacji.
właściwości chemiczne
Cykloheksen jest bezbarwną cieczą (cykliczną) o słodkawym zapachu.
właściwości fizyczne
przezroczysta, bezbarwna ciecz o słodkim zapachu. Stężenie progowe zapachu wynosi 0,18 ppm (cytowane, Amoore i Hautala, 1983).
wykorzystuje
występuje w smole węglowej i otrzymuje się go przez katalityczne poddanie cykloheksanolu i dehydrogenację cykloheksanu., Cykloheksen jest stosowany w wytwarzaniu kwasu adypinowego, kwasu maleinowego i butadienu; w ekstrakcji oleju; jako stabilizator benzyny wysokooktanowej; oraz w syntezie organicznej.
wykorzystuje
Składnik alkilacji. W produkcji kwasu adypinowego, kwasu maleinowego, kwasu heksahydrobenzoesowego i aldehydu. Aby przygotować butadien w laboratorium. Został zasugerowany do syntezy kwasu maleinowego i jako stabilizator benzyny wysokooktanowej.,
zastosowanie
produkcja kwasu adypinowego, kwasu maleinowego, kwasu heksahydrobenzoesowego i aldehydu; Stabilizator dla benzyny wysokooktanowej
metody produkcji
Cykloheksen jest otrzymywany przez odwodnienie cykloheksanolu przez reakcję termiczną mieszaniny etylenowo-propylenowo-butadienowej (1).
definicja
ChEBI: cykloalken, czyli cyloheksan z pojedynczym wiązaniem podwójnym.
Opis ogólny
bezbarwny płyn. Nierozpuszczalny w wodzie i mniej gęsty niż woda. Temperatura zapłonu 20°F. opary cięższe niż powietrze. Wdychanie wysokich stężeń może mieć działanie narkotyczne. Używany do produkcji innych chemikaliów.,
powietrze & reakcje wody
wysoce łatwopalne. Nierozpuszczalny w wodzie.
profil reaktywności
Cykloheksen może reagować energicznie z silnymi utleniaczami. Może reagować egzotermicznie ze środkami redukującymi, uwalniając gaz wodorowy. W obecności różnych katalizatorów (takich jak kwasy) lub inicjatorów, mogą podlegać egzotermiczne reakcje polimeryzacji addycyjnej. Łatwo utlenia się w powietrzu, tworząc niestabilne nadtlenki, które mogą wybuchnąć samoistnie .
zagrożenie dla zdrowia
dostępnych jest bardzo niewiele danych toksykologicznych dotyczących cykloheksenu., Wytwarzanie inhalacjiodrażnienie oczu i dróg oddechowych. Jest również drażniący dla skóry. Jego ostra toksycznośćjest niska; działanie toksyczne jest podobne do działania cykloheksanu. Narażenie na duże koncentracje lub spożycie może powodować senność.Pojedyncze narażenie na 15 000 ppm cykloheksenu może być śmiertelne dla szczurów.
zagrożenie pożarowe
wysoce łatwopalne: łatwo zapala się przez ciepło, iskry lub płomienie. Opary mogą tworzyć wybuchowe mieszaniny z powietrzem. Opary mogą podróżować do źródła zapłonu i błysk z powrotem. Większość oparów jest cięższa od powietrza., Będą one rozprzestrzeniać się wzdłuż ziemi i zbierać się w niskich lub zamkniętych obszarach (kanały, piwnice, zbiorniki). Zagrożenie wybuchem pary w Pomieszczeniach, Na zewnątrz lub w kanałach. Odpływ do kanalizacji może spowodować pożar lub wybuch. Pojemniki mogą eksplodować po podgrzaniu. Wiele płynów jest lżejszych od wody.
profil bezpieczeństwa
umiarkowanie toksyczny przez drogi oddechowe i połknięcie. Bardzo niebezpieczne zagrożenie pożarowe pod wpływem płomienia; może reagować z utleniaczami. Niebezpieczne; trzymać z dala od ciepła i otwartego ognia. Aby walczyć z ogniem, użyj pianki, CO2, suchej substancji chemicznej.,
potencjalne narażenie
może być stosowane jako półprodukt w produkcji innych substancji chemicznych (np. kwas adypinowy, Kwas maleinowy, kwas heks-ahydro benzoesowy), ekstrakcji oleju oraz jako katalizator.
Rakotwórczość
Cykloheksen nie wykazywał działania mutagennego u Salmonellatyphimurium z aktywacją metaboliczną lub bez niej.
Los środowiskowy
biologiczny. Cykloheksen ulega biodegradacji do cykloheksanonu (Dugan, 1972; Verschueren, 1983).
Fotolityczne. Dla reakcji cykloheksenu z Ohradykalami w atmosferze odnotowano następujące stałe szybkości: 6,80 x 10-11 cm3 / cząsteczka?sec (Atkinson et al., 1979), 6.,75 x 10-11cm3 / molecule?sec at 298 K (Sablji? and Güsten, 1990), 5.40 x 10-11 cm3/molecule?sec at 298 K (Rogers, 1989), 1.0 x 10-10 cm3/molecule?sec at 298 K (Atkinson, 1990); with ozone in the gasphase:1.69 x 10-16 cm3/molecule?sec at 298 K (Japar i in., 1974), 2.0 x 10-16 at 294 K (Adeniji etal., 1981), 1.04 x 10-16 cm3/molecule?sec (Atkinson i in., 1983), 1.04 x 10-16 at 298 K (Atkinsonand Carter, 1984); with No3 in the atmosphere: 5.26 x 10-13 cm3/molecule?sec (Sablji? and Güsten, 1990); 5.3 x 10-13 cm3/molecule?sec at 298 K (Atkinson, 1990), and 5.28 x 10-13 cm3/molecule?,secat 295 K (Atkinson, 1991). Cox et al. (1980) zgłosił stałą szybkości 6,2 x 10-11cm3/cząsteczka?sec dla reakcji gazowego cykloheksenu z rodnikami OH na podstawie wartości 8x 10-12 cm3/cząsteczka?sec dla reakcji etylenu z rodnikami OH.
chemiczne / fizyczne. Gazowymi produktami powstałymi w reakcji cykloheksenu z ozonem były (%wydajności): kwas mrówkowy , tlenek węgla , dwutlenek węgla, etylen i aldehyd (Hatakeyama et al., 1987). W eksperymencie Komory smogowej przeprowadzonym w temperaturze 25 °C cykloheksan reagował z ozonem., The following products and their respective molaryields were: oxalic acid (6.16%), malonic acid (6.88%), succinic acid (0.63%), glutaric acid(5.89%), adipic acid (2.20%), 4-hydroxybutanal (2.60%), hydroxypentanoic acid (1.02%),hydroxyglutaric acid (2.33%), hydroxyadipic acid (1.19%), 4-oxobutanoic acid (6.90%), 4-oxopentanoic acid (4.52%), 6-oxohexanoic acid (4.16%), 1,4-butandial (0.53%), 1,5-pentanedial(0.44%), 1,6-hexanedial (1.64%), and pentanal (17.05%).
Grosjean et al., (1996) investigated the atmospheric chemistry of cyclohexene with ozone and anozone-nitrogen oxide mixture under ambient conditions. The reaction of cyclohexene and ozone inthe dark yielded pentanal and cyclohexanone. The sunlight irradiation of cyclohexene with ozonenitrogenoxide yielded the following carbonyls: formaldehyde, acetaldehyde, acetone, propanal,butanal, pentanal, and a C4 carbonyl.
Cyclohexene reacts with chlorine dioxide in water forming 2-cyclohexen-1-one (Rav-Acha etal., 1987).
Shipping
UN2256 Cyclohexene, Hazard Class: 3; Labels:3-Flammable liquid.,
metody oczyszczania
wolny cykloheksen z nadtlenków przez przemywanie kolejnymi porcjami rozcieńczonego zakwaszonego siarczanu żelaza lub roztworem NaHSO3, następnie wodą destylowaną, suszenie za pomocą CaCl2 lub CaSO4 i destylację pod N2. Alternatywne metody usuwania nadtlenków obejmują przejście przez kolumnę tlenku glinu, refluksowanie drutem sodowym lub stearynianem miedziowym (następnie destylację z sodu). Dien jest usuwany przez refluxing z bezwodnikiem maleinowym przed destylacją w próżni. Zabieg 0,1 moli MeMgI w 40mL eteru dietylowego usuwa ślady utlenionych zanieczyszczeń., Inne procedury oczyszczania obejmują mycie wodnym NaOH, suszenie i destylację pod N2 przez przędzową kolumnę taśmową, redestylowanie z CaH2, przechowywanie pod drutem sodowym i przechodzenie przez kolumnę tlenku glinu, pod N2, bezpośrednio przed użyciem. Przechowywać w
Substancja może tworzyć wybuchowe nadtlenki. Podpunkt może ulegać polimeryzacji pod pewnymi warunkami.Niekompatybilny z utleniaczami (chlorany, azotany, nadtlenki,nadmanganiany, nadchlorany, chlor, brom, fluor itp.); kontakt może powodować pożary lub wybuchy., Trzymaj się z dala od materiałów alkalicznych, silnych zasad, silnych kwasów, oksoa-cids, epoksydów.
Usuwanie odpadów
rozpuścić lub wymieszać materiał z palnym rozpuszczalnikiem i spalić w spalarni chemicznej-tor wyposażonej w dopalacz i płuczkę. Wszystkie federalne, stanowe i lokalne przepisy dotyczące ochrony środowiska muszą być przestrzegane.