Hintergrund
Primärer Hyperparathyreoidismus (PHPT) ist die dritthäufigste endokrine Erkrankung. Es wird in 85% bis 90% der Fälle durch ein einzelnes Nebenschilddrüsenadenom verursacht. Vitamin-D-Mangel (VDD) ist ein häufiger Befund bei PHPT mit einer Inzidenz, die in der Literatur von 53% bis 77% variiert. Ziel unserer Studie ist es, eine Kohorte von Patienten mit PHTP mit und ohne VDD zu beschreiben.,
Methoden
Retrospektive Studie aus einer prospektiv gehalten Datenbank der Patienten mit PHPT behandelt, die von unserer Gruppe, die zwischen Januar 2015 und Juli 2017. Die durchgeführte Operation war eine bilaterale Halsuntersuchung durch einen zwei Zentimeter langen Einschnitt mit radioguided Parathyreoidektomie. Die Eigenschaften der Patienten wurden aus den elektronischen Krankenakten ermittelt und analysiert. Patienten ohne vollständige Krankenakten wurden nicht in unsere Studie aufgenommen., Alle Daten wurden in nicht identifizierbarer Weise gemäß den in der Deklaration von Helsinki dargelegten Grundsätzen und gemäß den Anforderungen für die Genehmigung durch unseren Institutional Review Board erhoben.
Ergebnisse und Diskussion
insgesamt 50 Patienten mit PHPT enthalten waren, vier Fünftel von Ihnen waren Frauen und ein Fünftel waren Männer; das Durchschnittsalter der Patienten in unserer Studie lag bei 56,7 Jahren. Die mittlere präoperative PTH betrug 97 pg / ml mit signifikant vermindertem postoperativen Wert (alle Patienten wurden geheilt, normale Calcium-und PTH-Spiegel 12 Monate nach der Operation). Das mittlere präoperative Kalzium betrug 10.,2 mg/dl. Fünfunddreißig Patienten (70%) hatten vor der Operation eine präoperative VDD und hatten eine subjektive Verschlimmerung ihrer PHPT-Symptome, als Vitamin D verabreicht wurde, um das Defizit zu korrigieren. Der mittlere präoperative Vitamin D (VD) – Spiegel betrug 27,5 ng/dl und nach acht Wochen nach der Operation 29,1 ng / dl (Bereich: 13,2 bis 50). Pathologiebericht zeigte, dass fast 88% der Fälle durch einzelne oder doppelte Adenome (76% durch einzelne Adenome) und 12% durch hyperplasische Drüsen verursacht wurden.,
Schlussfolgerung
In unserer Serie hatten fast alle unsere Patienten mit PHPT ein einzelnes oder ein doppeltes Adenom und keine Drüsenhyperplasie. VDD verbesserte sich ohne VD-Supplementierung nach Heilung des PHPT. Diese Ergebnisse legen nahe, dass VDD aufgrund der sehr geringen Inzidenz von Schilddrüsenhyperplasie keine PHPT verursacht.
Schlüsselwörter
Hyperparathyreoidismus, Vitamin-D-Mangel, Nebenschilddrüsenadenom
Einführung
Die Überproduktion von Nebenschilddrüsenhormon (PTH), Hyperparathyreoidismus (HPT) genannt, kann als primär, sekundär oder tertiär eingestuft werden ., Primärer Hyperparathyreoidismus (PHPT) entsteht durch eine ungeregelte Überproduktion von PTH aus einer abnormalen Nebenschilddrüse oder Drüsen . Die Prävalenz von PHPT ist seit dem Aufkommen routinemäßiger Labortests gestiegen, von denen ein bis sieben Personen pro 1000 Personen und Jahr betroffen sind (die Prävalenz ist von 0, 1% auf 0, 4% gestiegen) in den Vereinigten Staaten von Amerika . Es ist die dritthäufigste endokrine Diagnose und die häufigste Ursache für Hyperkalzämie im ambulanten Bereich ., Die überwiegende Mehrheit der Patienten mit PHPT ist älter als 45 Jahre, wobei das Durchschnittsalter bei der Diagnose zwischen 52 und 59 Jahren lag . Das Risiko, an PHPT zu erkranken, ist bei Frauen fünfmal höher als bei Männern mit einem Verhältnis von 3 zu 4:1 zwischen Frauen und Männern . Die meisten Fälle (85% bis mehr als 90%) von PHPT sind sekundär zu einem einzelnen Nebenschilddrüsenadenom . Die Diagnose von PHPT wird normalerweise biochemisch mit der Kombination von Hyperkalzämie und einem erhöhten oder unangemessen normalen PTH-Spiegel gestellt ., Vitamin-D-Mangel (VDD) ist ein sehr häufiger Befund bei Patienten mit PHPT, wobei die berichtete Inzidenz zwischen 53% und 77% der Fälle variiert . Wir definierten Vitamin-D-Mangel basierend auf einem Papier von Norman, et al. , in dem er den Normalbereich über 35 ng/ml in Reihen von mehr als 10.000 Patienten mit nachgewiesener PHPT definierte. Es gibt ein Missverständnis, dass Patienten mit Hyperkalzämie, erhöhten PTH-Spiegeln und VDD, dass der Ursprung des erhöhten PTH-Spiegels und des Kalziumspiegels sekundär zu den niedrigen Vitamin-D-Spiegeln ist., Ziel unserer Studie ist es, eine Kohorte von Patienten mit PHPT mit oder ohne VDD zu beschreiben und zu zeigen, dass die überwiegende Mehrheit der Patienten mit PHPT (nachgewiesen mit Biopsie der abnormalen Nebenschilddrüse) eine einzelne Drüsenerkrankung mit VDD hat und nicht vier Drüsenhyperplasie, wie es zu erwarten ist, wenn der Ursprung des PHPT der VDD war.
Materialien und Methoden
Dies ist eine retrospektive Studie aus einer prospektiv gepflegten Datenbank von Patienten mit PHPT, die von unserer Gruppe von Januar 2015 bis Juli 2017 im American British Cowdray Medical Center in Mexiko-Stadt behandelt wurden., Die von unserer Gruppe durchgeführte Operation bestand aus einer bilateralen Halskorrektur durch einen zwei Zentimeter langen Einschnitt und einer radioguided Parathyreoidektomie, wie sie zuvor von verschiedenen Autoren beschrieben wurde . Wir verwenden weiterhin intraoperative PTH-Spiegel (Basislinie, 10 und 20 Minuten nach einer Resektion) . Die Patientendemografie, die aus unseren elektronischen Krankenakten erhalten wurde, umfasste Alter, Geschlecht, präoperative, 24 Stunden, 8 Wochen postoperative Serumkalzium-und PTH-Spiegel. Die präoperativen, postoperativen Vitamin-D-Spiegel und die pathologischen Ergebnisse wurden ebenfalls überprüft., Die Daten wurden analysiert Berechnung der absoluten und relativen Frequenzen, Maß der zentralen Tendenz nach den Variablen. Patienten ohne vollständige Krankenakten wurden nicht einbezogen. Alle Daten wurden in nicht identifizierbarer Weise gemäß den in der Deklaration von Helsinki dargelegten Grundsätzen und gemäß den Anforderungen für die Genehmigung durch unseren Institutional Review Board erhoben .
Ergebnisse
Insgesamt 50 Patienten mit PHPT wurden in unsere Studie einbezogen. Vier Fünftel der Patienten waren Frauen und ein Fünftel waren Männer; Das Durchschnittsalter bei der Diagnose für unsere Studienpopulation war 56.,7 jahre (Bereich: 29 bis 87). Der mittlere präoperative PTH betrug 97 pg/ml (Bereich: 26,5 bis 247), der postoperative 24-Stunden-Wert 38,7 pg/ml und nach acht Wochen nach der Operation 55,2 pg / ml. Der mittlere präoperative Calciumspiegel betrug 10,2 mg/dl (Bereich: 8,8 bis 11,9), nach 24 Stunden und acht Wochen nach der Operation 8,6 mg/dl bzw. Fünfunddreißig Patienten (70%) hatten vor der Operation eine präoperative VDD und hatten eine subjektive Verschlimmerung ihrer PHPT-Symptome, wenn eine Korrektur präoperativ versucht wurde. Der mittlere präoperative VD-Spiegel betrug 27,5 ng/dl und nach acht Wochen nach der Operation 29.,1 ng / dl (Bereich: 13,2 bis 50). Der abschließende Pathologiebericht zeigte, dass fast 88% der Fälle durch ein einzelnes oder doppeltes Adenom (76% der Fälle durch ein einzelnes Adenom) und 12% der Fälle durch vier Drüsenhyperplasie verursacht wurden.
PHPT ist definiert als Hyperkalzämie oder stark schwankende Serumcalciumspiegel, die aus der unangemessenen oder autogenen Sekretion von PTH durch eine von mehreren Nebenschilddrüsen in Abwesenheit eines bekannten oder anerkannten Stimulus resultieren . Ungefähr 100.000 neue Fälle pro Jahr werden in den USA gemeldet ., Der genaue Ursprung von PHPT ist unbekannt, obwohl die Exposition gegenüber niedrig dosierter therapeutischer ionisierender Strahlung und familiärer Veranlagung für einige Fälle verantwortlich ist . Bei der Entwicklung von PHPT wurden verschiedene genetische Aberrationen identifiziert, einschließlich Anomalien in den Tumorsuppressorgenen und Proto-Onkogenen. Bestimmte DNA-Mutationen in der Nebenschilddrüsenzelle können einen proliferativen Vorteil gegenüber normalen Nachbarzellen haben und so ein klonales Wachstum ermöglichen ., Große Populationen dieser veränderten Zellen, die die gleiche Mutation innerhalb eines funktionierenden Nebenschilddrüsengewebes enthalten, legen nahe, dass solche Drüsen ein Ergebnis der klonalen Expansion sind . Die meisten PHPT-Fälle sind sporadisch, dennoch tritt PHPT auch im Spektrum einer Reihe von Erbkrankheiten auf, wie multiple endokrine Neoplasien (MÄNNER), MÄNNER Typ 1 (Wermer-Syndrom) , MÄNNER Typ 2A (Sipple-Syndrom) , isolierte familiäre HPT und familiäre HPT mit Kiefer-Tumor-Syndrom . Alle diese werden autosomal dominant vererbt.,
Unabhängig davon, was die meisten Literaturberichte berichten, ist PHPT in mehr als 95% der Fälle symptomatisch, wenn den subtilen Symptomen und Anzeichen, die diese Krankheit aufgrund des schwankenden Kalziumspiegels hervorrufen kann, gebührende Aufmerksamkeit geschenkt wird . PHPT wird biochemisch mit der Kombination von Hyperkalzämie und einem erhöhten oder unangemessen normalen PTH-Spiegel diagnostiziert . Die Mehrheit der Patienten mit PHPT wird eine gleichzeitige VDD haben, wobei die berichtete Inzidenz zwischen 53% und 77% der Fälle variiert . Bei unseren Patienten hatten 70% unserer Patienten (35 Patienten) eine präoperative VDD., Dies ist im Vergleich zu einer Serie von Norman, et al. . In dieser Serie von mehr als 10.000 Patienten mit nachgewiesener PHPT wurde festgestellt, dass 77% der Patienten 25 OH-Vitamin-D-Spiegel unter 30 ng/ml (normaler Bereich über 35 ng/ml), 36% Werte unter 20 ng/ml und keiner der Patienten hatten erhöhte 25 OH-Vitamin-D-Spiegel. VDD ist bei Patienten mit PHPT mit einem Durchschnittswert von 22,4 ng/ml zu erwarten . In unserer Studie hatten 70% unserer Patienten vor der Operation eine präoperative VDD mit einem mittleren präoperativen VD-Spiegel von 27, 5 ng / dl., Die Patienten in unserer Kohorte mit VDD hatten eine subjektive Verschlimmerung ihrer PHPT-Symptome, wenn eine Korrektur präoperativ versucht wurde. Diese Patienten hatten Hyperkalzämie und VDD, wir ersetzen VDD normalerweise nicht bei Patienten mit offener Hyperkalzämie.
Fuller Albright führte in den 1930er und 1940er Jahren umfassende Forschungen zur Physiologie der Nebenschilddrüsen durch und verbesserte so unser Verständnis der komplexen Wechselwirkung und Homöostase des Calciumstoffwechsels ., Nichtsdestotrotz wurde erst in den 1960er Jahren über die Bedeutung von Vitamin D bei Nebenschilddrüsenerkrankungen in einem Fall mit begleitender Osteomalazie und PHPT berichtet . Es wurde berichtet, dass VDD im Winter etwa 14% der gesunden erwachsenen Bevölkerung betrifft . Wie bereits erwähnt, sind VDD und PHPT in einer Studie von Kantorovitch et al.relativ häufig. , bestehend aus 229 Patienten, die zur Bewertung der niedrigen Knochenmineraldichte (BMD) überwiesen wurden, ergab eine Prävalenz von 2.2% für koexistierende VDD und PHPT in ihrer Kohorte. VDD scheint den Schweregrad von PHPT zu beeinflussen. Silverberg, et al., , untersuchte den Zusammenhang von vitamin-D-Spiegel auf der schwere der Erkrankung in der 124 Patienten mit PHPT. Diejenigen mit den niedrigsten Vitamin-D-Spiegeln (25-Hidroxy-Vitamin D/25 OHD) hatten höhere PTH-Konzentrationen und einen höheren Knochenumsatz in Biopsiestudien. In einer anderen Studie mit 148 Patienten mit PHPT, Rao, et al. zeigte eine inverse Korrelation zwischen serum-25-OHD-und Nebenschilddrüse Gewicht. Das Vorhandensein größerer Nebenschilddrüsenadenome bei PHPT-Patienten mit VDD kann die Zunahme der Schwere der Erkrankung erklären .,Jahrhundert hatten signifikante Verbesserungen bei der Vitamin-D-Supplementierung, die zu einer Veränderung der klinischen Darstellung von PHPT führten . Osteitis fibrosa cystica (gesehen in weniger als 5% der Fälle von PHPT) wurde eine seltene Manifestation der Krankheit und die PTH-Spiegel und das Gewicht der Nebenschilddrüsenadenome nahmen dramatisch ab . Die Beziehung von VDD und PHPT ist auf zwei getrennten Ebenen offensichtlich. Erstens scheint die Krankheit unabhängig von der klinischen Schwere der PHPT bei Personen mit begleitender VDD schwerwiegender zu sein., Zweitens scheint VDD bei Patienten mit PHPT häufiger zu sein als bei geografisch übereinstimmenden Populationen . Der Zusammenhang zwischen VDD und PHPT hat klare Implikationen. Begleitende VDD und PHPT können dazu führen, dass der Serumcalciumspiegel in den normalen Bereich fällt (normokalzämischer PHPT), was zu diagnostischen Schwierigkeiten führen kann .
Es gibt ein Missverständnis, dass Patienten mit Hyperkalzämie, erhöhten PTH-Spiegeln und VDD, dass der Ursprung des erhöhten PTH-Spiegels und des Kalziumspiegels sekundär zu den niedrigen Vitamin-D-Spiegeln ist Niedrige Vitamin-D-Spiegel verursachen KEINE hohen Serumcalciumspiegel ., Die Idee, dass VDD eine Abnahme der Serumcalciumspiegel verursacht (aufgrund der Abnahme der intestinalen Absorption) und dass diese Abnahme der Serumcalciumkonzentration zu einer Aktivierung aller vier Nebenschilddrüsen führt, wobei eine nachfolgende Vier-Drüsen-Nebenschilddrüsenhyperplasie zu einer Erhöhung der PTH-Sekretion führt, die Hyperkalzämie fördert, sollte überdacht werden (Abbildung 1). Norman, et al., , ergab, dass 98% der Patienten in ihrer Studie, die PHPT mit gleichzeitiger VDD hatten, ein Nebenschilddrüsenadenom hatten und nur zwei Prozent eine Nebenschilddrüsenhyperplasie hatten, die das derzeitige Denken widerlegte (Abbildung 1). Dies gilt für unsere Studienpopulation, in der der abschließende Pathologiebericht zeigte, dass fast 88% der Fälle durch ein einzelnes oder doppeltes Adenom (76% der Fälle durch ein einzelnes Adenom) und 12% der Fälle durch eine Drüsenhyperplasie verursacht wurden.
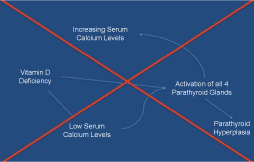 Abbildung 1: Fehlerhafte Pathophysiologie des sekundären Hyperparathyreoidismus., Abbildung 1
Abbildung 1: Fehlerhafte Pathophysiologie des sekundären Hyperparathyreoidismus., Abbildung 1
In Bezug auf das Management legen vorläufige Daten zur Vitamin-D-Repletion bei Patienten mit leichter PHPT nahe, dass in einigen Fällen eine Korrektur der VDD ohne Verschlechterung der zugrunde liegenden Hyperkalzämie durchgeführt werden kann , aber andere verfügbare Daten legen nahe, dass die Vitamin-D-Repletion die Hyperkalzämie, die Hyperkalziurie und die Symptome von PHPT verschlimmern kann In einigen seltenen Fällen verursacht eine hyperkalzämische Krise ., Die Patienten in unserer Kohorte mit PHPT und VDD hatten eine subjektive Verschlimmerung ihrer Symptome, als die Korrektur präoperativ versucht wurde, aber diese Beobachtung kann voreingenommen sein, da wir keine formellen Fragebögen zu Symptomen vor und nach der Operation durchgeführt haben.
Mehrere Studien haben sich auf die Repletion von VDD in PHPT konzentriert, und oft mit Zusatz von Patienten mit leichten und minimal symptomatischen oder in den seltenen Fällen von wirklich asymptomatischen Erkrankungen, die nicht internationalen Kriterien für die Operation entsprechen. Die größeren Studien sind typische prospektive, aber unkontrollierte oder historische Beobachtungsstudien., In diesen Studien kann die Änderung der klinischen Diagnose, der Labordiagnostik und des Managements im Laufe der Zeit die Ergebnisse beeinflussen, die zu einer Verzerrung ihrer Schlussfolgerungen führen. Shah, et al. , führte 2014 eine Metaanalyse der Weltliteratur durch und kam zu dem Schluss, dass der Vitamin-D-Ersatz bei Probanden mit PHPT und koexistentem VDD die OHD um 25 erhöht und die Serum-PTH signifikant reduziert, ohne Hyperkalzämie und Hyperkalziurie zu verursachen, erwähnte jedoch, dass der Befund ihrer Studie durch größere randomisierte Kontrollstudien bestätigt werden muss., In der Literatur wurde berichtet, dass der Ersatz von Vitamin D bei Patienten mit PHPT den PTH-Spiegel und den Knochenumsatz senken und möglicherweise die Knochenmasse in verschiedenen Kompartimenten erhöhen kann oder nicht . Bei einigen Patienten treten jedoch erhöhte Kalziumspiegel im Plasma auf, die entweder einen Vitamin-D-Entzug oder eine Operation auslösen . Der dritte internationale Workshop zum Management milder PHPT empfiehlt die Vitamin-D-Repletion . Wie oben beschrieben, sind die wissenschaftlichen Beweise für diese Empfehlung jedoch schwach., Nur prospektive, randomisierte und geblindete, placebokontrollierte Studien können den Nachweis für eine Vitamin-D-Repletion oder-behandlung bei PHPT erbringen.
Wie bei allen retrospektiven Serien weist unsere Studie mehrere Einschränkungen auf: Der retrospektive Aspekt kann zu Selektionsverzerrungen und Fehlklassifizierungen oder Informationsverzerrungen führen, die zeitliche Beziehung ist häufig schwer zu beurteilen. Retrospektive Studien benötigen möglicherweise sehr große Stichprobengrößen für seltene Ergebnisse, und unsere Stichprobengröße ist im Vergleich zu anderen Autoren begrenzt., Wir haben keine 1,25-Dihydroxyvitamin-D-Konzentrationen gemessen Dies hätte uns geholfen zu sehen, wie sich der VDD verbessert, ohne dass nach einer Parathyreoidektomie eine Supplementierung erforderlich wäre. Unsere Gruppe korrigiert die VDD nicht, wenn eine symptomatische PHPT diagnostiziert wird., Bei der Einstellung normaler oder niedriger normaler Serumcalciumkonzentrationen mit minimalen Erhöhungen der PTH-Spiegel (größer als 65 bis weniger als 100 pg/dl) und minimal symptomatischer Erkrankung, bei der die Diagnose eines normokalzämischen PHPT unterhalten wird, aber nicht von VDD-induzierten Erhöhungen unterschieden werden kann, korrigieren wir den VDD (unser Ziel ist ein 25-OHD über 35 bis 40 ng/dl), aber mit enger Überwachung der Patienten, um eine schnelle Diagnose verschlimmernder Symptome rechtzeitig zu stellen und den normokalzämischen PHPT angemessen mit einer Operation zu behandeln.,
Schlussfolgerung
In unserer Serie hatten die meisten Patienten PHPT sekundär zu Adenomen, nicht Vier-Drüsen-Hyperplasie. VDD verbesserte sich ohne VD-Supplementierung nach Resektion der Adenome. Diese Ergebnisse legen nahe, dass VDD nicht die PHPT verursacht, sondern ein häufiger Befund ist, der bei der Diagnose helfen kann. Vorsicht ist geboten, wenn eine Supplementierung mit Vitamin D bei Patienten mit normalen oder niedrigen normalen Serumcalciumkonzentrationen mit minimalen Erhöhungen der PTH-Spiegel empfohlen wird, bei denen die Diagnose einer normokalzämischen PHPT gestellt wird, die jedoch nicht von VDD unterschieden werden kann.,
Konkurrierende Interessen
Die Verfasser erklären, dass sie keine konkurrierenden Interessen haben.
Die Autoren haben keine nicht finanziellen konkurrierenden Interessen (politische, persönliche, religiöse, ideologische, akademische, intellektuelle, kommerzielle oder andere) in Bezug auf dieses Manuskript zu erklären.,ns
Idee: Rodrigo Arrangoiz
Literaturübersicht, Datensammlung, erste Manuskript Ausarbeitung und Bearbeitung: Rodrigo Arrangoiz, Luis Fernando Negrete, Jorge Sánchez-García
Letzte Manuskript Ausarbeitung: Rodrigo Arrangoiz
Überprüfung und Bearbeitung des Manuskripts: Rodrigo Arrangoiz, David Caba, Fernando Cordera, Luis Fernando Negrete, Eduardo Moreno, Enrique Luque, Jorge Sánchez-García, Efrain Cruz, Manuel Muñoz
Die Ergebnisse dieses Manuskripts wurden in einer mündlichen Präsentation auf der Konferenz des Academic Surgical Congress im Januar 2018 in Jacksonville, Florida, vorgestellt.,
- Arrangoiz R, Lambreton F, Luque-De-Leon E, Fernando Cordera, Muñoz-Juárez M, et al. (2016) Aktuelles Denken über primären Hyperparathyreoidismus. JSM Kopf-Hals-Krebs-Fälle Rev 1: 1002.
- Norman J, Goodman A, Politz D (2011) Calcium, Parathormon und vitamin D bei Patienten mit primärem Hyperparathyreoidismus: Referenzwerten entwickelt von 10.000 Fällen. Endocr Pract 17: 384-394.
- Wermers RA, Khosla S, Atkinson EJ, Achenbach SJ, Oberg AL, et al., (2006) Inzidenz von primärem Hyperparathyreoidismus in Rochester, Minnesota, 1993-2001: ein Update über die sich ändernde Epidemiologie der Krankheit. J Bone Miner Res 21: 171-177.
- Adami S, Marcocci C, Gatti D (2002) Epidemiologie des primären Hyperparathyreoidismus in Europa. J Knochen Miner Res 17: 18-23.
- Habib Z, Camacho-P (2010) Primären Hyperparathyreoidismus: ein update. Curr Opin Endocrinol Diabetes Obes 17: 554-560.
- Khan AA, Hanley DA, Rizzoli R, Bollerslev J, Young JE, et al., (2017) Primärer Hyperparathyreoidismus: Überprüfung und Empfehlungen zu Bewertung, Diagnose und Management. Ein kanadischer und internationaler Konsens. Osteoporose Int 28: 1-19.
- Palmieri S, Roggero L, Cairoli E, Morelli V, Scillitani A, et al. (2017) Auftreten von malignen Neoplasien bei Patienten mit primärem Hyperparathyreoidismus. Eur J Intern Med 43: 77-82.
- Norman J, Lopez J, Politz D (2012) Verzicht auf einseitige parathyroidectomy: warum wir kehrten unsere position nach 15.000 Nebenschilddrüsen-Operationen., J Am Coll Surg 214: 260-259.
- Norman J, Politz D (2010) Die prospektive Studie bei 3.000 aufeinanderfolgenden Nebenschilddrüsenoperationen zeigt 18 objektive Faktoren, die die Entscheidung für einen einseitigen versus bilateralen chirurgischen Ansatz beeinflussen. J Am Coll Surg 211: 244-249.
- Norman J, Politz D (2009) 5.000 Nebenschilddrüsenoperationen ohne eingefrorenen Abschnitt oder PTH-Assays: Messung der individuellen Nebenschilddrüsenhormonproduktion in Echtzeit. Ann Surg Oncol 16: 656-666.,
- Beatriz de Rienzo-Madero (2017) Die Rückkehr des bilateral neck exploration für primären Hyperparathyreoidismus. Die Medizinische Wissenschaft, 21: 305-316.
- Norman J, Chheda H, Farrell C (1998) Minimalinvasive Parathyreoidektomie bei primärem Hyperparathyreoidismus: Verringerung der Operationszeit und möglicher Komplikationen bei gleichzeitiger Verbesserung der kosmetischen Ergebnisse. Am Surg 64: 391-395.
- Costello D, Norman J (1999) Minimal-invasive radioguided parathyroidectomy. Surg Oncol Clin N Am 8: 555-564.,
- Murphy C, Norman J (1999) Die 20% regel: eine einfache, sofortige radioaktivität messung definiert heilung und ermöglicht beseitigung von gefrorenen abschnitte und hormon assays während parathyroidektomie. Surgery 126: 1023-1028.
- Flynn MB, Bumpous JM, Schill K, McMasters KM (2000) Minimal-invasive radioguided parathyroidectomy. J Am Coll Surg 191: 24-31.,
- Carter AB, Howanitz PJ (2003) Intraoperative Tests für Parathormon: eine umfassende überprüfung der Verwendung des Assays und der einschlägigen Literatur. Arch Pathol Lab Med 127: 1424-1442.
- Helsinki (2004) Ethische Grundsätze für die medizinische Forschung an menschlichen Probanden.
- Fraser WD (2009) Hyperparathyreoidismus. Lancet 374: S. 145-158.
- Beard CM, Heide H, O ‚ Fallon WM, Anderson JA, Earle JD, et al., (1989) Therapeutic radiation and hyperparathyroidism. A case-control study in Rochester, Minn. Arch Intern Med 149: 1887-1890.
- Fujiwara S, Sposto R, Ezaki H, Akiba S, Neriishi K, et al. (1992) Hyperparathyroidism among atomic bomb survivors in Hiroshima. Radiat Res 130: 372-378.
- Arnold A, Shattuck TM, Mallya SM, Krebs LJ, Costa J, et al. (2002) Molecular pathogenesis of primary hyperparathyroidism. J Bone Miner Res 17: 30-36.,
- Arnold A, Staunton CE, Kim HG, Gaz RD, Kronenberg HM (1988) Monoclonality and abnormal parathyroid hormone genes in parathyroid adenomas. N Engl J Med 318: 658-662.
- Thakker RV, Newey PJ, Walls GV, Bilezikian J, Dralle H, et al. (2012) Clinical practice guidelines for multiple endocrine neoplasia type 1 (MEN1). J Clin Endocrinol Metab 97: 2990-3011.,
- Calmettes C, Ponder BA, Fischer JA, Raue F (1992) eine Frühzeitige Diagnose der multiplen endokrinen Neoplasie Typ-2-Syndrom: consensus statement. Konzertierte Aktion der Europäischen Gemeinschaft: Medulläres Schilddrüsenkarzinom. Eur J Clin Invest 22: 755-760.
- Hannan FM, Nesbit MA, Christie PT, Fratter C, Dudley NE, et al. (2008) Familiärer isolierter primärer Hyperparathyreoidismus, verursacht durch Mutationen des MEN1-Gens. Nat Clin Pract Endocrinol Metab 4: 53-58.,
- Simonds WF, Robbins CM, Agarwal SK, Hendy GN, Carpten JD, et al. (2004) Familiärer isolierter Hyperparathyreoidismus wird selten durch Keimbahnmutation in HRPT2, dem Gen für das Hyperparathyreoidismus-Kiefer-Tumor-Syndrom, verursacht. J Clin Endocrinol Metab 89: 96-102E.
- Perrier ND (2005) Asymptomatischer Hyperparathyreoidismus: eine medizinische Etikettenschwindel? Chirurgie 137: 127-131.
- Albright F, Walter Bauer, Jessie Reed Cockrill, Lesen Ellsworth (1931) Untersuchungen über die Physiologie der Nebenschilddrüsen: II., Die Beziehung des Serumcalciums zum Serumphosphor auf verschiedenen Ebenen der Nebenschilddrüsenaktivität. J Clin Invest 9: 659-677.
- Albright F, Walter Bauer, Jessie Reed Cockrill, Lesen Ellsworth (1932) Studies In Nebenschilddrüsen Physiologie: Iii. Die Wirkung von Phosphat Einnahme in Klinischen Hyperparathyreoidismus. J Clin Invest 11: 411-435.
- Vaishava H, Rizvi SN (1969) Primärer Hyperparathyreoidismus im Zusammenhang mit Ernährungs-Osteomalazie. Am J Med 46: 640-644.,
- Chapuy MC, Preziosi P, Maamer M, Arnaud S, Galan P, et al. (1997) Prävalenz von Vitamin-D-Insuffizienz in einer erwachsenen Normalbevölkerung. Osteoporose Int 7: 439-443.
- Kantorovich V, Gacad MA, Seeger LL, Adams JS (2000) Die Knochenmineraldichte steigt bei Patienten mit koexistierender Vitamin-D-Insuffizienz und primärem Hyperparathyreoidismus mit Vitamin D-Repletion. J Clin Endocrinol Metab 85: 3541-3543.
- Silverberg SJ (2007) Vitamin-D-Mangel und der primäre Hyperparathyreoidismus., J Bone Miner Res 2: 100-104.
- Rao DS, Honasoge M, Göttliche GW, Phillips ÄH, Lee MW, et al. (2000) Wirkung der Vitamin-D-Ernährung auf das Parathyroidadenomgewicht: pathogenetische und klinische Implikationen. J Clin Endocrinol Metab 85: 1054-1058.
- Grau A, Lucas J, Horne A, Gamble G, Davidson JS, et al. (2005) Vitamin-D-Repletion bei Patienten mit primärem Hyperparathyreoidismus und koexistierender Vitamin-D-Insuffizienz. J Clin Endocrinol Metab 90: 2122-2126.,
- Tucci JR (2009) Vitamin D-Therapie bei Patienten mit primärem Hyperparathyreoidismus und Hypovitaminose D. Eur J Endocrinol 161: 189-193.
- Silverberg SJ, Shane E, Dempster DW, Bilezikian JP (1999) Die Auswirkungen von vitamin-D-Insuffizienz bei Patienten mit primärem Hyperparathyreoidismus. Am J Med 107: 561-567.
- Grubbs EG, Rafeeq S, Jimenez C, Feng L, Lee JE, et al. (2008) Präoperative Vitamin-D-Ersatztherapie bei primärem Hyperparathyreoidismus: sicher und vorteilhaft?, Chirurgie 144: 852-858.
- Isidro ML, B Ruano (2009) Biochemische Wirkungen der Calcifediol-Supplementierung bei mildem, asymptomatischem Hyperparathyreoidismus mit gleichzeitigem Vitamin-D-Mangel. Endokrine 36: 305-310.
- Shah VN, Shah CS, Bhadada SK, Rao DS (2014) Wirkung von 25 (OH) D-Ersatz bei Patienten mit primärem Hyperparathyreoidismus (PHPT) und gleichzeitig vorhandenem vitamin-D-Mangel auf die serum-25(OH) D -, calcium-und PTH: eine meta-Analyse und überprüfung der Literatur. Clin Endocrinol (Oxf) 80: 797-803.,
- Bilezikian JP, Khan AA, Potts JT Jr (2009) Leitlinien für das management der asymptomatischen primären Hyperparathyreoidismus: Zusammenfassung von der Dritten internationalen workshop. J Clin Endocrinol Metab 94: 335-339.