al estudiar las relaciones entre genotipo y fenotipo, es importante examinar la ocurrencia estadística de fenotipos en un grupo de genotipos conocidos., En otras palabras, dado un grupo de genotipos conocidos para un rasgo, ¿cuántos genotipos idénticos muestran el fenotipo relacionado? Es posible que se sorprenda al saber que, para algunos rasgos, el fenotipo puede no ocurrir tan a menudo como el genotipo. Por ejemplo, digamos que todos en la población w tienen las mismas combinaciones de alelos para un determinado rasgo, sin embargo, solo el 85% de la población realmente muestra el fenotipo esperado de esas combinaciones de alelos. La proporción de genotipos que realmente muestran fenotipos esperados se llama penetrancia. Así, en el ejemplo anterior, la penetrancia es del 85%., Este valor se calcula a partir de observar poblaciones cuyos genotipos conocemos.
de hecho, grandes estudios de población son necesarios para medir la penetrancia, y los estudios de penetrancia nos ayudan a predecir la probabilidad de que un rasgo sea evidente en aquellos que portan los alelos subyacentes. En general, cuando sabemos que el genotipo está presente pero el fenotipo no es observable, el rasgo muestra penetrancia incompleta. Básicamente, cualquier cosa que muestre menos del 100% de penetrancia es un ejemplo de penetrancia incompleta., Por lo tanto, aunque la penetrancia de un rasgo es un valor estadísticamente calculado basado en la aparición de un fenotipo entre genotipos conocidos, la penetrancia incompleta es simplemente una descripción cualitativa sobre un grupo de genotipos conocidos.
un ejemplo específico de penetrancia incompleta es la enfermedad ósea humana osteogénesis imperfecta (OI). La mayoría de las personas con esta enfermedad tienen una mutación dominante en uno de los dos genes que producen colágeno tipo 1, COL1A1 o COL1A2. El colágeno es un tejido que fortalece los huesos y los músculos y múltiples tejidos corporales., Las personas con OI tienen huesos débiles, color azulado en el blanco de sus ojos y una variedad de afecciones que causan debilidad en sus articulaciones y dientes. Sin embargo, esta enfermedad no afecta a todas las personas que tienen mutaciones en COLIA1 y COLIA2 de la misma manera. De hecho, algunas personas pueden portar la mutación pero no tienen síntomas. Por lo tanto, las familias pueden transmitir sin saberlo la mutación de una generación a la siguiente a través de alguien que lleva la mutación pero no expresa el fenotipo OI.,
ejemplos de penetrancia incompleta como OI demuestran que incluso las enfermedades monogénicas no tienen patrones de expresión predecibles en una población. ¿Hay alguna manera de explicar esta imprevisibilidad? Pensémoslo. Si dos personas tienen la misma mutación dominante en COL1A1, ¿por qué solo una de ellas podría mostrar síntomas de OI? ¿Podría tener que ver con otros genes que rescatan el mal efecto de un gen de colágeno mutado? ¿Podría ser que aquellos que tienen OI simplemente expresen más colágeno mutado que la persona que no se ve afectada?, Para considerar las posibles explicaciones para la penetrancia incompleta, tenemos que recordar cuántos pasos hay entre la transcripción de genes y la expresión de proteínas.
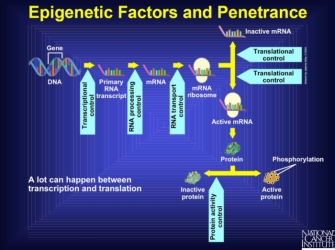
tenga en cuenta que la expresión de otros genes, como los reguladores transcripcionales o translacionales, puede influir en el efecto final de un producto genético. Cualquier cosa que interfiera con la vía de la transcripción a la activación de proteínas se conoce como un factor epigenético. De hecho, hay múltiples puntos en los que otro producto genético puede intervenir en las etapas previas a la producción de una proteína., La interferencia en estas etapas podría detener la producción por completo, crear una forma alterada de la proteína que nunca podría ser activa, o hacer cualquier número de otras cosas que hace que el gen silencioso. Por lo tanto, la etapa final de una proteína activa refleja muchos procesos diferentes que conducen a la secuencia de aminoácidos y la forma final de la proteína, todos los cuales pueden ser interferidos por otros genes. Además, algunos genes pueden regular al alza o a la baja las tasas de transcripción, lo que cambia la cantidad total de proteína producida., Así, los genes que afectan la forma final y la cantidad de expresión de otro gen pueden influir en la formación del fenotipo derivado del gen regulado (Figura 1).
entonces, si existen tantos puntos de modificación posibles para un producto genético, ¿cómo podemos reducir la pregunta de qué causa la penetrancia incompleta? Curiosamente, algunos científicos han intentado hacer esto observando cómo las mutaciones genéticas que causan OI afectan a los ratones. Estos investigadores insertaron una forma mutada de COL1A1 en ratones y los criaron para que todos contuvieran esta mutación., Los ratones se vieron afectados de manera similar a aquellos con OI humana: muchos tenían debilidad ósea severa y fracturas óseas múltiples, incluso al nacer. De hecho, cuando los investigadores examinaron los huesos de ratón de cerca, encontraron que el 70% de los ratones con el gen COL1A1 mutado mostraron evidencia de OI (fracturas óseas); sin embargo, el 30% restante parecía completamente normal. En estos ratones sin fenotipo OI, hubo la misma cantidad de expresión de COL1A1 que en aquellos ratones que sí mostraron el fenotipo., Además, los investigadores utilizaron una cepa pura de ratones que tenía poca variabilidad en sus genomas para empezar. Esto significa que el contexto genético en el que se expresó COL1A1 no varió entre los ratones estudiados. Sin embargo, a pesar de que todos los ratones tenían genomas extremadamente similares y todos expresaban la misma cantidad de COL1A1, el 30% de ellos no mostró ningún fenotipo de OI. Estos resultados siguen siendo desconcertantes.
por lo tanto, incluso las poderosas técnicas experimentales disponibles actualmente no pueden explicar la penetrancia., Las dos explicaciones más populares para la penetrancia incompleta, el fondo genético y los niveles de expresión variables, no explicaron la falta de fenotipo en el 30% de los ratones (Pereira et al., 1994).