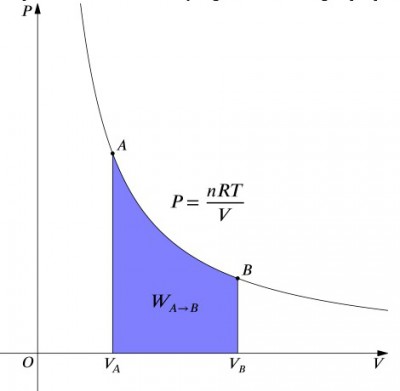
Paine-tilavuus-kaavio on isoterminen prosessi.
Isoterminen viittaa prosessiin, jossa järjestelmä muuttuu—onko se olla paine, tilavuus ja/tai sisältö—ilman lämpötila muuttuvat. Tästä näkökulmasta ensimmäinen laki termodynamiikan, tämä tarkoittaa, että sisäinen energia järjestelmä ei muutu, koska lämpötila on mitta keskimääräinen kineettinen energia molekyylejä järjestelmän sisällä., Tämä sitten näyttää:
ja siten,
missä:
- on sisäisen energian muutos
- on lämpöä
- työ
Mitä nämä yhtälöt siis on, että työn tulo-järjestelmän on oltava täysin tasapainossa lämmöntuotto, ja päinvastoin. Jos eristetty astia, jossa ilma on pakattu (vähentää sen määrää, positiivinen arvo), niin lämpö on poistettava järjestelmästä mukaisesti (negatiivinen arvo). Sen sijaan jos säiliön annetaan laajentua (negatiivinen), lämpö on lisättävä järjestelmään, jotta lämpötila pysyy vakiona., Työn laskemiseksi kaavalle on tehtävä integraatio . Tämän voidaan ajatella myös laskevan käyrän alla olevaa aluetta. Käyrän muodon vuoksi se ei kuitenkaan ole yhtä yksinkertainen laskelma—esimerkiksi isobaariseen prosessiin verrattuna., Alla oleva kaava on integroitu yhtälö, ja laskee työ tahansa isoterminen prosessi:
missä:
- on määrä myyrät
- on ihanteellinen kaasuvakio
- on alkuperäinen paine
- on lopullinen tilavuus
Carnot-hyötysuhde selittää, suurin terminen hyötysuhde lämmön moottori on johdettu käyttämällä isoterminen prosesseja, joissa termodynaaminen sykli on valmis käyttöön 2 isoterminen ja 2 adiabaattinen prosessit., Vaihe muutokset ovat esimerkki isoterminen prosesseja, koska lämpötila pysyy vakiona, kunnes vaiheen muutos on täydellinen.
UC Berkleyn kemian osaston seuraava video selittää ideaa isotermisestä prosessista visuaalisuudella.