Bei der Untersuchung der Beziehungen zwischen Genotyp und Phänotyp ist es wichtig, das statistische Auftreten von Phänotypen in einer Gruppe bekannter Genotypen zu untersuchen., Mit anderen Worten, wie viele identische Genotypen zeigen bei einer Gruppe bekannter Genotypen für ein Merkmal den verwandten Phänotyp? Sie werden überrascht sein zu erfahren, dass der Phänotyp bei einigen Merkmalen möglicherweise nicht so häufig auftritt wie der Genotyp. Angenommen, jeder in Population W trägt die gleichen Allelkombinationen für ein bestimmtes Merkmal, zeigt jedoch nur 85% der Population tatsächlich den Phänotyp, der von diesen Allelkombinationen erwartet wird. Der Anteil der Genotypen, die tatsächlich erwartete Phänotypen zeigen, wird Penetranz genannt. Somit beträgt im vorhergehenden Beispiel die Penetranz 85%., Dieser Wert wird aus der Betrachtung von Populationen berechnet, deren Genotypen wir kennen.
In der Tat sind große Populationsstudien notwendig, um die Penetranz zu messen, und Penetranzstudien helfen uns vorherzusagen, wie wahrscheinlich es ist, dass ein Merkmal bei denen offensichtlich wird, die die zugrunde liegenden Allele tragen. Wenn wir wissen, dass der Genotyp vorhanden ist, der Phänotyp jedoch nicht beobachtet werden kann, zeigt das Merkmal im Allgemeinen eine unvollständige Penetranz. Grundsätzlich ist alles, was weniger als 100% Penetranz zeigt, ein Beispiel für unvollständige Penetranz., Obwohl die Penetranz eines Merkmals ein statistisch berechneter Wert ist, der auf dem Auftreten eines Phänotyps unter bekannten Genotypen basiert, ist die unvollständige Penetranz daher einfach eine qualitative Beschreibung einer Gruppe bekannter Genotypen.
Ein spezifisches Beispiel für unvollständige Penetranz ist die menschliche Knochenerkrankung osteogenesis imperfecta (OI). Die Mehrheit der Menschen mit dieser Krankheit hat eine dominante Mutation in einem der beiden Gene, die Kollagen vom Typ 1, COL1A1 oder COL1A2, produzieren. Kollagen ist ein Gewebe, das Knochen und Muskeln sowie mehrere Körpergewebe stärkt., Menschen mit OI haben schwache Knochen, bläuliche Farbe im Weiß ihrer Augen und eine Vielzahl von Beschwerden, die Schwäche in ihren Gelenken und Zähnen verursachen. Diese Krankheit betrifft jedoch nicht alle, die COLIA1-und COLIA2-Mutationen haben, auf die gleiche Weise. Tatsächlich können einige Menschen die Mutation tragen, haben aber keine Symptome. So können Familien die Mutation unwissentlich von einer Generation zur nächsten durch jemanden übertragen, der die Mutation trägt, aber den OI-Phänotyp nicht ausdrückt.,
Unvollständige Penetranzbeispiele wie OI zeigen, dass selbst monogene Erkrankungen in einer Population keine vorhersehbaren Expressionsmuster aufweisen. Gibt es eine Möglichkeit, diese Unvorhersehbarkeit zu erklären? Lass uns darüber nachdenken. Wenn zwei Personen die gleiche dominante Mutation in COL1A1 haben, warum zeigt dann möglicherweise nur eine von ihnen tatsächlich OI-Symptome? Könnte es mit anderen Genen zu tun haben, die die schlechte Wirkung eines mutierten Kollagengens retten? Könnte es sein, dass diejenigen, die OI haben, einfach mehr mutiertes Kollagen ausdrücken als die Person, die nicht betroffen ist?, Um die möglichen Erklärungen für eine unvollständige Penetranz zu berücksichtigen, müssen wir uns daran erinnern, wie viele Schritte zwischen Gentranskription und Proteinexpression bestehen.
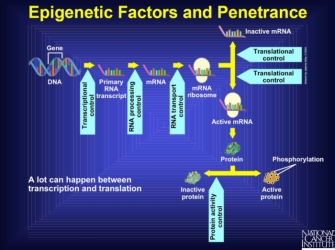
Beachten Sie, dass die Expression anderer Gene, wie Transkriptions-oder Translationsregulatoren, die endgültige Wirkung eines Genprodukts beeinflussen kann. Alles, was den Weg von der Transkription zur Proteinaktivierung stört, wird als epigenetischer Faktor bezeichnet. In der Tat gibt es mehrere Punkte, an denen ein anderes Genprodukt in die Stadien vor der Produktion eines Proteins eingreifen kann., Störungen in diesen Stadien können die Produktion vollständig stoppen, eine veränderte Form des Proteins erzeugen, die möglicherweise nie aktiv ist, oder eine Reihe anderer Dinge tun, die das Gen zum Schweigen bringen. Das Endstadium eines aktiven Proteins spiegelt also viele verschiedene Prozesse wider, die zur Aminosäuresequenz und endgültigen Proteinform führen, die alle von anderen Genen gestört werden können. Darüber hinaus können einige Gene die Transkriptionsraten nach oben oder unten regulieren, wodurch sich die Gesamtmenge des produzierten Proteins ändert., Somit können Gene, die die endgültige Form und Expressionsmenge eines anderen Gens beeinflussen, Einfluss auf die Bildung des vom regulierten Gen abgeleiteten Phänotyps haben (Abbildung 1).
Wenn also so viele verschiedene mögliche Modifikationspunkte für ein Genprodukt existieren, wie können wir dann die Frage eingrenzen, was unvollständige Penetranz verursacht? Interessanterweise haben einige Wissenschaftler tatsächlich versucht, dies zu tun, indem sie beobachtet haben, wie sich die genetischen Mutationen, die OI verursachen, auf Mäuse auswirken. Diese Forscher fügten eine mutierte Form von COL1A1 in Mäuse ein und züchteten sie so, dass sie alle diese Mutation enthielten., Die Mäuse waren auf ähnliche Weise betroffen wie Menschen mit menschlicher OI: Viele hatten schwere Knochenschwäche und mehrere Knochenbrüche, sogar bei der Geburt. Als die Forscher die Mausknochen genau untersuchten, stellten sie fest, dass 70% der Mäuse mit dem mutierten COL1A1-Gen Hinweise auf OI (Knochenbrüche) zeigten; Die restlichen 30% erschienen jedoch völlig normal. Bei diesen Mäusen ohne OI-Phänotyp gab es die gleiche Menge an COL1A1-Expression wie bei jenen Mäusen, die den Phänotyp zeigten., Darüber hinaus verwendeten die Forscher einen reinrassigen Stamm von Mäusen, der zunächst wenig Variabilität in ihren Genomen aufwies. Dies bedeutet, dass der genetische Kontext, in dem COL1A1 exprimiert wurde, bei den untersuchten Mäusen nicht variierte. Trotz der Tatsache, dass alle Mäuse extrem ähnliche Genome hatten und alle die gleiche Menge an COL1A1 exprimierten, zeigten 30% von ihnen keinen OI-Phänotyp. Diese Ergebnisse sind weiterhin verwirrend.
Daher können selbst die derzeit verfügbaren leistungsstarken experimentellen Techniken die Penetranz nicht erklären., Die beiden populärsten Erklärungen für unvollständige Penetranz, genetischer Hintergrund und variable Expressionsniveaus, erklärten nicht das Fehlen eines Phänotyps bei 30% der Mäuse (Pereira et al., 1994).