3) cationi adiacenți unui atom cu electoni de pereche singuri.deoarece heteroatomii, cum ar fi oxigenul și azotul, sunt mai electronegativi decât carbonul, s-ar putea să vă așteptați ca, prin definiție, să fie grupuri de retragere a electronilor care destabilizează carbocațiile. De fapt, opusul este adesea adevărat: dacă atomul de oxigen sau azot este în poziția corectă, efectul general este stabilizarea carbocării., Acest lucru se datorează faptului că, deși aceste heteroatome sunt grupuri de retragere a electronilor prin inducție, ele sunt grupuri de donare a electronilor prin rezonanță, iar acest efect de rezonanță este mai puternic. (Am întâlnit anterior aceeași idee atunci când se analizează aciditatea relativă și bazicitatea fenolilor și aminelor aromatice în secțiunea 7.4)., Luați în considerare două perechi de carbocationul specii de mai jos:
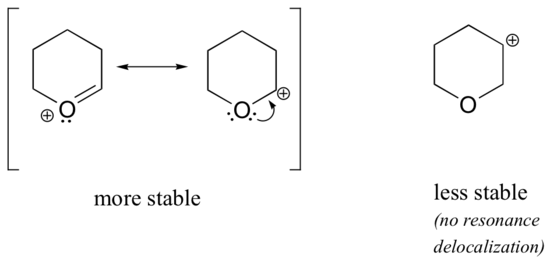
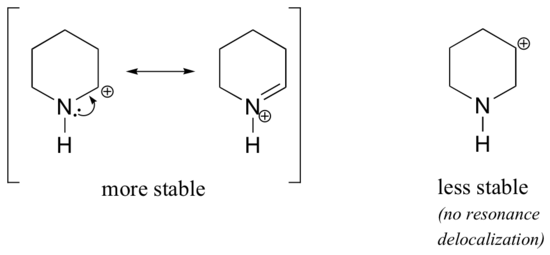
În mai stabil carbocations, la heteroatom acționează ca un electron donarea grup de rezonanță: în vigoare, lone pereche pe heteroatom este disponibil pentru delocalize sarcina pozitivă. În carbocațiile mai puțin stabile, carbonul încărcat pozitiv este la mai mult de o legătură distanță de heteroatom și, prin urmare, nu sunt posibile efecte de rezonanță., De fapt, în aceste specii de carbocație, heteroatomii destabilizează de fapt sarcina pozitivă, deoarece se retrag electroni prin inducție