3) Kationen, die an ein Atom mit einsamen Paarelektronen angrenzen.
Da Heteroatome wie Sauerstoff und Stickstoff elektronegativer sind als Kohlenstoff, könnte man erwarten, dass sie per Definition elektronentziehende Gruppen wären, die Carbokationen destabilisieren. In der Tat ist oft das Gegenteil der Fall: Wenn sich das Sauerstoff-oder Stickstoffatom in der richtigen Position befindet, ist der Gesamteffekt die Carbokationsstabilisierung., Dies ist auf die Tatsache zurückzuführen, dass diese Heteroatome zwar durch Induktion elektronentragende Gruppen sind, aber durch Resonanz elektronenspendende Gruppen sind, und es ist dieser Resonanzeffekt, der stärker ist. (Wir sind zuvor auf dieselbe Idee gestoßen, als wir die relative Acidität und Basizität von Phenolen und aromatischen Aminen in Abschnitt 7.4 betrachteten.), Betrachten Sie die beiden folgenden Paare von Carbokationsspezies:
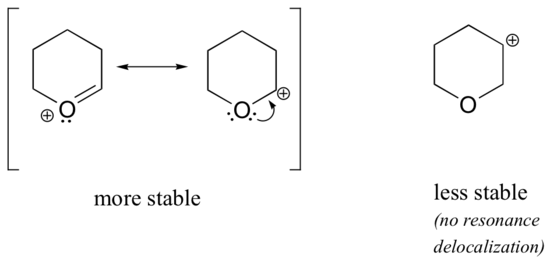
In den stabileren Carbokationen wirkt das Heteroatom als Elektronenspendergruppe durch Resonanz: In der Tat wirkt das einsame Paar auf dem Heteroatom durch Resonanz ist verfügbar, um die positive Ladung zu delokalisieren. In den weniger stabilen Carbokationen ist der positiv geladene Kohlenstoff mehr als eine Bindung vom Heteroatom entfernt, und somit sind keine Resonanzeffekte möglich., Tatsächlich destabilisieren die Heteroatome bei diesen Carbocation-Spezies tatsächlich die positive Ladung, weil sie Elektronen sind, die sich durch Induktion zurückziehen