co je konečník?
konečník je na konci tlustého střeva a má délku asi 5 palců. Konečník je obvykle prázdný, s výjimkou případů, kdy stolice pochází z horního tlustého střeva do konečníku těsně před pohybem střev. V té době je stolice připravena k vylučování análním kanálem. Anální kanál má dva svalové „ventily“, nazývané vnitřní a vnější svěrače. Stolice prochází těmito svěrači. Svěrače nám umožňují udržet stolici, dokud nebudeme připraveni na pohyb střev., V tomto okamžiku se svěrače uvolňují a uvolňují stoličku.
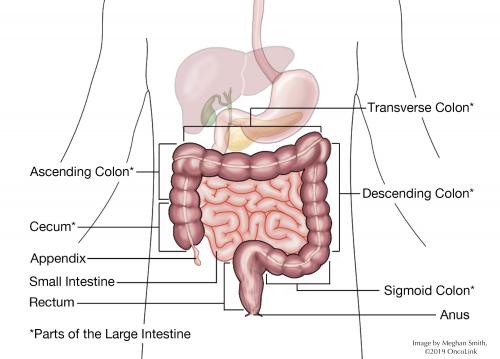
co je rakovina konečníku?
rakovina konečníku je maligní (rakovinná) tkáň, která roste ve stěně konečníku. Nádory často začínají, když normální tkáň ve stěně konečníku tvoří adenomatózní polyp nebo prekancerózní růst, rostoucí na podšívce rektální stěny. Jak se tento polyp zvětšuje, vzniká nádor. Tento proces může trvat mnoho let, což umožňuje čas na včasnou detekci pomocí screeningových testů. Většina rakoviny konečníku je typ rakoviny nazývaný adenokarcinom.,
co způsobuje rakovinu konečníku a jsem ohrožen?
každý rok se odhaduje, že ve Spojených státech bude diagnostikováno asi 44 180 nových případů rakoviny konečníku. Má tendenci se vyskytovat více u mužů než u žen. Rakoviny tlustého střeva a konečníku jsou často seskupeny a mají stejné rizikové faktory. Průměrný věk diagnózy je 66 let a riziko se zvyšuje s věkem. Jedinci s osobní nebo rodinnou anamnézou kolorektálního karcinomu nebo polypů, zděděné syndromy kolorektálního karcinomu (tj.,, Familiární adenomatózní polypóza (FAP) a dědičná Non polypóza kolorektální karcinom (HNPCC) a pacienti s ulcerózní kolitidou nebo Crohnovou chorobou jsou vystaveni vyššímu riziku. Tito pacienti mohou vyžadovat screening v mladším věku než běžná populace. Osoba s jedním příbuzným prvního stupně (rodič, sourozenec nebo dítě) s rakovinou tlustého střeva je 2 až 3krát vyšší pravděpodobnost vzniku rakoviny jako někdo, kdo nemá postiženého příbuzného. To však neznamená, že lidé bez rodinné historie nejsou ohroženi., Asi 80% nových případů kolorektálního karcinomu je diagnostikováno u lidí, kteří by nebyli identifikováni jako „vysoké riziko.“
studie případů kolorektálního karcinomu zjistily, že určité faktory životního stylu mohou člověka vystavit vyššímu riziku. Mezi tyto faktory patří:
- strava s vysokým obsahem tuku a červeného masa.
- dieta s nízkým obsahem ovoce a zeleniny.
- vysoký kalorický příjem.
- nízké hladiny fyzické aktivity.
- obezita.
kromě toho může kouření a nadměrný příjem alkoholu hrát roli ve vývoji kolorektálního karcinomu.,
navzdory vyhýbání se všem těmto faktorům se u některých lidí stále vyvine rakovina tlustého střeva nebo konečníku. Při screeningu a včasné detekci mohou být tito pacienti ve většině případů vyléčeni.
Jak mohu zabránit rakovině konečníku?
Vzhledem k tomu, rizikové faktory uvedené výše, nízkotučné diety, vysokým obsahem ovoce a zeleniny a nízkým obsahem červeného masa, pravidelné cvičení a udržování zdravé tělesné hmotnosti může pomoci zabránit tlustého střeva nebo rakovina konečníku. Měli byste se také vyhnout kouření a nadměrnému příjmu alkoholu.,
termín “ chemoprevence „lze definovat jako“ použití chemické sloučeniny k prevenci, inhibici nebo zvrácení tvorby rakoviny.“Existují studie, při pohledu na vitamíny A, E, D, a, C, kyselina listová, vápník, selen, kyselina acetylsalicylová, inhibitory cox-2, a hormonální substituční terapie jako potenciální chemopreventivní látky, které mohou zabránit nebo zvrátit vznik polypů a kolorektálního karcinomu. Tyto studie byly neprůkazné a pro obecnou populaci nebyla učiněna žádná konkrétní doporučení. Některé z těchto látek jsou i nadále testovány v klinických studiích.,
jaké screeningové testy se používají pro rakovinu konečníku?
jeden screeningový test, který je specifický pro rakovinu konečníku, je digitální rektální vyšetření (DRE). Během DRE poskytovatel vloží prst v rukavici do konečníku pacienta a cítí se pro abnormální výrůstky nebo zúžení (zúžení). Studie neprokázaly, že screening s DRE skutečně snižuje úmrtí v důsledku rakoviny konečníku. Jiné screeningové testy jsou stejné jako ty, které se používají pro screening rakoviny tlustého střeva, včetně fekálních okultních krevních testů, kolonoskopie a sigmoidoskopie. Tyto testy zobrazují jak tlusté střevo, tak konečník.,
Některé nádory a polypy mohou krvácet, a tato krev může být detekována ve vzorcích stolice, zkušební nazývá fekální okultní krevní testy (FOBT). Samotný tok může najít pouze asi 24% rakovin. Americká společnost pro rakovinu doporučuje, aby FOBT byl prováděn každý rok spolu s flexibilní sigmoidoskopií každých 5 let po věku 50 let. Tyto dva testy detekují asi 76% kolorektálních nádorů. Sigmoidoskop je štíhlá, flexibilní trubice, která má schopnost prohlížet konečník a nejnižší část tlustého střeva., Pokud se při tomto testu objeví polyp nebo nádor, bude pacient odkázán na úplnou kolonoskopii.
kolonoskopem, který je používán během kolonoskopie, je podobný sigmoidoscope, ale je delší a může zobrazit celý konečníku a tlustého střeva. Pokud je nalezen polyp, lékař jej může odstranit a odeslat do patologické laboratoře, aby zjistil, zda je adenomatózní (rakovinný). Americká rakovinová společnost doporučuje, aby kolonoskopie byla prováděna každých 10 let po věku 50 let. Pacienti s rodinnou nebo osobní historií by měli mít častější projekce., Ty by měly začít ve věku, který je o deset let mladší, než byl jejich příbuzný v diagnóze. Pacienti s anamnézou ulcerózní kolitidy jsou také vystaveni zvýšenému riziku a měli by mít častější screening než široká veřejnost. Pacienti by měli mluvit se svým pečovatelským týmem o tom, která metoda screeningu je pro ně nejlepší a jak často by měla být provedena.
Další screeningové testy, které mohou detekovat rakovinu, zahrnují fekální immuochemický test (FIT) a testy DNA stolice (Cologuard®)., Tyto testy nabízejí pohodlí domácího testování a minimální přípravu před testem, ale nemusí detekovat všechny nádory a nemusí být pokryty pojištěním. Tyto testy by měly používat pouze osoby s nízkým rizikem kolorektálního karcinomu a pod vedením poskytovatele zdravotní péče.
jaké jsou příznaky rakoviny konečníku?
Na rozdíl od rakoviny tlustého střeva způsobuje většina rakovin konečníku příznaky., Patří mezi ně: červená krev vidět ve stolici, nevysvětlitelné zácpa střídající se s průjmem, změny v průměru stolice (pacienti si všimnout, „tužka-tenké stolice“), a tenezmy, což je pocit nutkání mít pohyb střev, když nechcete a/nebo neschopnost vyprázdnit konečník. Pokud jsou nádory pokročilejší, mohou napadnout okolní tkáně a způsobit inkontinenci močového měchýře (neschopnost udržet moč) nebo bolest v důsledku tlaku v hýždích nebo perineu.
jak je diagnostikována rakovina konečníku?,
jakmile screeningové testy zjistí rakovinu konečníku, jsou zapotřebí další testy k určení rozsahu nádoru. Testy používané k určení šíření nádoru jsou CT vyšetření, MRI a endoskopický ultrazvuk (EUS). EUS je typ ultrazvuku, který používá zvukové vlny k určení hloubky nádoru a zda se jedná o okolní lymfatické uzliny. Biopsie se obvykle provádí v průběhu EUS, kolonoskopie nebo proctoscopy (test, který pouze názory rektální oblasti), který umožňuje poskytovateli péče, určit typ nádoru., Hladina karcinoembryonálního antigenu (CEA) je markerem kolorektálního karcinomu, který se nachází v krvi a je zvýšen v 95% případů. Ženy s pokročilými nádory by také měly mít pánevní vyšetření, aby zjistily, zda nádor napadl do vagíny nebo děložního čípku.
kromě výše uvedených testů může být vzorek nádoru odeslán do patologické laboratoře. To lze provést biopsickým vzorkem nebo větším vzorkem, který se během operace odstraní., Patolog připraví zprávu o patologii, což je písemná zpráva, která vám poskytne více podrobností o typu nádoru, velikosti a jakýchkoli změnách specifických pro váš nádor. Patologie nejčastěji odhaluje adenokarcinom.
tkáň z biopsie by měla být zkontrolována na mutace čtyř genů neodpovídajících oprav (MMR) a mikrosatelitové nestability (MSI). To by mělo být provedeno ve všech stádiích kolorektálního karcinomu. Geny MMR zahrnují msh2, MLH1, MSH6 a PSM2. Abnormality s testováním MMR mohou naznačovat, že k nádoru došlo v důsledku dědičného rakovinového syndromu., Mikrosatelitů změny se vyskytují v sekvenování DNA v nádorových buňkách nebo v nemožnosti opravit chyby při DNA se zkopíruje do buňky. Když k tomu dojde, nazývá se mikrosatelitová nestabilita (MSI). MSI lze klasifikovat jako MSI high (MSI-H), Microsatelite stable (MSS) nebo MSI low (MSI-L). Tyto informace mohou pomoci při léčbě. Pacienti s metastatickým kolorektálním karcinomem by měli mít také genotyp nádorové tkáně pro mutace RAS, které zahrnují mutace KRAS, NRAS a BRAF. Tyto výsledky mohou pomoci rozhodnout o možnostech léčby.
jak probíhá rakovina konečníku?,
Staging pomáhá určit, jak daleko rakovina rostla a zda se rozšířila do jiných orgánů nebo lymfatických uzlin. Pomocí výše uvedených testů je stanovena fáze výběru nejlepších možností léčby. Systém TNM (také nazývaný systém nádorových uzlin – metastáz) popisuje velikost nádoru (T), pokud se jedná o lymfatické uzliny (N) A pokud se rozšířil do dalších oblastí těla (M). Dále může být kolorektální karcinom klasifikován jako nízký stupeň nebo vysoký stupeň. Grade se zaměřuje na to, jak odlišné rakovinné buňky vypadají z normální buňky., Vysoce kvalitní rakoviny mají tendenci růst a šířit se rychleji.
staging systém je velmi složitý, a celý pracovní systém, je uvedeno na konci tohoto článku. Ačkoli komplikovaný, systém staging pomáhá poskytovatelům zdravotní péče určit rozsah rakoviny, a na oplátku, rozhodovat o léčbě rakoviny pacienta. Stupeň rakoviny, nebo rozsah onemocnění, je založen na informacích shromážděných prostřednictvím různých testů provedených při diagnostice a zpracování rakoviny.
jak se léčí rakovina konečníku?,
chirurgie
V posledních několika letech došlo k významnému zlepšení chirurgických technik pro léčbu rakoviny konečníku. V minulosti, většina pacientů vyžaduje kolostomie po rektální operaci rakoviny a má významné nežádoucí účinky (jako je inkontinence a mužské impotence) z poškození nervů, které často došlo během operace. Využití předoperační chemoradiation (kombinace chemoterapie a záření) a zlepšení operačních technik vedlo k méně vedlejších účinků a méně pacientů vyžadující kolostomii., Navíc předoperační chemoterapie & záření (nazývané neoadjuvantní terapie) může zlepšit úspěšnost úplného odstranění nádoru.
chirurgie je nejčastější léčbou rakoviny konečníku. Pokud je nádor malý, může být odstraněn chirurgickým zákrokem zvaným lokální excize, která odstraňuje pouze rakovinnou oblast. Pacienti s onemocněním fáze 0 a I jsou obvykle léčeni pouze chirurgicky.,
větší nádor vyžaduje resekci (odstranění nádoru a některé zdravé tkáně, která ho obklopuje) a anastomózu (dva konce střeva bez nádoru jsou znovu připojeny). Pokud nelze konce střev znovu připojit, provede se kolostomie.
nejčastějším chirurgickým zákrokem je celková mezorektální excize nebo TME. Tato operace odstraňuje konečník a mezorektum, oblast tukové tkáně pod konečníkem, která obsahuje lymfatické uzliny. Toto je nejčastější oblast pro šíření rakoviny. Počet pacientů vyžadujících kolostomii s touto operací je nízký., TME spolu s neoadjuvantní chemoradiací (podávanou před chirurgickým zákrokem) vedlo ke snížení recidiv v oblasti konečníku.
chirurgové používali k resekci břicha (nazývané abdomino-perineální resekce nebo APR). Dnes se TME nejčastěji provádí s nízkou přední resekcí (LAR), která obvykle umožňuje, aby rektální svěrač zůstal neporušený.
v některých případech, i když je chirurg schopen odstranit všechny viditelné nádory, může být doporučena chemoterapie a/nebo radiační terapie, aby se zabránilo návratu rakoviny (nazývaná recidiva)., Tato doporučení jsou založena na tom, co patolog zjistí při zkoumání nádoru pod mikroskopem, včetně, pokud okraje vzorku jsou bez nádoru, velikost nádoru, a pokud žádné krevní cévy nebo lymfatické uzliny jsou zapojeny.
normální konečník působí jako přidržovací plocha pro stolici. Pokud je zapotřebí ultra nízká rektální resekce a anastomóza, ztrácí se přidržovací oblast, což vede k častějším pohybům střev a/nebo inkontinenci. Abychom tomuto problému pomohli, byl vyvinut kolonický J-vak., Tento postup používá zbývající střevo k vytvoření sáčku ve tvaru J, který pak působí jako nová přidržovací plocha pro stolici. To je obvykle asi 5-6 cm na délku a snižuje počet střevních pohybů a inkontinence.
radiace a chemoterapie
pacienti s onemocněním fáze II a III mají vysoké riziko recidivy a měli by být léčeni chemoterapií a zářením. To může být provedeno buď před operaci (před operací, také se nazývá neoadjuvantní terapie), nebo ve spojení s post-operativní léčba (po operaci, také se nazývá adjuvantní terapie).,
vzhledem k velké velikosti pánve (kostnatá struktura, ve které leží konečník) je pro chirurga často těžké odstranit dostatek normální okolní tkáně, aby měl okraje bez nádoru. To platí zejména pro větší nádory. Dává chemoradiation pre-operativně může zmenšit nádor, který by nebyl schopen být odstraněny chirurgicky, a proto tito pacienti kandidáty na potenciálně kurativní chirurgický zákrok. Toto je známé jako „downstaging“ nádor., Downstaging s chemoradiation má také povoleno u pacientů s nádory, které by jinak vyžadovaly kolostomii nyní resekce a anastomóza (přepojení střev) po léčbě. Studie prokázaly, že dává fluorouracil (5-FU) nebo kapecitabinem (5FU pro-drug) v kombinaci s radiační terapií (tzv. chemoradiation) před operací (tzv. neoadjuvantní terapie) výsledky v méně krátkodobé a dlouhodobé toxicity a méně recidivy nádoru v oblasti konečníku. Z tohoto důvodu se neoadjuvantní terapie stala standardem péče o rakovinu konečníku.,
léčba metastatického onemocnění (rakovina, která se rozšířila)
doporučení léčby u pacientů s metastatickým onemocněním závisí na tom, zda je pacient vhodný pro intenzivní terapii. Možnosti chemoterapie u pacientů s metastatickým onemocněním závisí na tom, jakou léčbu původně dostávali. Účast v klinických studiích může být doporučena před standardní terapií.
pacientům s karcinomem konečníku ve stadiu IV může být nabídnuta resekce nádoru (chirurgie), záření a/nebo chemoterapie., Někteří pacienti mohou být kandidáty na chirurgickou léčbu rakoviny, která se rozšířila do dalších okolních orgánů(tj. Většina z těchto ošetření se provádí na pomoc příznaky, ale nejsou považovány za léčitelné.
možnosti Chemoterapie u pacientů s pokročilým onemocněním může zahrnovat kombinaci fluorouracil, kapecitabin, leukovorin, irinotekan, oxaliplatina, regorafenib, trifluridine a tipiracil, bevacizumab, panitumumab, cetuximab, nivolumab, ramucirumab, ziv-aflibercept, a pembrolizumab., Bylo zjištěno, že režimy užívající irinotekan nebo oxaliplatinu jsou u těchto pacientů účinnější než samotný fluorouracil a leucovorin.
Bevacizumab, ramucirumab a ziv-aflibercept jsou typy antiangiogenní terapie. Tyto práce blokují receptor vaskulárního endoteliálního růstového faktoru (VEGF). Nádory potřebují živiny, aby přežily a jsou schopny získat tyto živiny pěstováním nových krevních cév. Tento lék funguje tak, že útočí na nové krevní cévy, které nádor vytvořil-jinými slovy odříznutím zdroje potravy. Tato činidla mohou být použita v kombinaci s chemoterapií., Regorafenib je perorální cílená léčba nazývaná inhibitor tyrosinkinázy (TKI). Kináza je enzym, který podporuje růst buněk. Existuje mnoho typů kináz, které řídí různé fáze růstu buněk. Regorafenib se zaměřuje na několik různých receptorů a blokuje růst nádoru a angiogenezi (vývoj přívodu krve do nádoru).
trifluridin a Tipracil (Lonsurf) je orální kombinovaná chemoterapie, která interferuje s DNA nádorových buněk a zabraňuje růstu buněk., Receptor epidermálního růstového faktoru (EGFR) je abnormálně nad exprimován v mnoha rakovinách (včetně nádorů tlustého střeva a konečníku). Inhibice EGFR může mít za následek snížení růstu nádorových buněk a sníženou produkci dalších faktorů odpovědných za metastázy (šíření nádoru). Zdá se, že pacienti bez mutací KRAS (kras wild-type) nejlépe reagují na tuto terapii, a proto mají další možnosti léčby anti-EGFR agenty., Cetuximab (Erbitux), panitumumab (Vectibix) jsou typy monoklonálních protilátek, které se zaměřují na rakovinné buňky specificky, šetřící normální buňky, a proto způsobuje různé nežádoucí účinky, než tradiční chemoterapie. Panitumumab a cetuximab práci tím, že blokuje vazbu pro epidermální růstový faktor EGFR, brání epidermální růstový faktor z práce a zpomalení nebo zastavení růstu rakoviny.
Nivolumab a Pembolizumab jsou typy monoklonálních protilátek, které stimulují imunitní systém k ničení rakovinných buněk., T-buňky jsou typem bílých krvinek, které jsou velmi důležité pro normální fungování imunitního systému. Tyto léky fungují jako forma imunoterapie vazbou na „programované smrti receptor“ (PD1) na T-buněk, ke stimulaci imunitního systému, najít a zabít rakovinné buňky. Tato činidla se používají u nádorů, které vykazovaly nedostatek genů pro opravu nesouladu (MMR) (dMMR) nebo nádorů, které mají vysokou expresi mikrosatelitové nestability (MSI-H).
klinické studie
existují klinické výzkumné studie pro většinu typů rakoviny a pro každou fázi onemocnění., Klinické studie jsou navrženy tak, aby určovaly hodnotu specifických léčebných postupů. Zkoušky jsou často navrženy tak, aby léčbě určité fázi rakoviny, a to buď jako první forma léčby nabídl, nebo jako možnost pro léčbu poté, co jiné typy léčby selhaly pracovat. Mohou být použity k vyhodnocení léků nebo léčby k prevenci rakoviny, k jejímu odhalení dříve nebo k řízení vedlejších účinků. Klinické studie jsou nesmírně důležité pro podporu našich znalostí o této nemoci. Prostřednictvím klinických studií víme, co dnes děláme, a v současné době se testuje mnoho vzrušujících nových terapií., Promluvte si se svým poskytovatelem o účasti na klinických studiích ve vaší oblasti. Můžete také prozkoumat aktuálně otevřené klinické studie pomocí služby Oncolink Clinical Trials Matching Service.
následná péče a přežití
jakmile pacient dokončí léčbu, budou pečlivě sledovány pro opakování., Postupujte podle doporučení po léčbě rakoviny konečníku patří fyzikální vyšetření (včetně digitální rektální vyšetření) každé 3 měsíce po dobu 2 let, poté každých 6 měsíců po dobu 3 let; CEA kontrolovány na úrovni (pokud zvýšené v době stanovení diagnózy) každé 3 měsíce po dobu 2 let, poté každých 6 měsíců po dobu 3 let; a kolonoskopie za 1 rok, s opakováním v 1 roce, pokud abnormální, nebo každé 2-3 roky, pokud ne jsou nalezeny polypy. CT vyšetření pánve se doporučuje každých 6-12 měsíců u pacientů s více lokalizovaným onemocněním., CT vyšetření hrudníku, břicha a pánve se doporučuje každoročně u pacientů s vysokým rizikem recidivy rakoviny tlustého střeva. U pacientů, kteří dokončili léčbu stádiu choroby IV, pánevní CT se doporučuje každých 3-6 měsíců první 2 roky.
Strach z recidivy, finanční dopady léčby rakoviny, problémy zaměstnanosti a strategie zvládání jsou společné emocionální a praktické problémy, s nimiž rektální rakovinu přežili. Váš zdravotnický tým může identifikovat zdroje pro podporu a řízení těchto praktických a emocionálních výzev, kterým čelí během rakoviny a po ní.,
přežití rakoviny je relativně nové zaměření onkologické péče. S více než 15 milionů onkologických pacientů v USA, tam je třeba pomoci pacientům přechod z aktivní léčby na přežití. Co se stane dál, jak se vrátíte k normálu, co byste měli vědět a dělat, abyste žili zdravě? Vymírání plán péče může být prvním krokem v vzdělávat sami o navigaci život po rakovině a pomůže vám zasvěceně komunikovat s poskytovateli zdravotní péče. Vytvořte plán péče o přežití dnes na OncoLink.,
Zdroje pro Další Informace
Rakovina tlustého Střeva Aliance
Rakovina tlustého Střeva Aliance přináší hlas přeživší do boje kolorektálního karcinomu prostřednictvím pacienta, podporu, vzdělávání, výzkumu a advokacie.
boj proti kolorektálnímu karcinomu
poskytuje advokacii, vzdělávání a podporu.
Chris 4 Life Colon Cancer Foundation
poskytuje vzdělávání, podporu a financuje výzkum.
Colon Club
podporuje vzdělávání a povědomí zajímavými a mimo krabici způsoby.,
American Society of Colon a Rektálních Chirurgů
Společnost pro colon a rektálních chirurgů a dalších lékařů specializované na léčbu pacientů s nemocí a poruch, které ovlivňují tlustého střeva, konečníku a řitního otvoru.
Colon-Rectal.com
Lékaři s desítkami let zkušeností a odborných školení v péči o tyto typy problémů přispěly text a obrázky na těchto webových stránkách.
Dodatek: kompletní Staging rakoviny konečníku
Americký Smíšený výbor pro rakovinu (3.,>
|
Regional Lymph Nodes (N) |
Description |
|---|---|
|
NX |
Regional lymph nodes cannot be assessed |
|
N0 |
No regional lymph node metastasis |
|
N1 |
One to three regional lymph nodes are positive (tumor in lymph nodes measuring ≥0.,e positive |
|
N2a |
Four to six regional lymph nodes are positive |
|
N2b |
Seven or more regional lymph nodes are positive |
|
Distant Metastasis (M) |
Description |
|---|---|
|
M0 |
No distant metastasis by imaging, etc.,stasis is identified |
|
M1a |
Metastasis to one site or organ is identified without peritoneal metastasis |
|
M1b |
Metastasis to two or more sites or organs is identified without peritoneal metastasis |
|
M1c |
Metastasis to the peritoneal surface is identified alone or with other site or organ metastases |