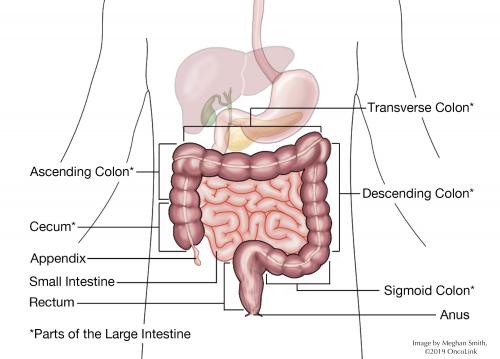
mikä on peräsuoli?
peräsuoli on paksusuolen päässä ja sen pituus on noin 5 tuumaa. Peräsuoli on yleensä tyhjä, paitsi kun uloste tulee ylemmästä paksusuolesta peräsuoleen juuri ennen suolen liikettä. Tuolloin uloste on valmis erittymään peräaukon kanavan kautta. Peräaukkokanavaan on kaksi lihaksikas ”venttiilit” kutsutaan sisäistä ja ulkoista sulkijalihasta. Uloste kulkee näiden sulkijalihasten läpi. Sulkijalihasten avulla voimme säilyttää ulosteen, kunnes olemme valmiita suolen toimintaan., Tällä hetkellä sphincters rentoutua, vapauttaen jakkara.
Mikä on peräsuolen syöpä?
Peräsuolen syöpä on pahanlaatuinen (syöpä) kudosta, joka kasvaa seinän peräsuolen. Kasvaimet alkavat usein, kun normaalin kudoksen peräsuolen seinämän muodostaa adenomatoottisen polyyppi, tai pre-cancerous growth, kasvaa peräsuolen seinän vuori. Kun tämä polyyppi kasvaa suuremmaksi, kasvain muodostuu. Tämä prosessi voi kestää useita vuosia, mikä mahdollistaa varhaisen havaitsemisen seulontatesteillä. Useimmat peräsuolen syövät ovat eräänlainen syöpä kutsutaan adenokarsinooma.,
mikä aiheuttaa peräsuolen syövän ja olenko vaarassa?
joka vuosi arvioidaan, että Yhdysvalloissa todetaan noin 44 180 uutta peräsuolisyöpätapausta. Sitä esiintyy yleensä enemmän miehillä kuin naisilla. Paksusuolen ja peräsuolen syövät on usein ryhmitelty yhteen ja niillä on samat riskitekijät. Diagnoosin keski-ikä on 66 vuotta, ja riski kasvaa iän myötä. Yksilöiden henkilökohtainen tai suvussa paksusuolen syövän tai polyypit, perinnöllinen paksusuolen syöpä oireyhtymät (ts.,, Familiaalinen adenomatoottinen polypoosi (FAP) ja perinnöllinen ei-polypoottinen kolorektaalisyöpä (HNPCC) sekä haavaista koliittia tai Crohnin tautia sairastavat potilaat ovat suuremmassa vaarassa. Nämä potilaat saattavat tarvita seulontaa tavallista väestöä varhaisemmassa iässä. Henkilö yhdellä ensimmäisen asteen sukulaisella (vanhempi, sisarus tai lapsi), jolla paksusuolen syöpä on 2-3 kertaa niin todennäköisesti kehittää syöpä kuten joku, joka ei ole vaikuttanut suhteellinen. Tämä ei kuitenkaan tarkoita, etteivätkö ihmiset, joilla ei ole sukutaustaa, olisi vaarassa., Noin 80 prosenttia uusista kolorektaalisyöpätapauksista todetaan ihmisillä, joita ei tunnistettaisi ”suuririskisiksi”.”
kolorektaalisyöpätapausten tutkimuksissa havaittiin, että tietyt elintapatekijät saattavat nostaa ihmisen riskiä. Näitä tekijöitä ovat:
- runsaasti rasvaa ja punaista lihaa sisältävä ruokavalio.
- ruokavalio alhainen hedelmissä ja vihanneksissa.
- runsaskalorinen saanti.
- vähäinen liikunta.
- lihavuus.
lisäksi tupakoinnilla ja runsaalla alkoholinsaannilla voi olla merkitystä paksusuolen syövän kehittymiseen.,
huolimatta kaikkien näiden tekijöiden välttämisestä joillekin ihmisille kehittyy edelleen paksusuoli-tai peräsuolisyöpä. Seulonnan ja varhaisen havaitsemisen avulla nämä potilaat voidaan parantaa useimmissa tapauksissa.
Miten voin ehkäistä peräsuolen syöpää?
kun otetaan Huomioon riskitekijät lueteltu edellä, vähärasvainen ruokavalio, runsaasti hedelmiä ja kasviksia ja vähän punaista lihaa, säännöllinen liikunta ja säilyttää terveen paino voi auttaa ehkäisemään paksusuolen tai peräsuolen syöpä. Myös tupakointia ja liiallista alkoholinkäyttöä kannattaa välttää.,
termi ”chemoprevention” voidaan määritellä ”käyttö kemiallinen yhdiste estää, estää tai kääntää muodostumista syöpä.”On olemassa tutkimuksia tarkasteltaessa vitamiineja, E, D, ja C, foolihappo, kalsium, seleeni, asetyylisalisyylihappo, cox-2-estäjät, ja hormonikorvaushoito mahdollisina chemopreventive aineita, jotka voivat estää tai kääntää muodostumista polyyppien ja paksusuolen syöpä. Tutkimukset ovat olleet tuloksettomia, eikä väestölle ole annettu erityisiä suosituksia. Joitakin näistä lääkeaineista testataan edelleen kliinisissä tutkimuksissa.,
Mitä seulontatestejä käytetään peräsuolen syöpä?
peräsuolen syövälle ominainen seulontatesti on digitaalinen peräsuolitutkimus (DRE). Aikana DRE, tarjoaja lisätään gloved sormella osaksi potilaan peräsuoleen ja tuntee epänormaali kasvaimet tai ahtaumat (ahtauma). Tutkimukset eivät ole osoittaneet, että seulonta DRE todella vähentää kuolleisuutta peräsuolen syövän. Muut seulontatestit ovat samoja kuin paksusuolen syövän seulonnassa, mukaan lukien ulosteen okkultistinen veritestaus, kolonoskopia ja sigmoidoskopia. Nämä testit seulovat sekä paksusuolen että peräsuolen.,
Jotkut kasvaimet ja polyypit voi vuotaa verta, ja tämä veri voidaan havaita jakkara näytteitä testi kutsutaan ulosteen piilevän veren testaaminen (FOBT). Yksinään FOBT voi löytää vain noin 24 prosenttia syövistä. American Cancer Society suosittelee, että FOBT tehdään joka vuosi sekä joustava sigmoidoskopia 5 vuoden välein, 50 ikävuoden jälkeen. Nämä kaksi testiä osoittavat noin 76% paksusuolen kasvaimia. Sigmoidoskooppi on hoikka, joustava putki, jolla on kyky tarkastella peräsuolta ja paksusuolen alinta osaa., Jos polyyppi tai kasvain löytyy tämän testin, potilas ohjataan täydellinen kolonoskopia.
colonoscope, jota käytetään aikana kolonoskopia, on samanlainen sigmoidoskooppi, mutta on pidempi ja voi tarkastella koko peräsuolen ja paksusuolen. Jos polyyppi löytyy, lääkäri voi poistaa sen ja lähettää sen patologian laboratorioon sen määrittämiseksi, onko se adenomatoottinen (syöpä). Yhdysvaltain Syöpäyhdistys suosittelee kolonoskopian tekemistä 10 vuoden välein 50 ikävuoden jälkeen. Potilailla, joilla on perhe tai henkilöhistoria, pitäisi olla useammin seulontoja., Nämä pitäisi aloittaa iässä, joka on kymmenen vuotta nuorempi kuin heidän sukulaisensa oli diagnoosi. Myös potilailla, joilla on aiemmin ollut haavainen paksusuolitulehdus, on suurempi riski, ja heidän seulontansa tulisi olla yleisempää kuin suuren yleisön. Potilaiden tulee keskustella hoitoryhmänsä kanssa siitä, mikä seulontamenetelmä on heille paras ja kuinka usein se pitäisi tehdä.
Muut seulontatestejä, joka voi havaita syöpä ovat ulosteen immuochemical testi (FIT) ja ulosteen DNA-testit (Cologuard®)., Nämä testit tarjoavat mukavuutta kotitestaus ja minimaalinen Pre-test valmistelu, mutta ei ehkä havaita kaikkia kasvaimia ja ei ehkä kuulu vakuutus. Näitä testejä saavat käyttää vain ne, joilla on alhainen paksusuolen syövän riski ja terveydenhuollon tarjoajan johdolla.
mitkä ovat peräsuolen syövän merkit?
toisin kuin paksusuolen syövät, useimmat peräsuolen syövät aiheuttavat oireita., Näitä ovat: veren puna-ja nähdä ulosteessa, selittämätön ummetus vuorottelevat ripuli, muutokset halkaisija jakkara (potilaat saattavat huomata ”lyijykynä-ohut uloste”), ja tenesmus, joka on tunne tarvitse olla suolen, kun sinulla ei ole ja/tai ei pysty tyhjentämään peräsuoli. Jos kasvaimet ovat edistyneet, ne voivat tunkeutua läheisiin kudoksiin ja aiheuttaa virtsarakon inkontinenssia (kyvyttömyys pitää virtsaa) tai kipua pakaroiden tai välilihan paineen vuoksi.
miten peräsuolen syöpä diagnosoidaan?,
kun peräsuolisyöpä löydetään seulontatesteillä, tarvitaan lisätutkimuksia kasvaimen laajuuden selvittämiseksi. Kasvaimen leviämisen määrittämiseen käytettävät testit ovat CT-kuvat, MRIs ja endoskooppinen ultraääni (EUS). EUS on eräänlainen ultraääni, joka käyttää ääniaaltoja määrittää syvyys kasvain ja onko ympäröivä imusolmukkeet ovat mukana. Biopsia on yleensä tehty aikana EUS, kolonoskopia tai proctoscopy (testi, joka näkee vain peräsuolen alueella), joka mahdollistaa hoidon tarjoajalle määrittää kasvaimen tyyppi., Carcinoembryonic antigeeni (CEA) taso on merkki paksusuolen syöpä, joka on veressä ja on kohonnut 95% tapauksista. Naiset, joilla on kehittynyt kasvaimia, pitäisi myös olla lantion tentti arvioida, jos kasvain on tunkeutunut emättimeen tai kohdunkaula.
edellä mainittujen testien lisäksi kasvainnäyte voidaan lähettää patologian laboratorioon. Tämä voidaan tehdä biopsia näyte tai suurempi näyte, joka poistetaan leikkauksen aikana., Patologi laatii patologian raportin, joka on kirjoitettu raportti, joka antaa sinulle lisätietoja siitä, kasvaimen tyyppi, koko, ja muutoksia nimenomaan teidän kasvain. Patologia useimmiten paljastaa adenokarsinooman.
kudosta koepala tulisi tarkistaa mutaatioita neljä paritonta korjaus (MMR) geenit ja microsatellite epävakaus (MSI). Tämä tulee tehdä kaikissa kolorektaalisyövän vaiheissa. MMR-geenejä ovat MSH2, MLH1, MSH6 ja PSM2. MMR-testauksen poikkeavuudet voivat viitata siihen, että kasvain on ilmennyt periytyvän syöpäoireyhtymän vuoksi., Mikrosatelliitti tapahtuu muutoksia sekvensointi DNA syöpäsoluja tai kyvyttömyys korjata tehtyjä virheitä, kun DNA kopioituu soluun. Kun tämä tapahtuu, sitä kutsutaan mikrosatelliitin epävakaudeksi (MSI). MSI voidaan luokitella MSI high (MSI-H), Microsatellite stable (MSS) tai MSI low (MSI-L). Nämä tiedot voivat auttaa ohjaamaan hoitoa. Metastasoitunutta kolorektaalisyöpää sairastavien potilaiden kasvainkudoksen genotyypitys on tehtävä RAS-mutaatioille, joihin kuuluvat KRAS -, NRAS-ja BRAF-mutaatiot. Nämä tulokset voivat auttaa päättämään hoitovaihtoehdoista.
miten peräsuolen syöpä on lavastettu?,
Lavastus auttaa määrittämään, kuinka pitkälle syöpä on kasvanut ja onko se levinnyt muihin elimiin tai imusolmukkeisiin. Käyttämällä edellä mainittuja testejä, vaihe on päättänyt valita parhaat hoitovaihtoehdot. TNM-järjestelmä (kutsutaan myös kasvain – solmu – etäpesäke järjestelmä) kuvaa koko kasvain (T), jos imusolmukkeet ovat mukana (N), ja jos se on levinnyt muihin kehon alueille (M). Lisäksi kolorektaalisyöpiä voidaan luokitella matala-tai korkea-asteisiksi. Grade keskittyy siihen, miten erilaisilta syöpäsolut näyttävät normaalista solusta., Korkean luokan syövillä on taipumus kasvaa ja levitä nopeammin.
lavastus järjestelmä on hyvin monimutkainen, ja koko lavastus järjestelmä on kuvattu lopussa tämän artikkelin. Vaikka monimutkainen, lavastus järjestelmä auttaa terveydenhuollon tarjoajat määrittää, missä määrin syöpä, ja puolestaan tekevät hoitopäätökset potilaan syöpä. Vaiheessa syöpä, tai missä määrin taudin, perustuu kerättyjen tietojen kautta erilaisia testejä tehty, koska diagnoosi ja työ-ja syöpä on suoritettu.
miten peräsuolisyöpää hoidetaan?,
Leikkaus
viime useita vuosia, on ollut merkittäviä parannuksia kirurginen tekniikoita hoitoon peräsuolen syöpä. Aiemmin suurin osa potilaista tarvitaan kolostomia jälkeen peräsuolen syöpä ja oli merkittäviä sivuvaikutuksia (kuten inkontinenssi ja impotenssi) alkaen hermovaurio, joka esiintyi usein leikkauksen aikana. Hyödyntäminen pre-operative chemoradiation (yhdistelmä kemoterapiaa ja säteily) ja parantaa kirurgisia tekniikoita on johtanut vähemmän sivuvaikutuksia ja vähemmän vaativien potilaiden avanne., Lisäksi preoperatiivinen kemoterapia & säteily (kutsutaan neoadjuvant therapy) voi parantaa onnistumisprosentti kokonaan poistaa kasvain.
leikkaus on yleisin hoito peräsuolen syöpiin. Jos kasvain on pieni, se voidaan poistaa kirurgisen kutsutaan paikallisen poiston, joka poistaa vain syövän alueella. Potilaat, joilla on vaiheen 0 ja I sairaus, hoidetaan tyypillisesti vain leikkauksella.,
suurempi kasvain vaatii resektiota (kasvaimen poisto ja sitä ympäröivä terve kudos) ja anastomoosia (suolen kaksi kasvainta vapaata päätä yhdistetään uudelleen). Jos suolen päätä ei voi kytkeä uudelleen, tehdään kolostomia.
yleisin leikkaus on yhteensä mesorectal excision tai TME. Tämä leikkaus poistaa peräsuolen ja mesorectum, alueen rasvakudoksen alla peräsuolen, joka sisältää imusolmukkeet. Tämä on yleisin syövän levinneisyysalue. Tällä leikkauksella kolostomiaa tarvitsevia potilaita on vähän., TME yhdessä neoadjuvanttikemoradiaation (annetaan ennen leikkausta) kanssa on johtanut uusiutumien vähenemiseen peräsuolen alueella.
Kirurgit tekivät resektion vatsan kautta (kutsutaan abdomino-perineal resektioksi tai APR: ksi). Tänään, TME on useimmiten suoritetaan pieni anteriorinen resektio (LAR), joka tyypillisesti sallii peräsuolen sulkijalihaksen säilyvät.
joissakin tapauksissa, vaikka kirurgi pystyy poistamaan kaikki näkyvä kasvain, kemoterapiaa ja/tai sädehoitoa, saattaa olla suositeltavaa estää syövän tulossa takaisin (kutsutaan uusiutumisen)., Nämä suositukset perustuvat siihen, mitä patologi havaitsee, kun tarkastellaan kasvain mikroskoopilla, mukaan lukien, jos marginaalit näyte on ilmainen kasvain, kasvaimen koon, ja jos jokin verisuonten tai imusolmukkeet ovat mukana.
normaali peräsuoli toimii ulosteen pitoalueena. Kun ultra low peräsuolen resektio ja anastomosis tarvitaan, omistusosuus alue on menetetty, mikä lisää usein suoliston liikkeitä ja/tai inkontinenssi. Tämän ongelman avuksi kehitettiin paksusuolen J-pussi., Tämä menettely käyttää jäljellä suolen luoda J-muotoinen pussi, joka sitten toimii uusi pitoalue jakkara. Se on yleensä noin 5-6 cm pitkä ja vähentää suolen ja inkontinenssi.
Säteily ja Kemoterapiaa
Potilaat, joilla on vaiheen II ja III tauti on suuri riski toistumisen ja pitäisi olla kemoterapiaa ja säteily. Tämä voidaan tehdä joko pre-operatiivisesti (ennen leikkausta, myös kutsutaan neoadjuvant therapy) tai yhdessä leikkauksen jälkeinen hoito (leikkauksen jälkeen, kutsutaan myös adjuvanttihoito).,
Koska suuri koko lantion (luinen rakenne, joka sijaitsee peräsuolen), se on usein vaikea kirurgi poistaa tarpeeksi normaali ympäröivään kudokseen, jotta kasvain-ilmainen marginaalit. Tämä koskee erityisesti suurempia kasvaimia. Antaa chemoradiation pre-operatiivisesti voi kutistua kasvain, joka ei olisi voinut olla poistaa kirurgisesti, ja siksi näiden potilaiden ehdokkaita mahdollisesti parantava leikkaus. Tämä tunnetaan ”downstaging” kasvain., Downstaging kanssa chemoradiation on myös mahdollistanut potilaille, joilla on kasvaimia, jotka muuten vaativat avanne nyt on resektio ja anastomosis (rekonnektio suolen) hoidon jälkeen. Tutkimukset ovat osoittaneet, että antamalla fluorourasiilin (5-FU) tai kapesitabiinin (5FU pro-lääke) samanaikaisesti sädehoidon kanssa (kutsutaan chemoradiation) ennen leikkausta (kutsutaan neoadjuvant therapy) johtaa vähemmän lyhyen ja pitkän aikavälin myrkyllisyyden ja vähemmän uusiutumista kasvain peräsuolen alueella. Tämän vuoksi neoadjuvanttihoidosta on tullut peräsuolen syövän hoidon standardi.,
Hoitoa metastaattiseen sairauteen (syöpä, joka on levinnyt)
Hoito-suosituksia potilailla, joilla on metastasoitunut tauti riippuu siitä, onko potilas on asianmukaista tehohoitoa. Solunsalpaajavaihtoehdot metastasoitunutta tautia sairastaville potilaille riippuvat siitä, millaista hoitoa he alun perin saivat. Kliinisiin tutkimuksiin osallistumista voidaan suositella ennen tavanomaista hoitoa.
potilaille, joilla on vaiheen IV peräsuolisyöpä, voidaan antaa kasvaimen (leikkaus), säteilyn ja / tai kemoterapian resektio., Jotkut potilaat voivat olla ehdokkaita kirurginen hallinta syöpä, joka on levinnyt muihin läheisiin elimiin (eli maksa, munasarjat). Suurin osa näistä hoidoista tehdään oireiden auttamiseksi, mutta niitä ei pidetä parannettavina.
Kemoterapiaa vaihtoehtoja potilaille, joilla on pitkälle edennyt tauti voi sisältää yhdistelmä fluorourasiili, kapesitabiini, leucovorin, irinotekaani, oksaliplatiini, regorafenib, trifluridine ja tipiracil, bevasitsumabia, panitumumabia, setuksimabi, nivolumab, ramucirumab, ziv-aflibersepti, ja pembrolizumab., Irinotekaania tai oksaliplatiinia käytettäessä havaittiin, että fluorourasiili ja leukovoriini olivat näillä potilailla tehokkaampia.
bevasitsumabi, ramusirumabi ja ziv-aflibersepti ovat angiogeenisen hoidon tyyppejä. Nämä vaikuttavat salpaamalla verisuonten endoteelikasvutekijäreseptorin (VEGF). Kasvaimet tarvitsevat ravinteita selviytyäkseen ja pystyvät saamaan nämä ravintoaineet kasvattamalla uusia verisuonia. Tämä lääkitys toimii hyökkäämällä uusia verisuonia kasvain on muodostunut – toisin sanoen katkaisemalla sen ravinnonlähde. Näitä lääkeaineita voidaan käyttää yhdessä solunsalpaajahoidon kanssa., Regorafenibi on suun kautta annettava kohdennettu hoito, jota kutsutaan tyrosiinikinaasin estäjäksi (TKI). Kinaasi on entsyymi, joka edistää solujen kasvua. On olemassa monenlaisia kinaaseja, jotka säätelevät solun kasvun eri vaiheita. Regorafenib tavoitteet useisiin eri reseptoreihin ja estää kasvaimen kasvua ja angiogeneesiä (kehittäminen verenkiertoa kasvain).
Trifluridine ja Tipracil (Lonsurf) on suullinen yhdistelmä kemoterapiaa, joka häiritsee DNA syöpäsoluja ja estää soluja kasvamasta., Epidermaalinen kasvutekijäreseptori (EGFR) on epänormaalisti yli ilmaistu monissa syövissä (mukaan lukien paksusuolen ja peräsuolen). Estämällä EGFR saattaa pienentää kasvaimen solujen kasvua ja tuotanto väheni muut tekijät vastuussa etäpesäke (kasvain levinnyt). Potilaat, joilla ei ole KRAS-mutaatioita (Kras wild-tyyppi), näyttävät reagoivan parhaiten tähän hoitoon, ja siksi heillä on muita hoitovaihtoehtoja EGFR-estäjillä., Setuksimabia (Erbitux) ja panitumumabia (Vectibix) ovat tyypit monoklonaalisia vasta-aineita, jotka kohdistuvat syöpäsolujen erityisesti, säästävät normaalit solut ja näin ollen aiheuttaa erilaisia haittavaikutuksia kuin perinteiset kemoterapia. Panitumumabi ja setuksimabi vaikuttavat estämällä epidermaalisen kasvutekijän sitoutumisen EGFR: ään, estämällä epidermaalisen kasvutekijän toiminnan ja hidastamalla tai pysäyttämällä syövän kasvua.
Nivolumab ja Pembolizumab ovat erilaisia monoklonaalisia vasta-aineita, jotka stimuloivat immuunijärjestelmää tuhoamaan syöpäsoluja., T-solut ovat eräänlainen valkosolujen, jotka ovat erittäin tärkeitä normaalin toiminnan immuunijärjestelmää. Nämä lääkkeet toimivat eräänlaisena immunoterapia sitovat ”ohjelmoitu kuolema-reseptorin” (PD1) löytyy T-solut stimuloivat immuunijärjestelmää, löytää ja tappaa syöpäsoluja. Näitä aineita käytetään kasvaimissa, jotka osoittivat puutetta epäsuhta korjaus (MMR) geenit (DMMR) tai kasvaimia, joilla on korkea ilmentymä mikrosatelliitti epävakautta (MSI-H).
kliiniset tutkimukset
useimmissa syöpätyypeissä ja taudin kaikissa vaiheissa on tehty kliinisiä tutkimuksia., Kliiniset tutkimukset on suunniteltu määrittämään tiettyjen hoitojen arvo. Tutkimuksissa on usein suunniteltu hoitoon jossain vaiheessa syöpään, joko niin, että ensimmäinen muoto hoitoa tarjotaan, tai kuten vaihtoehto hoitoon, kun muut hoidot ovat epäonnistuneet töihin. Niiden avulla voidaan arvioida lääkkeitä tai hoitoja syövän ehkäisemiseksi, havaita se aikaisemmin tai auttaa hallitsemaan sivuvaikutuksia. Kliiniset tutkimukset ovat erittäin tärkeitä edistettäessä tietämystämme tästä taudista. Kliinisten tutkimusten kautta tiedämme, mitä teemme tänään, ja monia jännittäviä uusia hoitomuotoja testataan parhaillaan., Keskustele palveluntarjoajasi kanssa osallistumisesta alueellasi tehtäviin kliinisiin tutkimuksiin. Voit myös tutustua tällä hetkellä avoimiin kliinisiin tutkimuksiin OncoLink Clinical Trials Matching-palvelun avulla.
jatkohoito ja Survivorship
Kun potilas on suorittanut hoito, ne seuraa tarkasti toistumisen., Seurata suosituksia sen jälkeen, kun hoito peräsuolen syöpä ovat fyysinen tentti (mukaan lukien digitaalinen peräsuolesta tentti) 3 kuukauden välein 2 vuoden ajan, sitten joka 6 kuukautta 3 vuotta; CEA taso tarkastetaan (jos koholla diagnoosi) 3 kuukauden välein 2 vuoden ajan, sitten joka 6 kuukautta 3 vuotta; ja kolonoskopia 1 vuosi, toista 1 vuosi, jos epänormaali, tai 2-3 vuoden välein, jos ei polyypit löytyvät. Lantion CT-kuvausta suositellaan 6-12 kuukauden välein potilaille, joilla on paikallisempi sairaus., Rintakehän, vatsan ja lantion TT-kuvausta suositellaan vuosittain potilaille, joilla on suuri paksusuolen syövän uusiutumisen riski. Potilaille, jotka ovat suorittaneet hoidon vaiheen IV taudin hoitoon, suositellaan lantion TT: tä 3-6 kuukauden välein ensimmäisten 2 vuoden ajan.
Pelko toistumisen, taloudellinen vaikutus syövän hoito -, työllisyys-kysymyksiä ja selviytymisstrategioita ovat yleisiä emotionaalinen ja käytännön kysymyksiä kokenut peräsuolen syövän sairastaneet. Sinun terveydenhuollon tiimin voi tunnistaa resursseja, tukea ja hoitoa näiden käytännön ja emotionaalisia haasteita, aikana ja jälkeen syövän.,
syöpäpotilaiden selviytyminen on onkologian hoidon suhteellisen uusi painopiste. Kun pelkästään Yhdysvalloissa on yli 15 miljoonaa syöpään selviytynyttä, on tarpeen auttaa potilaita siirtymään aktiivisesta hoidosta selviytymiseen. Mitä seuraavaksi tapahtuu, miten palautut normaaliksi, mitä sinun pitäisi tietää ja tehdä elääksesi terveellisesti eteenpäin? Survivalorship hoito suunnitelma voi olla ensimmäinen askel kouluttaa itseäsi noin navigoinnin elämän jälkeen syövän ja auttaa sinua kommunikoida asiantuntevasti terveydenhuollon tarjoajien. Luo survivalorship hoito suunnitelma tänään OncoLink.,
Resurssit Lisätietoja
Colon Cancer Alliance
Colon Cancer Alliance tuo ääni eloonjääneet taistelemaan peräsuolen syövän läpi potilaan tuki, koulutuksen, tutkimuksen ja asianajo.
Fight Colorectal Cancer
tarjoaa edunvalvontaa, koulutusta ja tukea.
Chris 4 Life Colon Cancer Foundation
antaa koulutusta, tukea ja rahoittaa tutkimusta.
Paksusuolen Club
– Edistää koulutusta ja tietoisuutta mielenkiintoinen ja kättelyssä tavoin.,
American Society of Paksusuolen ja Peräsuolen Kirurgit
Yhteiskunta paksusuolen ja peräsuolen kirurgit ja muut kirurgit omistettu hoitoon potilailla, joilla on sairauksia ja häiriöitä, jotka vaikuttavat paksusuolen, peräsuolen ja peräaukon.
Colon-Rectal.com
Lääkärit, joilla on vuosikymmenten kokemus ja erikoistuneet koulutus hoitaa tämäntyyppiset ongelmat ovat vaikuttaneet teksti ja kuvat tällä sivustolla.
liite: täydellinen peräsuolen syövän eteneminen
American Joint Committee on Cancer (3.,>
|
Regional Lymph Nodes (N) |
Description |
|---|---|
|
NX |
Regional lymph nodes cannot be assessed |
|
N0 |
No regional lymph node metastasis |
|
N1 |
One to three regional lymph nodes are positive (tumor in lymph nodes measuring ≥0.,e positive |
|
N2a |
Four to six regional lymph nodes are positive |
|
N2b |
Seven or more regional lymph nodes are positive |
|
Distant Metastasis (M) |
Description |
|---|---|
|
M0 |
No distant metastasis by imaging, etc.,stasis is identified |
|
M1a |
Metastasis to one site or organ is identified without peritoneal metastasis |
|
M1b |
Metastasis to two or more sites or organs is identified without peritoneal metastasis |
|
M1c |
Metastasis to the peritoneal surface is identified alone or with other site or organ metastases |