“extractie” verwijst naar de overdracht van verbindingen van een vaste of vloeibare stof naar een ander oplosmiddel of een andere fase. Wanneer een theezakje aan warm water wordt toegevoegd, worden de stoffen die verantwoordelijk zijn voor de smaak en kleur van thee uit de grond in het water geëxtraheerd (figuur 4.1 a). Cafeïnevrije koffie wordt gemaakt met behulp van oplosmiddelen of superkritische kooldioxide om de cafeïne uit koffiebonen te halen., Bakkers gebruiken het extract van vanille, amandel, sinaasappel, citroen en pepermunt in hun gerechten, essences die zijn gewonnen uit plantaardige materialen met behulp van alcohol (figuur 4.1 b).

figuur 4.1: voorbeelden van extractie: a) thee, b) Bakextracten, c) plantaardige pigmenten geëxtraheerd in waterdruppels nadat de sprinklers een gevallen blad op het trottoir raakten.
in het scheikundelaboratorium is het meest gebruikelijk om vloeistof-vloeistofextractie te gebruiken, een proces dat plaatsvindt in een scheidingstrechter (figuur 4.2)., Een oplossing met opgeloste componenten wordt in de trechter geplaatst en een onmengbaar oplosmiddel wordt toegevoegd, resulterend in twee lagen die aan elkaar worden geschud. Het komt het meest voor dat de ene laag waterig is en de andere een organisch oplosmiddel. Componenten worden “geëxtraheerd” wanneer ze van de ene laag naar de andere gaan. De vorm van de scheidingstrechter zorgt voor een efficiënte drainage en scheiding van de twee lagen.
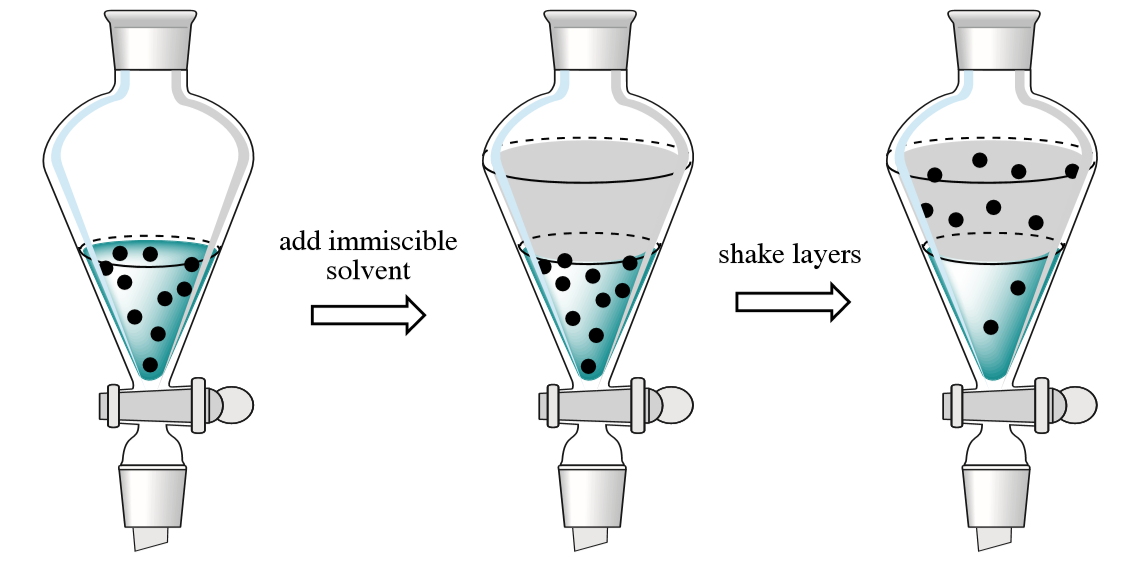
verbindingen verplaatsen van de ene vloeistof naar de andere, afhankelijk van hun relatieve Oplosbaarheid in elke vloeistof. Een korte gids voor oplosbaarheid is het “als lost op als” principe, wat betekent dat niet-polaire verbindingen gemakkelijk in niet-polaire oplosmiddelen moeten worden geëxtraheerd (en vice versa). De stoffen die verantwoordelijk zijn voor de smaak en kleur van thee moeten polair zijn als ze gemakkelijk worden geëxtraheerd in heet water. Wanneer toegestaan om tussen twee vloeistoffen in een scheidingstrechter te equilibreren, eindigt de meerderheid van een verbinding vaak in de laag dat het oplosbaarder is.,
Contributor
-
Lisa Nichols (Butte Community College). Organic Chemistry Laboratory Techniques is gelicenseerd onder een Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International Licentie. Volledige tekst is online beschikbaar.