3) kationy sąsiadujące z atomem z pojedynczą parą elektonów.
ponieważ heteroatomy takie jak tlen i azot są bardziej elektronowe niż węgiel, można się spodziewać, że z definicji będą to grupy wycofujące elektrony, które destabilizują karbokacje. W rzeczywistości często jest odwrotnie: jeśli atom tlenu lub azotu znajduje się we właściwej pozycji, ogólnym efektem jest stabilizacja karbokacji., Wynika to z faktu, że chociaż te heteroatomy są grupami wycofującymi elektrony przez indukcję, to są grupami oddającymi elektrony przez rezonans i to właśnie ten efekt rezonansowy jest silniejszy. (Wcześniej zetknęliśmy się z tym samym pomysłem, rozważając względną kwasowość i zasadowość fenoli i amin aromatycznych w sekcji 7.4)., Rozważmy dwie pary gatunków karbokacji poniżej:
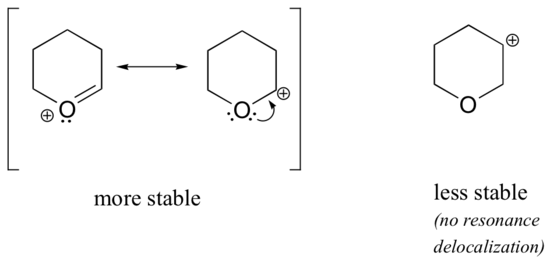
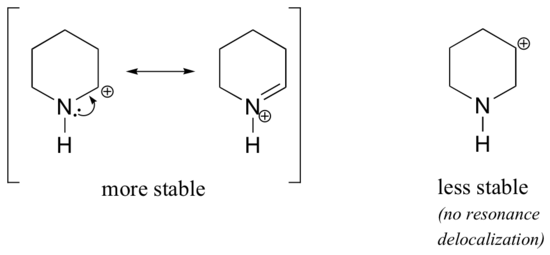
w bardziej stabilnych karbokacjach heteroatom działa jako grupa oddająca elektron poprzez rezonans: w efekcie para samotna na heteroatomie jest dostępna do delokalizacji ładunku dodatniego. W mniej stabilnych karbokationach dodatnio naładowany węgiel znajduje się więcej niż jedno wiązanie od heteroatomu, a zatem nie ma możliwości wystąpienia efektów rezonansowych., W rzeczywistości u tych karbokatomów heteroatomy faktycznie destabilizują ładunek dodatni, ponieważ są elektronami wycofującymi się przez indukcję